Clear Sky Science · sv
WDR5 omformar NANOG-kondensat för att driva transkriptionsprogram och upprätthålla stamcellsidentitet
Varför detta är viktigt för stamceller och cancer
Stamceller har en anmärkningsvärd förmåga att bli många olika celltyper — en egenskap som driver tidig utveckling, vävnadsreparation och, tyvärr, vissa cancerformer. Denna studie avslöjar hur två nyckelproteiner, NANOG och WDR5, samarbetar för att hålla stamceller i detta flexibla tillstånd. Genom att visa att WDR5 fysiskt kan omforma hur NANOG klustrar sig på DNA knyter arbetet ihop fysiken bakom proteindroppar i cellkärnan med genreglering i både friska stamceller och vid leukemi.
Proteiner som bestämmer en cells framtid
Embryonala stamceller förblir pluripotenta — det vill säga kapabla att bli nästan vilken cell som helst — tack vare masterregulatorer som NANOG, OCT4 och SOX2. Dessa proteiner slår på och av hela nätverk av gener. NANOG är särskilt central: det binder inte bara DNA utan rekryterar också stora enzymkomplex som lägger aktiverande kemiska markörer på histoner, proteinerna som packar DNA. WDR5 är en annan avgörande aktör. Det hjälper histonmodifierande maskiner att placera markörer som signalerar aktiva gener. Även om både NANOG och WDR5 är kända för att stödja stamcellsidentitet har det varit oklart hur de kommunicerar på molekylär nivå och om detta påverkar hur de bildar små droppar — eller “kondensat” — i kärnan.
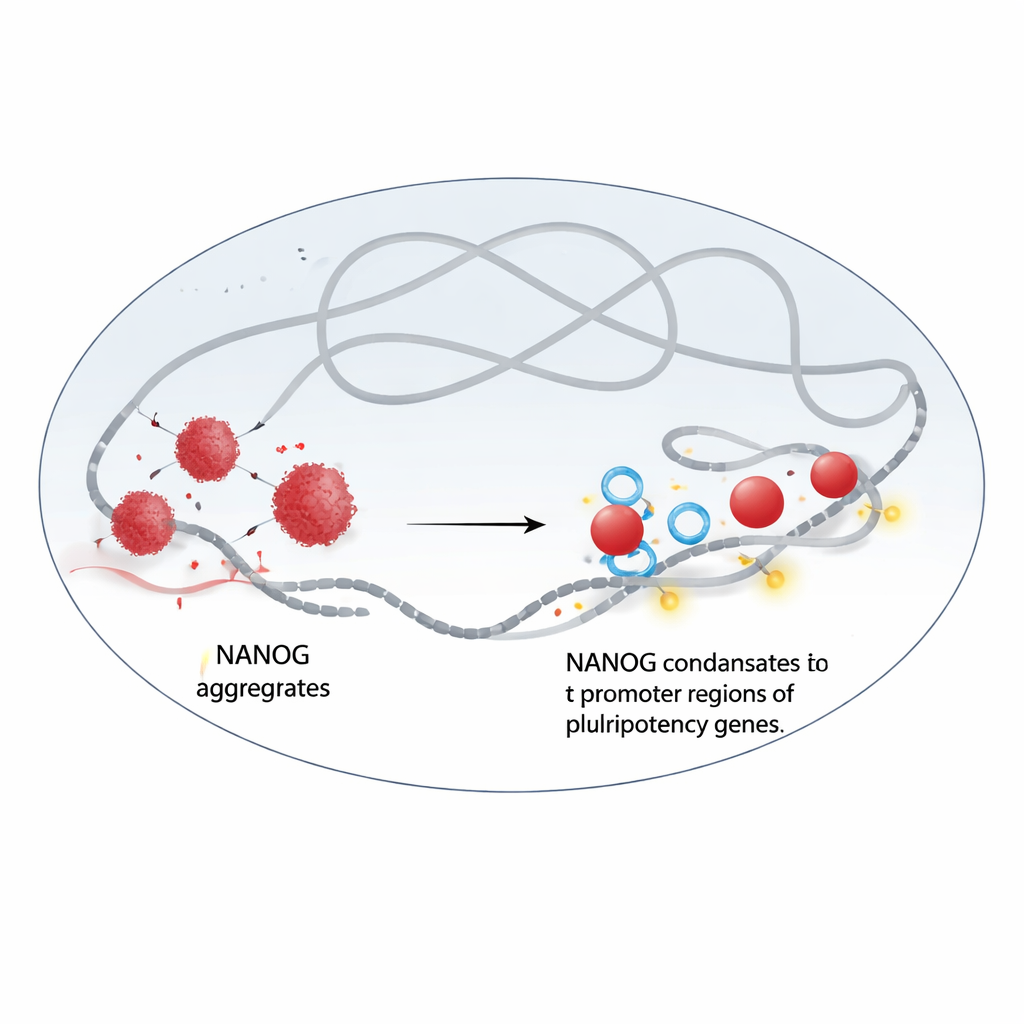
Från klumpar till flytande droppar
Författarna upptäckte att NANOG och WDR5 interagerar direkt. När NANOG renas för sig tenderar det att bilda oregelbundna, solidliknande klumpar. Med hjälp av elektronmikroskopi och fluorescensexperiment visade gruppen att tillsats av WDR5 omorganiserar dessa klumpar till runda, flytande droppar som beter sig som dynamiska kondensat. I levande celler samlas NANOG och WDR5 i ljusa nukleära punkter som snabbt löses upp när de behandlas med en kemikalie som är känd för att störa vätske–vätske-fasseparation. När detta sker förlorar båda proteinerna mycket av sitt grepp om kromatin, DNA–protein-komplexet som lagrar vår genetiska information, och deras närvaro vid nyckelgener för pluripotens sjunker kraftigt.
En särskild molekylär handskakning
För att förstå partnerskapet i atomär detalj bestämde forskarna kristallstrukturen av NANOGs DNA-bindande region bunden till WDR5. Till skillnad från många andra WDR5-partners, som använder korta flexibla slingor, engagerar NANOG WDR5 genom en utsträckt yta som inkluderar både en ostrukturerad arm och närliggande helixar. En enda argininaminosyra i NANOG, vid position 153, tränger djupt in i en central kanal i WDR5 och bildar en nyckelkomponent i ”lås-och-nyckel”-interaktionen. Att byta ut denna rest till alanin (R153A-mutationen) upphäver i stor utsträckning bindningen. Viktigt är att den mutanta NANOG fortfarande kan binda DNA, men WDR5 kan inte längre effektivt omvandla dess aggregat till flytande droppar, vilket visar att denna specifika kontakt är avgörande för att bilda funktionella kondensat.
Att hålla stamceller unga — och vad som händer när det misslyckas
När författarna konstruerade mössens embryonala stamceller så att de endast uttryckte NANOG R153A-mutanten blev konsekvenserna dramatiska. De mutanta cellerna förlorade de täta, kuppelformade kolonier som är typiska för pluripotenta celler och flackade ut, ett visuellt tecken på differentiering. De bildade färre alkalinfosfatas-positiva kolonier, en annan markör för stamcellsegenskaper, och nedreglerade många centrala pluripotensgener såsom Nanog själv, Sox2, Esrrb och Klf4. Samtidigt aktiverades gener förknippade med specifika linjer, inklusive ben- och utvecklingsregulatorer. Genom genome-wide profilering avslöjades att NANOG och WDR5 inte längre samexisterade vid tusentals promotorer, och två viktiga aktiverande histonmarkörer, H3K4me3 och H4K16ac, gick specifikt förlorade vid dessa gemensamma platser. Tidigt under differentieringen sjönk dessa kemiska markörer och nybildade RNA-transkript innan total mRNA-mängd minskade, vilket pekar på ett primärt fel i aktiv kromatinunderhåll.
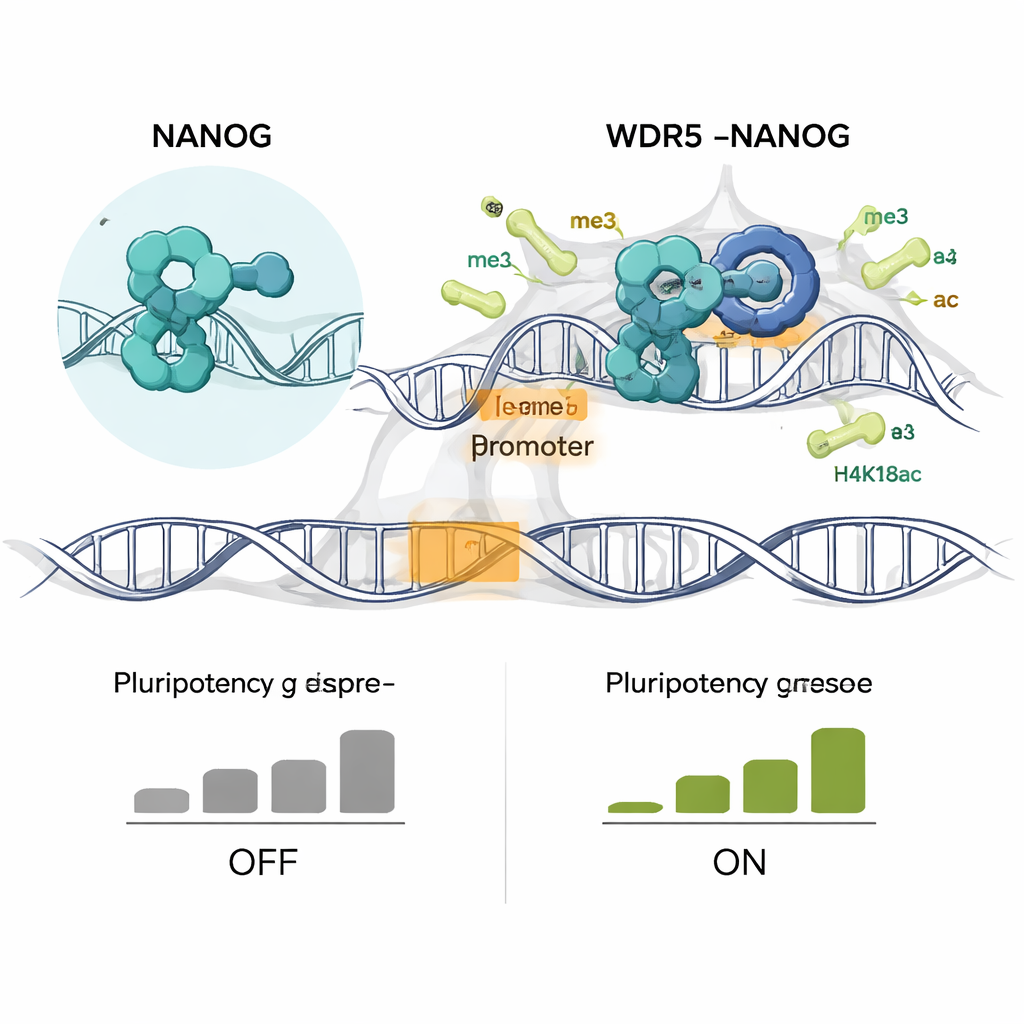
Att omvandla en grundläggande mekanism till en cancerstrategi
Eftersom liknande gennätverk driver vissa cancerstamceller testade gruppen om störning av NANOG–WDR5-axeln kunde dämpa leukemistamceller i en musmodell för akut myeloisk leukemi. En småmolekylär substans, C16, som binder samma WDR5-ficka som NANOG använder, försvagade selektivt WDR5–NANOG-interaktionen. I leukemiceller minskade C16 kraftigt kolonibildning, tömde den stamliknande populationen och pressade cellerna mot mogna myeloida öden, medan normala blodstamceller påverkades betydligt mindre än av ett befintligt leukemiläkemedel som riktar sig mot en annan WDR5-partner. RNA-sekvensering visade att C16 slog av genprogram för stamhet och självförnyelse och förstärkte differentieringsvägar. I möss reducerade C16-behandling leukemi-stam- och progenitorpopulationer, vilket understryker den terapeutiska potentialen i att rikta in sig på detta proteinkomplex.
Större bild: hur droppar hjälper bestämma cellsidentitet
Detta arbete visar att WDR5 gör mer än att sitta på kromatin och rekrytera enzymer: det kan fysiskt omforma NANOG från tröga aggregat till flexibla flytande kondensat som sätter sig på promotorer för pluripotensgener och lockar till sig aktiverande histonmarkörer. När denna omformning blockeras — antingen genom en precis mutation i NANOG eller genom en småmolekyl som stör deras kontakt — förlorar stamceller sin identitet och cancerstamceller tappar sitt grepp om självförnyelse. För en allmän läsare är huvudbudskapet att små förändringar i hur proteiner samlas i droppar på DNA kan få enorma konsekvenser för om en cell förblir ung och flexibel, mognar till en specifik identitet eller driver sjukdom.
Citering: Wang, D., Shi, X., Xie, J. et al. WDR5 remodels NANOG condensates to drive transcriptional programs and sustain stem cell identity. Nat Commun 17, 1907 (2026). https://doi.org/10.1038/s41467-026-68623-w
Nyckelord: stamcellspluripotens, NANOG, WDR5, fasseparation, leukemistamceller