Clear Sky Science · sv
Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa
Hur en sjukhussuperbakterie ändrar sin anfallsstrategi
Pseudomonas aeruginosa är en ökänd sjukhusmikrob som kan orsaka svårbehandlade lung- och sårinfektioner, särskilt hos sårbara patienter. Den överlever genom att växla mellan två levnadssätt: en skyddad, långsamt växande gemenskap kallad biofilm och en snabb, aggressiv form som invaderar vävnader. Denna studie avslöjar hur bakterien själv bestämmer när den ska bryta upp en långvarig biofilm och inleda en plötslig akut attack, vilket pekar ut potentiella nya svagheter för framtida behandlingar.
En mikrobiell tillvaro mellan gömställe och angrepp
Många bakteriella infektioner utvecklas i steg. I ett tidigt skede sprider sig fria, simmande celler genom kroppen och använder kraftfulla verktyg som skadar värdens vävnader. Senare slår de sig ofta ned i biofilmer — tjocka, slemmiga skikt fästa vid ytor som katetrar, lungvävnad eller sår. I dessa samhällen är cellerna inbäddade i en skyddande matris som gör dem svåra att slå ut med antibiotika eller immunsvar. Men biofilmer är inte ett återvändsgränd. Celler kan lämna, återfå rörlighet och tända nya omgångar av akut infektion på andra ställen. Hittills har det varit oklart hur Pseudomonas aeruginosa aktivt koordinerar övergången från kronisk uthållighet tillbaka till aggressiv sjukdom.
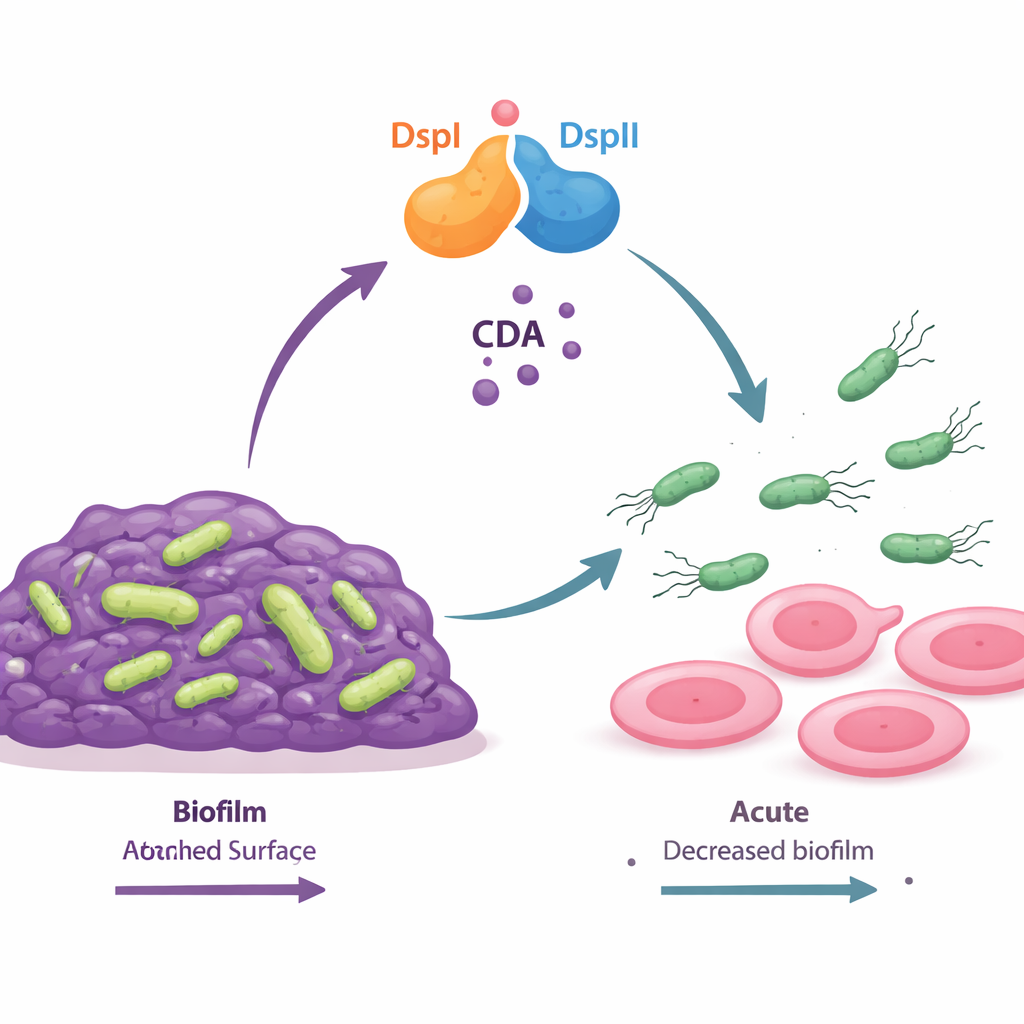
En två-proteinsvipp som tillverkar en kemisk "start"-signal
Författarna fann att två bakteriella proteiner, kallade DspI och DspII, samarbetar som ett slags molekylärt strömbrytare. Båda är enzymer av samma allmänna typ och sitter intill varandra i bakteriens genom, och slås på samtidigt när populationen blir tätare. När de bildar ett par tillverkar de en liten fettsyresignal kallad cis-2-decenoic acid (CDA), som tillhör en bredare grupp av kommunikationsmolekyler kända som DSF-signaler. Mutantbakterier som saknade antingen DspI eller DspII kunde inte längre producera CDA, bildade ovanligt tjocka biofilmer och förlorade förmågan att svärma över ytor. Först när båda proteinerna återställdes tillsammans återfick cellerna normal signalproduktion, biofilmsbrytning och rörlighet, vilket visar att de två enzymerna fungerar som ett ömsesidigt beroende team.
Från kemisk signal till rörelse och undflykt
CDA verkar inte ensam; den kopplar in sig i bakteriens interna kretsar. Forskarna visade att CDA sänker nivåerna av en annan budbärarmolekyl, cykliskt di-GMP, genom att öka aktiviteten hos ett specifikt enzym kallat RbdA som bryter ned denna budbärare. Höga nivåer av cykliskt di-GMP stimulerar normalt biofilmuppbyggnad genom att öka produktionen av slemmande matrix och undertrycka flageller, de små propellrar som driver simning. När CDA finns närvarande faller nivåerna av cykliskt di-GMP, en regulator vid namn FleQ växlar läge, produktionen av klibbiga sockerarter minskar och flagellerna förlängs och förstärks. Som en följd luckras biofilmer upp och cellerna återfår förmågan att röra sig bort och kolonisera nya områden.
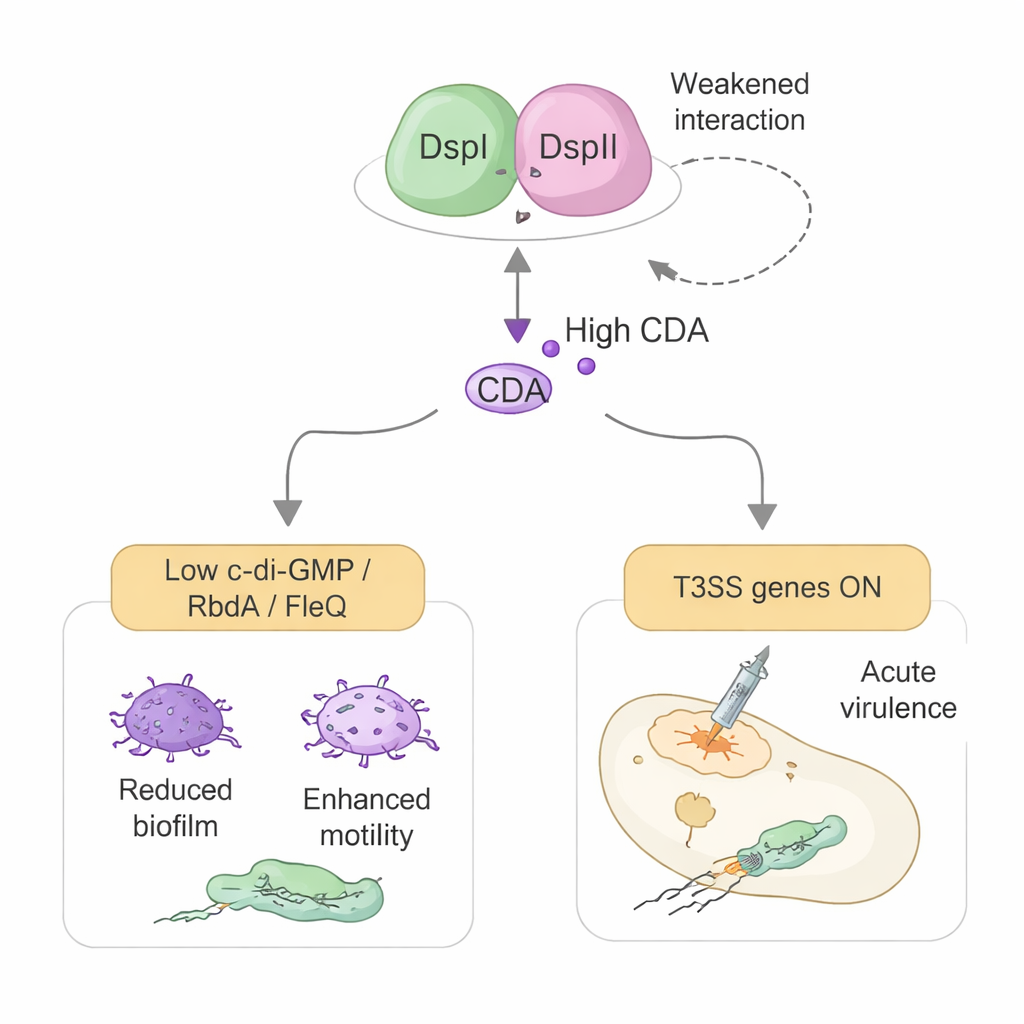
Omskrivning av bakteriers vapenarsenal
Studien avslöjar också en andra, oväntad roll för DspI och DspII som går bortom ren kemi. Samma proteinpar hjälper till att slå på bakteriens typ III-sekretionssystem (T3SS), en sprutliknande apparat som används för att injicera toxiner direkt i värdceller. Istället för att verka via CDA sker denna effekt genom direkt kontroll av genetiska brytare. DspI och DspII dämpar produktionen av två små regulatoriska RNA, RsmY och RsmZ, som normalt stänger av T3SS-proteintillverkning. De gör detta genom att binda till DNA-kontrollregionen för ett av RNA:na och fysiskt interagera med en huvudregulatorprotein kallad GacA. När RsmY och RsmZ hålls i schack frigörs en nedströms aktivator vid namn RsmA och generna för T3SS och dess huvudregulator ExsA slås på, vilket ökar cytotoxicitet i cellkultur och dödlighet i en insektinfektionsmodell.
Ett självjusterande system med läkemedelsmål
Listigt nog är styrkan i DspI–DspII-partnerskapet och dess kontroll över virulens i sig justerad av CDA-nivåer. Vid låga koncentrationer — som de som förväntas i celler som precis lämnar en biofilm — stärker CDA interaktionen mellan de två proteinerna och främjar mer signalproduktion och T3SS-aktivering. Vid höga koncentrationer inne i täta biofilmer försvagar CDA deras samspel och minskar deras bindning till DNA, vilket begränsar fortsatt signalsyntes och kostsam vapenproduktion i celler som stannar kvar. Denna dubbla roll gör DspI–DspII-komplexet till en central nav som länkar populationstäthet, biofilmsflykt och akut virulens. Eftersom störning av komplexet kan blockera både signalproduktion och aktivering av toxinsystemet utgör det ett attraktivt mål för framtida läkemedel som skulle kunna hålla Pseudomonas fast i ett mindre skadligt, kroniskt tillstånd och förhindra farliga uppblossningar.
Citering: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Nyckelord: Pseudomonas aeruginosa, biofilm dispersion, quorum sensing, virulence switch, cis-2-decenoic acid