Clear Sky Science · sv
Dynamisk signatur för aktivitet‑stabilitetsavvägning i lactamas‑evolution
Varför detta är viktigt för antibiotikaresistens
Antibiotikaresistens framstår ofta som en svart låda: bakterier förändras "på något sätt" och läkemedel slutar fungera. Den här studien öppnar lådan för ett av världens mest välkända resistensenzym, TEM‑1 β‑laktamas, som hjälper bakterier att bryta ner penicillinliknande antibiotika. Genom att följa hur enzymets form och rörelser förändras när det utvecklas för att träffa nyare läkemedel visar författarna varför mutationer som ökar aktivitet ofta försvagar stabiliteten, och hur evolutionen hittar uppfinningsrika sätt att balansera båda.
Från penicillinkämpe till bredare läkemedelsbrytare
TEM‑1 är ursprungligen mycket bra på att bryta ner äldre penicilliner men svag mot nyare, skrymmande läkemedel som cefotaxim. I många kliniska stammar dyker en enda nyckelmutation kallad G238S upp nära enzymets aktiva yta, facket där antibiotika klyvs. Denna mutation förbättrar dramatiskt enzymets förmåga att förstöra cefotaxim, samtidigt som den bara måttligt försämrar dess ursprungliga penicillinnedbrytning. Författarna visar att G238S inte bara vidgar fickan; den omorganiserar hur flera omgivande slingor och helixar rör sig, och skapar en ny funktionell konformation som bättre rymmer skrymmande läkemedel.
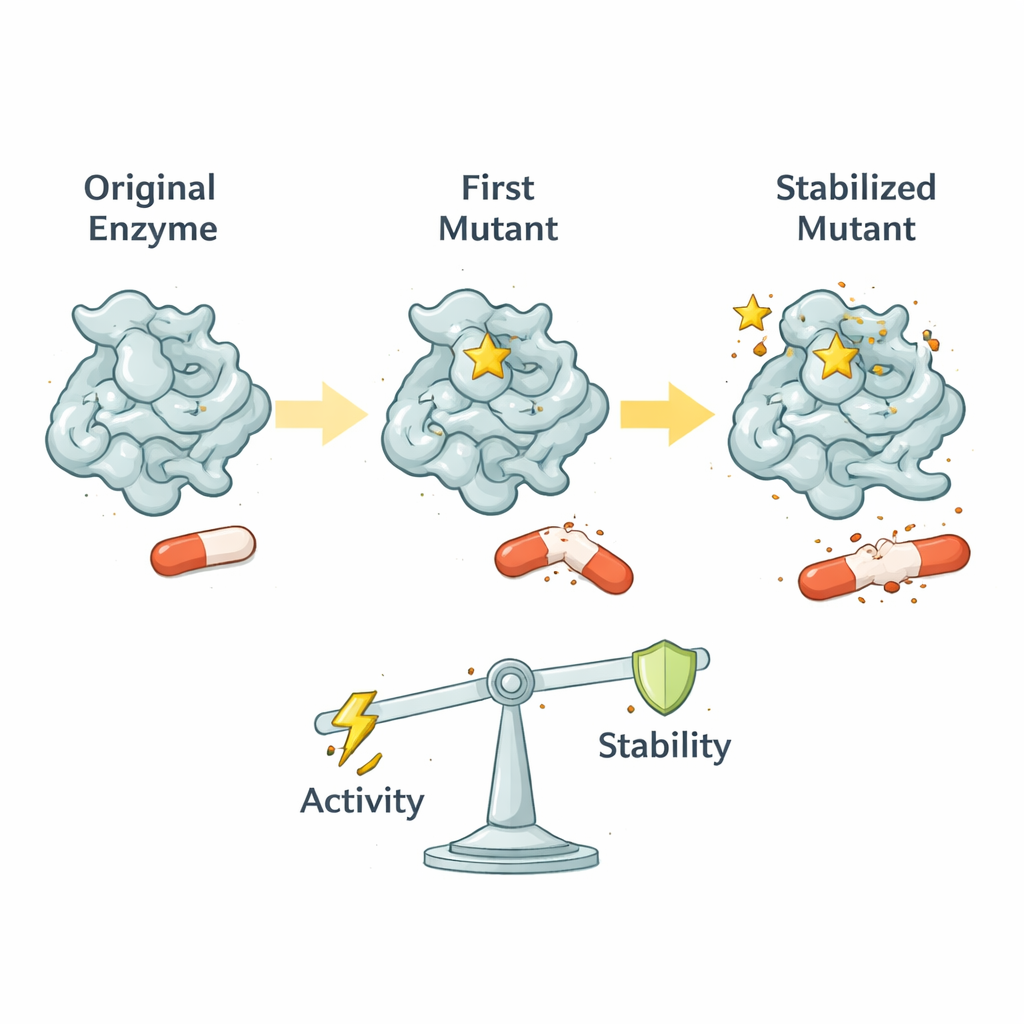
Proteinrörelser som en evolutionsreglknapp
Med avancerade kärnmagnetiska resonans‑(NMR) tekniker mätte forskarna hur olika delar av TEM‑1 rör sig över tidsskalor från biljondels till tusendels sekunder. Vildtypen av TEM‑1 är ganska stel, vilket hjälper den att effektivt bearbeta sina ursprungliga substrat. G238S lämnar större delen av denna snabba styvhet intakt men inför långsammare, noggrant avvägda rörelser i många väggar av det aktiva sätet. Dessa rörelser är tillräckligt snabba för att hålla jämna steg med enzymets kemi men inte så vilda att de stör kritiska katalytiska rester. Resultatet är ett "optimerat fönster" av flexibilitet: precis lagom rörelse för att öppna fickan för cefotaxim, samtidigt som den grundläggande kemiska maskineriet hålls korrekt inriktat.
Att balansera två former istället för att välja en
Evolutionen fryser inte TEM‑1 i en enda ny form. I stället provar enzymet åtminstone två huvudsakliga konformationer: ett "penicillinase"‑tillstånd som liknar den ursprungliga strukturen och ett mer öppet "cefotaximase"‑tillstånd bättre lämpat för nyare läkemedel. Ytterligare mutationer som dyker upp senare, såsom E104K och A42G, gör något subtilt. Istället för att helt enkelt göra den nya, cefotaxim‑vänliga formen mer stabil ombalanserar de blandningen av de två tillstånden. NMR‑data visar att olika delar av det aktiva sätet och det stödjande skelettet kan skifta sina populationer oberoende längs denna tvåtats‑kontinuum. Det leder till en kombinatorisk uppsättning enzymvarianter, var och en med en annan blandning av penicillin‑ och cefotaximliknande konformationer och därmed olika katalytiska profiler.
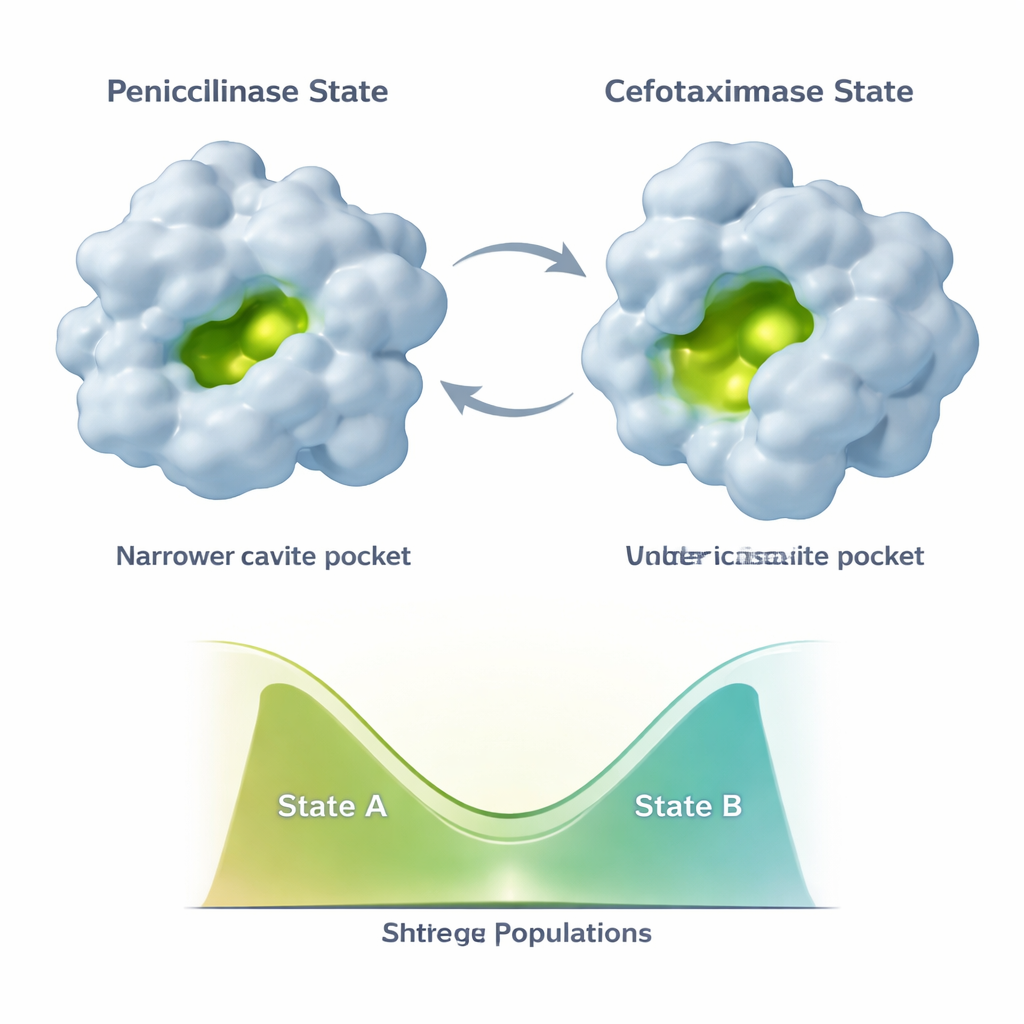
Dolda svaga punkter och långväga reparationer
Mutationer som förbättrar aktiviteten bär ofta en dold kostnad: de gör proteinet mindre stabilt. Istället för att bara titta på fullständig utfällning kartlade teamet lokal stabilitet på nivån av korta segment med väte–deuteriumutbytes‑masspektrometri. G238S visade sig destabilisera inte bara närliggande slingor utan också avlägsna helixar och skivregioner som bildar en strukturell ryggrad. Några av dessa regioner överlappar med ett "kryptiskt" allosteriskt fack—en sällan besökt öppning i proteinets kärna som kan binda små molekyler och dämpa aktiviteten. G238S gör detta fack lättare att öppna, och bygger effektivt in en mild själv‑inhiberande funktion i enzymet. Senare mutationer, särskilt A42G, förstärker detta försvagade ryggnätverk, förbättrar lokal stabilitet runt tre samverkande helixar utan att ta bort de gynnsamma rörelserna i det aktiva sätet. Med andra ord lagar evolutionen avlägsna strukturella svagheter istället för att backa ur den ursprungliga innovationen.
Vad studien avslöjar om evolutionens strategi
För en lekmannaläsare är huvudbudskapet att proteiner som TEM‑1 inte utvecklar resistens genom att trycka en enkel av‑på‑knapp. Varje mutation formar i liten skala hur enzymet andas, böjer sig och delar sin tid mellan olika arbetsposer. G238S öppnar dörren till ett nytt jobb—att bryta nyare antibiotika—men skapar också lokala skörheter och ett delvis själv‑inhiberande tillstånd. Sekundära mutationer fungerar som noggranna förstärkningar, stabiliserar skelettet och finjusterar balansen mellan gamla och nya konformationer så att enzymet kan förbli både aktivt och hållbart. Denna dynamiska syn på evolutionen, där rörelser och lokala svagheter är lika viktiga som statisk struktur, kan hjälpa till att styra designen av framtida antibiotika och läkemedel som riktar sig mot enzymer och som är svårare för bakterier att överlista.
Citering: Arcia, E., Keramisanou, D., Jacobs, L.M.C. et al. Dynamic signature of activity-stability tradeoff in lactamase evolution. Nat Commun 17, 1884 (2026). https://doi.org/10.1038/s41467-026-68620-z
Nyckelord: antibiotikaresistens, beta‑laktamas, proteinevolution, enzymdynamik, proteinstabilitet