Clear Sky Science · sv
Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells
Hur graviditet kan omforma livslång risk för bröstcancer
Varför sänker ett tidigt barnafödande en kvinnas livslånga risk för bröstcancer, medan att bara bli äldre ökar den? Denna studie använder möss för att skåda in i bröstets cellulära ”ekosystem” över tid och jämför djur som aldrig varit dräktiga med de som varit det. Genom att följa hur enskilda celler förändras med ålder och reproduktion avslöjar forskarna en sällsynt, formbytande celltyp som kan bidra till att förklara graviditetens långsiktiga skydd mot bröstcancer.
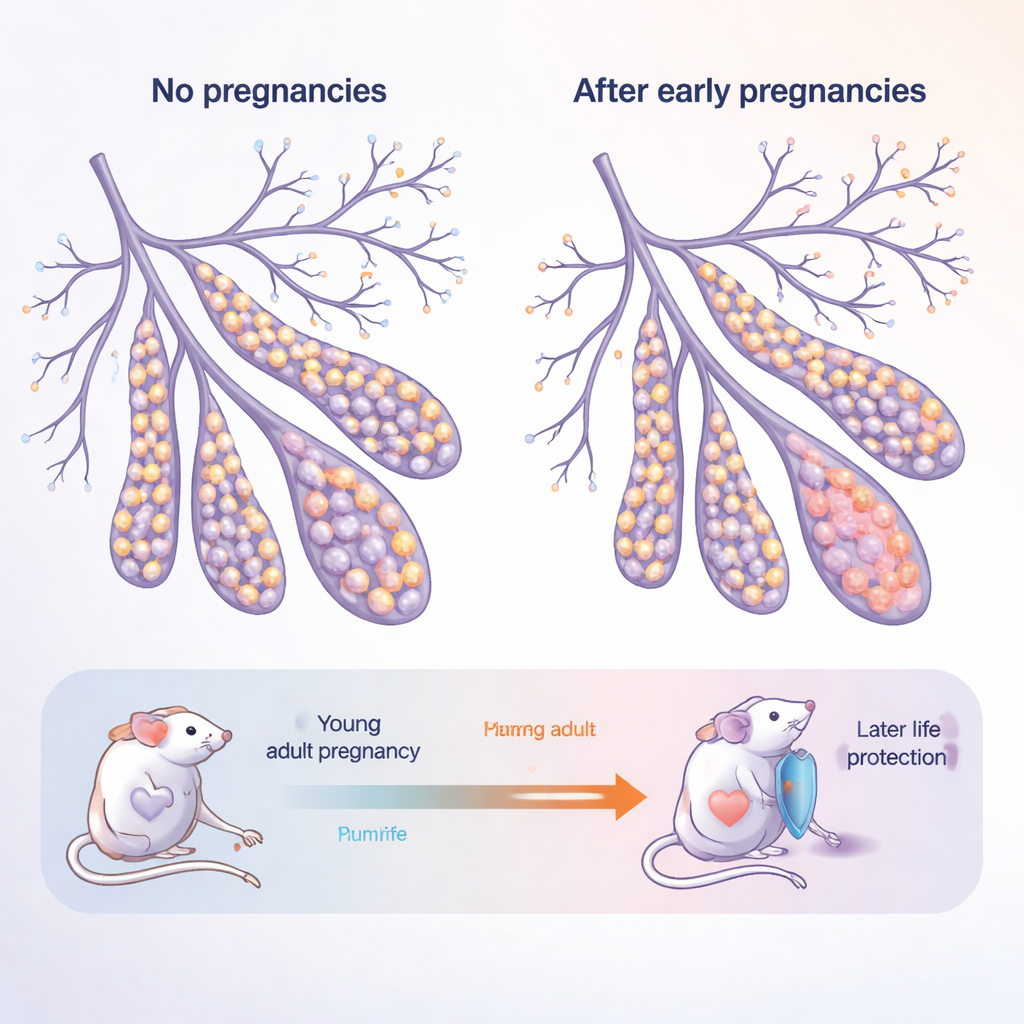
Bröstet som en levande, föränderlig vävnad
Bröstkörteln är inte ett statiskt organ: den växer och ombyggs dramatiskt i puberteten, under graviditet och igen när mjölkproduktionen upphör. Den bygger på två huvudlager av epitelceller som bekläder gångarna: inre ”luminala” celler som kommer i kontakt med mjölk och hormoner, och yttre ”basala” celler som ger struktur och hyser stamcellsliknande celler. Författarna studerade unga vuxna möss och äldre, ”postmenopausala” möss, där varje grupp antingen aldrig varit dräktig (nullipara) eller genomgått flera graviditeter (parous). Denna utformning efterliknar en kvinna som föder i tjugoårsåldern och sedan åldras in i femtioårsåldern och vidare.
Hur åldrande och graviditet drar vävnaden i olika riktningar
När möss åldrades utan att någonsin bli dräktiga skiftade deras bröstkörtlar mot en större andel basala celler och färre luminala celler. Dessa äldre, aldrig dräktiga körtlar producerade också många fler organoider — miniatyr 3D-strukturer odlade från enstaka celler — vilket indikerar att deras celler var ovanligt benägna att proliferera. I kontrast visade möss som genomgått graviditeter en ”normaliserad” balans: det åldersrelaterade uppsvinget av basala celler dämpades, och deras celler bildade färre organoider. Detta tyder på att graviditet lämnar ett bestående avtryck som både förändrar hur celler väljer sitt öde och håller tillbaka deras regenerativa — och potentiellt cancerbenägna — kapacitet.
Upptäckten av hybrida, formbytande celler
För att undersöka djupare användes single-cell RNA-sekvensering för att läsa vilka gener som var aktiva i tusentals enskilda mammaceller. Bland de förväntade luminala, basala, immuna och stromala cellerna fann de en sällsynt grupp som inte passade tydligt in i något av huvudlagren. Dessa celler uttryckte markörer för både luminala och basala linjer, och fick därför namnet ”hybrida” epitelceller. Slående nog ackumulerades dessa hybrider med åldern hos aldrig dräktiga möss men var mycket mindre vanliga hos lika gamla möss som varit gravida. Hybriderna uttryckte starkt en gen kallad Il33, som kodar för signalsubstansen IL‑33, tillsammans med markörer kopplade till tidiga utvecklingsstadier och hög plasticitet — förmågan att byta identitet eller beteende.
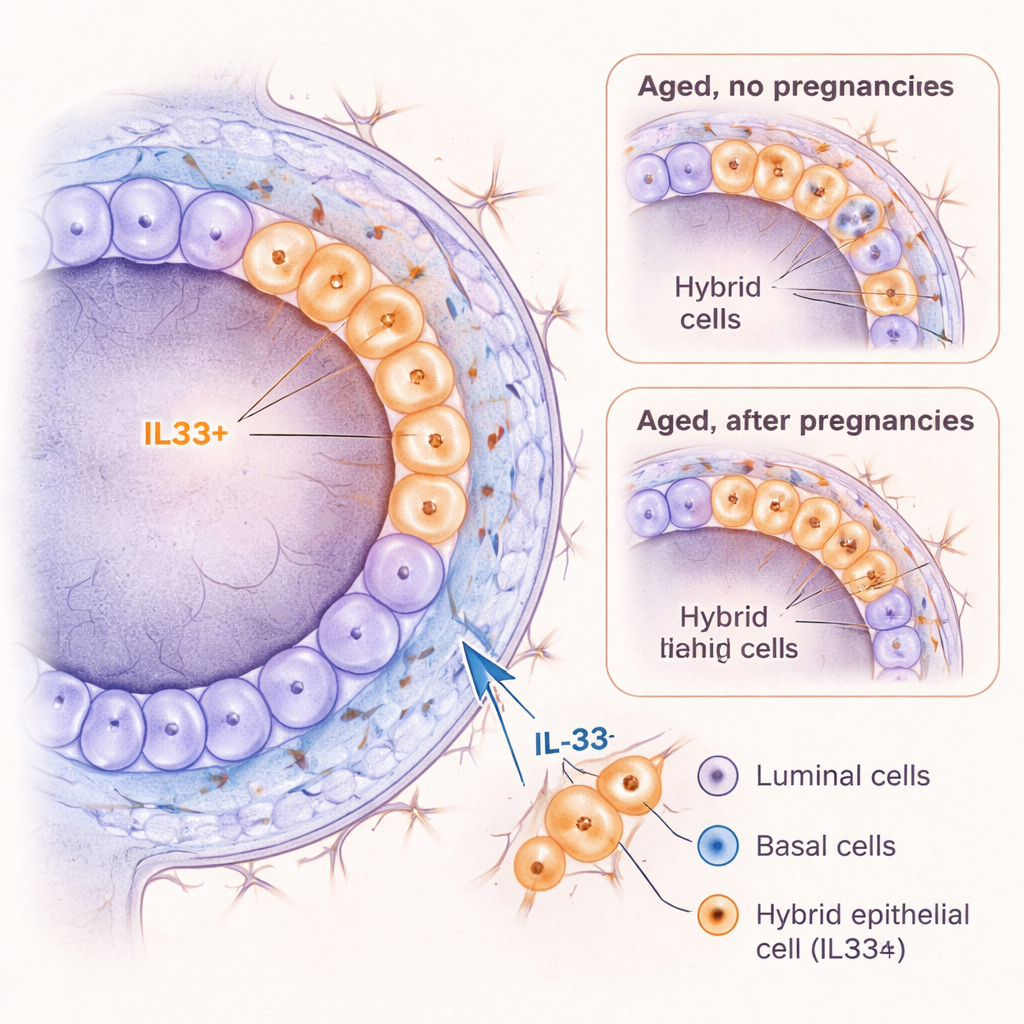
IL‑33 som drivkraft för riskfyllda celltillstånd
Eftersom IL‑33 har kopplats till inflammation och cancer i andra organ frågade forskarna om det aktivt kan pressa mammaceller in i ett hybridliknande tillstånd. När de behandlade unga musemammsceller med IL‑33 i 3D-kultur bildade basallagrets celler fler organoider, behöll en mer primitiv identitet och producerade fler celler med hybridmarkören KRT6A. I levande unga möss orsakade korttidsinjektioner av IL‑33 att gångarna vidgades och utlöste en våg av celldelning, tillsammans med en tillfällig topp av KRT6A-positiva hybrida celler och ett skifte mot fler basallika celler. Viktigt är att när cellerna bar en cancerrelaterad mutation (förlust av tumörsuppressorgen Trp53) ökade IL‑33 ytterligare deras tillväxt. Tillsammans tyder dessa fynd på att IL‑33 bidrar till att skapa ett plastiskt, proliferativt celltillstånd som kan vara särskilt sårbart för att bli canceröst.
Ledtrådar från mänsklig bröstvävnad
För att testa om liknande celler finns hos människor återanalyserade författarna flera stora single-cell-dataset från normal mänsklig bröstvävnad. De identifierade en liten population humana epitelceller som, likt musehybriderna, uppvisade både luminala och basala drag och uttryckte IL33 och relaterade gener. IL33-positiva celler blev vanligare med åldern i flera dataset. I primära humana mammaceller odlade i laboratoriet ökade IL‑33-behandling organoidbildning, försköt cellerna mot en basallik profil och berikade för CD44-positiva celler — en markör som ofta associeras med omogna, stamcellsliknande celler i bröstcancer. Även om tillgängliga humana prover inte tillät ett tydligt test av hur tidig graviditet förändrar denna population, är parallellerna med möss slående.
Vad detta innebär för förståelsen av bröstcancerskydd
För en lekmansläsare är huvudbudskapet att graviditet verkar omkoppla hur bröstvävnad åldras. Hos möss förhindrar en tidig graviditet uppbyggnaden av IL‑33-rika hybrida celler som suddar ut gränsen mellan bröstets huvudcellager och beter sig på ett mycket flexibelt, tillväxtbenäget sätt. IL‑33 själv kan driva celler mot detta riskfyllda, formbytande tillstånd, särskilt när cancerrelaterade mutationer finns. Genom att minska antalet eller uthålligheten hos dessa hybrida celler kan graviditet sänka sannolikheten att åldrande bröstvävnad innehåller fel typ av cell vid fel tidpunkt — en cell som är redo att välta över i cancer. Denna mekanistiska insikt skulle så småningom kunna vägleda strategier för att efterlikna de skyddande effekterna av tidig graviditet utan att kräva en graviditet i sig.
Citering: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
Nyckelord: bröstets åldrande, graviditet och bröstcancer, mammans stamceller, IL-33-signalering, hybrida epitelceller