Clear Sky Science · sv
Utökning av lastens räckvidd i antikropp-läkemedelskonjugat genom leverans av hydroxyinnehållande läkemedel via självimmolativa fosforamidater
Smartare missiler mot cancer
Cancerläkemedel kan vara oerhört effektiva, men de uppträder ofta som ett slags mattbombning: de skadar friska vävnader nästan lika mycket som tumörer. Antikropp–läkemedelskonjugat (ADCs) uppfanns för att lösa detta problem genom att fästa ett potent läkemedel på en antikropp som söker upp cancerceller, vilket omvandlar behandlingen till en styrd missil. Denna artikel förklarar en ny kemisk ”plugg” mellan antikropp och läkemedel som gör dessa missiler både mer precisa och mer flexibla, och som öppnar dörren för många fler typer av cancerläkemedel än vad dagens ADCs kan bära.
Varför dagens riktade läkemedel fortfarande är begränsade
ADCs byggs av tre delar: en antikropp som känner igen en markör på cancerceller, ett giftigt läkemedel (”lasten”) och en kemisk länk som binder ihop dem. De flesta godkända ADCs förlitar sig på bara några få typer av laster som skadar DNA eller blockerar celldelning på liknande sätt. En viktig orsak är länken: den måste hålla läkemedlet stadigt medan ADC:n cirkulerar i blodomloppet, för att sedan släppa det rent när det väl är inne i tumörcellen. Befintliga länkar fungerar bra bara med vissa kemiska grupper på läkemedel, särskilt aminer, och har ofta svårt med de många läkemedel som innehåller alkoholgrupper (–OH). Det betyder att ett stort antal lovande cancerämnen förblir oanvända eftersom de inte kan levereras säkert eller effektivt av nuvarande ADC-designs.
Lånar en metod från antivirala tabletter
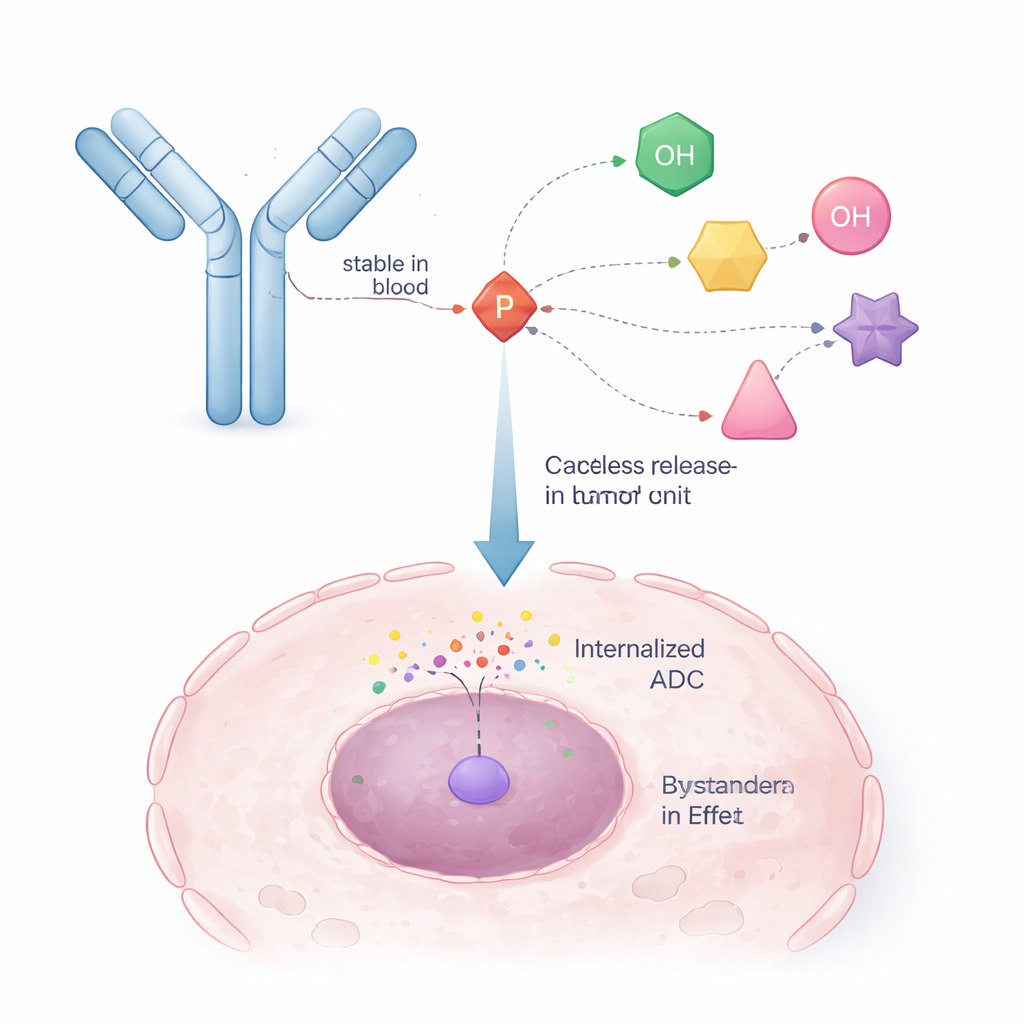
Forskarna vände sig till en strategi som redan bevisats i antivirala läkemedel, kallad ProTides. I dessa läkemedel maskerar en fosforbaserad kemisk enhet tillfälligt en laddad fosfatgrupp så att läkemedlet kan komma in i celler, för att sedan falla sönder inuti och släppa den aktiva formen. Författarna omkonstruerade detta koncept så att en arm av fosforkärnan används för att fästa vid en antikropp, medan de andra armarna håller cancerläkemedlet. Detta skapar en ”självimmolativ” länk: när en intern trigger (till exempel ett enzym i en tumörcell) klipper bort en liten del av strukturen, kollapsar fosforenheten på ett kontrollerat sätt och frigör ursprungliga läkemedelsmolekylen med dess alkoholgrupp återställd och oförändrad.
Att bygga en mångsidig kemisk plugg
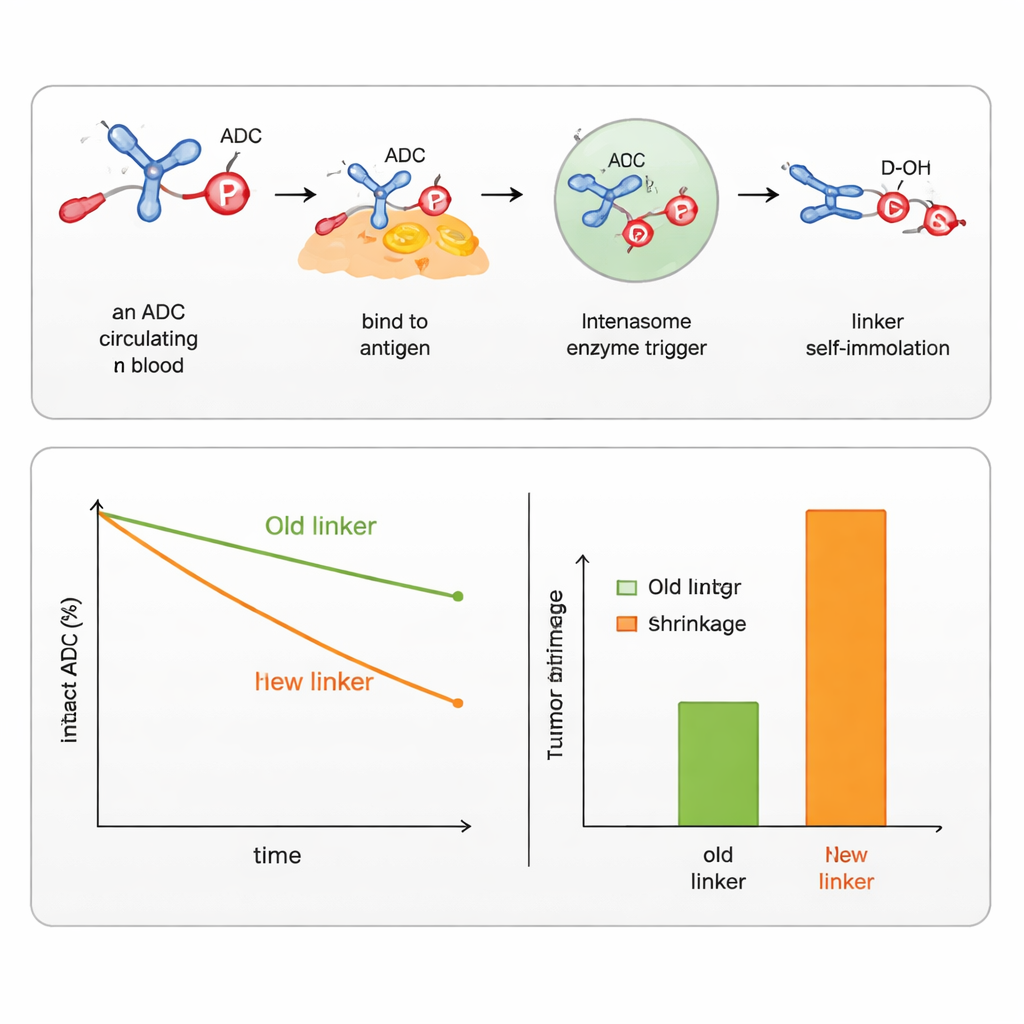
Teamet visade att genom att justera grupperna runt fosforatomen kunde de finjustera hur stabil länken är i blod och hur snabbt den faller sönder inne i celler. De designade versioner som svarar på flera typer av triggers som är vanliga inne i cancerceller, inklusive esteraser och proteaser (enzymer som klyver specifika bindningar), liksom enzymer som känner igen sockerbaserade grupper eller reducerande förhållanden i cellkompartiment. Med dessa konstruktioner lyckades de fästa och frigöra både aromatiska alkoholer (som cytostatikumet SN38) och alifatiska alkoholer (som DXd, lasten i en godkänd ADC mot bröstcancer). Jämfört sida vid sida med befintliga kommersiella länkar för SN38 och DXd höll de nya fosforamidatlänkarna läkemedlen fästa längre i serum, levererade mer läkemedel till tumörer och gav starkare tumörkrympning hos möss, samtidigt som de visade mindre påverkan på friska celler.
Låser upp många nya cancerläkemedelslaster
För att testa hur brett länken kan användas monterade forskarna ADCs som bar tio olika läkemedel som alla innehåller minst en –OH-grupp men verkar på mycket olika sätt inne i cancerceller. Dessa inkluderade hämmare av DNA-syntes, proteinveckning (HSP90), energimetabolism (NAMPT och DHODH) och proteinsyntes, samt välkända ämnen som paklitaxel och gemcitabin. Trots den stora variationen i strukturer kunde de tillverka enhetliga ADCs med hög läkemedelsladdning för samtliga. I cellstudier över flera cancertyper uppvisade de flesta av dessa ADCs nanomolära eller till och med sub-nanomolära potenser och tydlig selektivitet för celler som uttryckte antikroppens mål, vilket bekräftar att länken konsekvent kunde frigöra aktivt läkemedel inne i rätt celler.
Gemcitabin som skyltfönster
Gemcitabin är ett allmänt använt cytostatikum, men i sin konventionella form rensas det så snabbt från kroppen att patienterna måste få stora upprepade doser, vilket begränsar hur mycket som säkert kan ges. Med hjälp av fosforamidatlänken fäste författarna gemcitabin vid en HER2-riktad antikropp i någon av två alkoholpositioner och visade att båda versionerna återfick full aktivitet när de väl var inne i cancercellerna. I musmodeller med HER2-positiva tumörer gav en enda dos av gemcitabin-ADC:n — som innehöll ungefär tusen gånger mindre totalt gemcitabin än typiska fria läkemedelsregimer — stark och selektiv tumörkontroll. ADC:ns beteende i blodomloppet stämde väl överens med den nakna antikroppens, och höga doser tolererades väl hos råttor, vilket antyder en bred säkerhetsmarginal.
Vad detta innebär för framtidens cancerbehandling
För icke-specialister är huvudbudskapet att detta arbete levererar en ny, mycket anpassningsbar kemisk koppling som låter antikroppar bära en mycket bredare uppsättning cancerläkemedel än tidigare, och göra det säkrare. Genom att säkerställa att läkemedel stannar fästa under cirkulationen och frigörs rent först efter att ADC:n tagits in i en cancercell förbättrar fosforamidatlänkar hur mycket läkemedel som når tumören och minskar kollateral skada på friska vävnader. Lika viktigt är att de tillåter befintliga potenta småmolekylära läkemedel — med mycket olika former och verkningsmekanismer — att återanvändas som riktade terapier. Detta kan kraftigt utöka menyn av ADCs som finns tillgängliga för patienter och hjälpa till att bekämpa tumörer som blivit resistenta mot dagens begränsade uppsättning laster.
Citering: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Nyckelord: antikropp–läkemedelskonjugat, leverans av cancerläkemedel, självimmolativa länkar, fosforamidatkemi, riktad cytostatikabehandling