Clear Sky Science · sv
Ligandstyrd regiodivergent och enantioselektiv C–H‑cyanering av sekundära aminer
Varför små bindningsändringar spelar roll för stora läkemedel
Många storsäljande läkemedel innehåller små kvävebaserade byggstenar kallade aminer. Subtila förändringar i hur atomerna är bundna runt dessa aminer kan förvandla ett svagt läkemedel till en potent, precis behandling—eller till något inaktivt eller till och med skadligt. Denna artikel beskriver ett nytt sätt att modifiera dessa aminbyggstenar på begäran, så att kemister kan välja exakt var på molekylen reaktionen ska ske och vilken spegelbildsform som ska bildas, båda viktiga för att designa säkrare och mer effektiva läkemedel.
Välja en plats på en trång molekyl
Aminer i läkemedel har ofta flera mycket likartade kol–väte (C–H)‑bindningar som vanligtvis beter sig nästan likadant. Kemister vill kunna byta ut just en av dessa väten mot en användbar grupp, såsom en cyanogrupp (–CN), utan att störa resten av molekylen. Det är svårt eftersom standardreaktioner tenderar att gå till den mest reaktiva platsen som bestäms av molekylens struktur, inte efter kemistens val. Här arbetar författarna med enkla, flexibla sekundära aminer som bär två olika kolkedjor på kvävet. De visar att man, med samma utgångsamin, kan styra reaktionen till en av två närliggande positioner—antingen intill en liten N‑metylgrupp (den så kallade α′‑platsen) eller en kolatom längre bort på den andra kedjan (β‑platsen)—enbart genom att byta ligand som omger en kopparkatalysator.
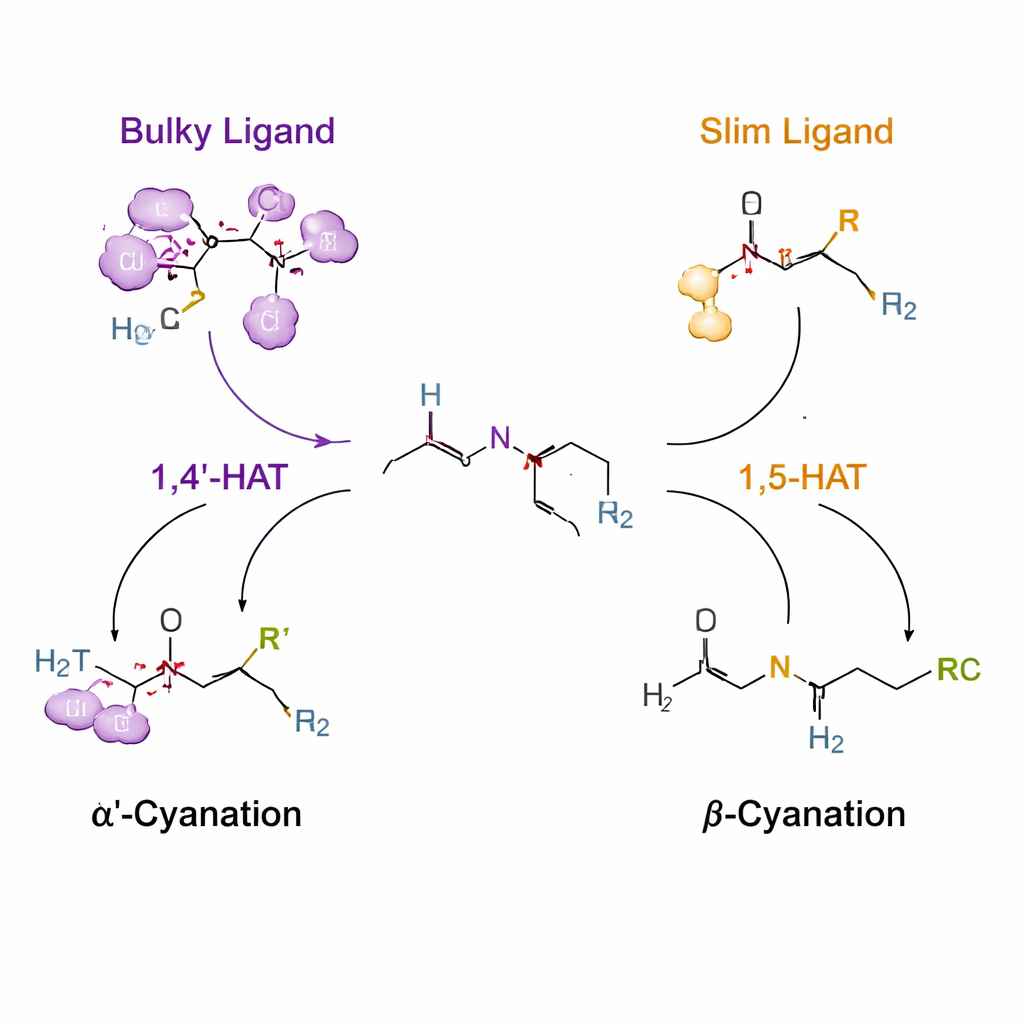
Använda kontrollerade väte‑”hopp” för att styra reaktiviteten
Nyckeltricket bygger på en process kallad väteatomöverföring, där en kortlivad kvävecentrerad radikal rycker åt sig ett väte från ett närliggande kol. Vanligtvis föredrar sådana radikaler en viss räckvidd, med en sexledad ”räckvidd” känd som 1,5‑HAT. Författarna fäster ett temporärt urea‑ och klorhandtag på aminen så att, under kopparkatalys, denna kväveradikal bildas och kan ta väte antingen från α′‑ eller β‑positionen. Genom att utforma ligander—organiska molekyler som omsluter koppar—omformar de radikalens omgivning. En mycket skrymmande ligand (benämnd L14) skjuter systemet mot ett ovanligt 1,4′‑HAT‑steg som riktar sig mot N‑metylgruppen och ger selektiv α′‑cyanering. Smalare ligander (såsom L8) tillåter den konventionella 1,5‑HAT‑vägen och styr istället reaktionen mot β‑positionen.
Från positionskontroll till kontroll av handighet
Utöver att välja var reaktionen sker vill teamet också kontrollera handigheten, eller kiraliteten, vilket är avgörande eftersom många läkemedel förekommer i vänster‑ och högerhänta former som beter sig olika i kroppen. För att uppnå detta introducerar de kirala ligander—molekyler som själva har en handad form—i kopparkomplexet. Två sådana ligander, L24 och L41, ger stark preferens för en spegelbild när reaktionen installerar en cyano grupp i β‑positioner, inklusive både benzylica platser (intill aromatiska ringar) och allylica platser (intill kol‑kol dubbelbindningar). Över en mängd olika aminutgångsmaterial ger metoden β‑cyanerade produkter med utmärkt selektivitet både för plats och handighet, och den fungerar i gram‑skala, vilket visar att processen är praktisk och robust för syntes.
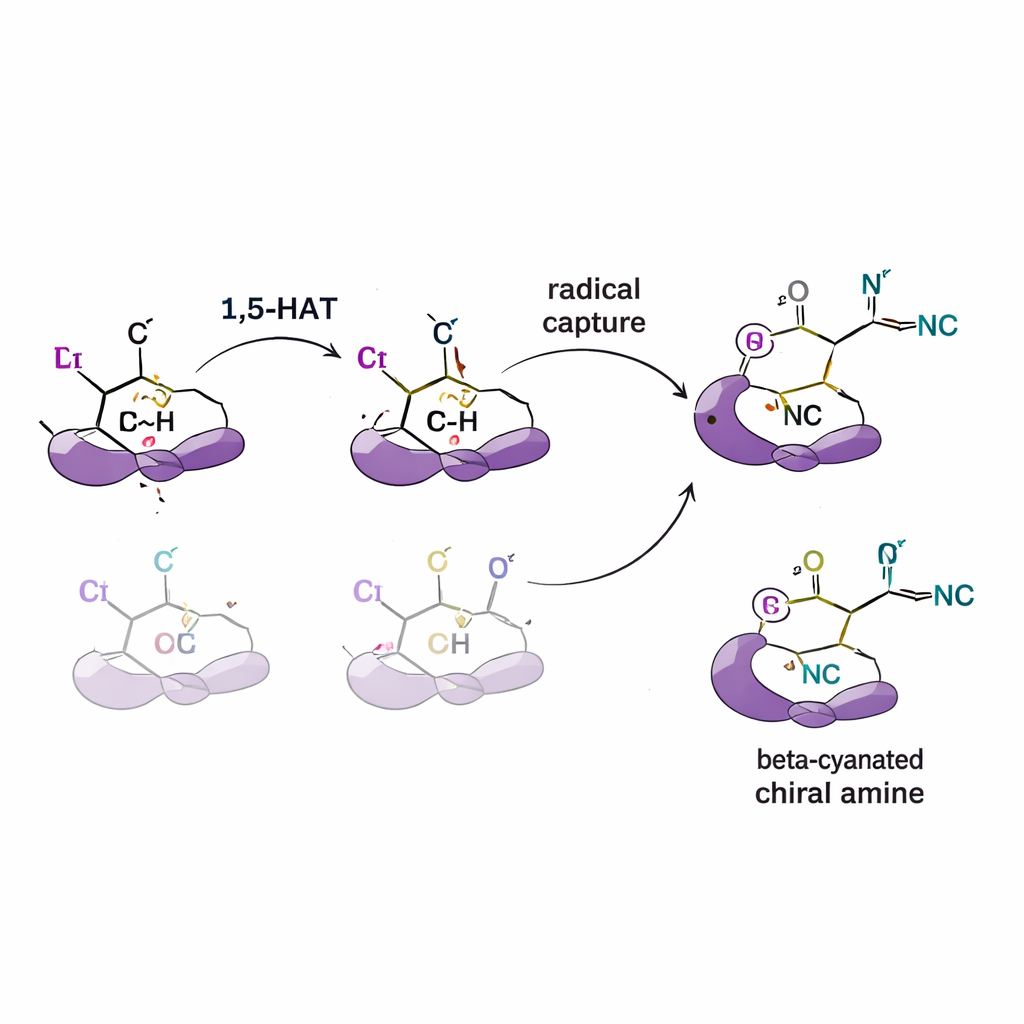
Testa mekanismen bakom selektiviteten
För att ta reda på hur denna kontroll uppstår genomför författarna en serie mekanistiska experiment. Genom att tillsätta radikalfällor bekräftar de att reaktiva radikalintermediärer faktiskt är involverade. Genom att använda substrat där vissa väten är ersatta med deuterium (en tyngre form av väte) detekterar de kinetiska isotopeffekter som pekar på väteöverföringssteget som det långsamma, selektivitetsavgörande steget i reaktionen. Märkningsexperiment visar också att väte förflyttas i ett enda, enkelriktat steg snarare än att skjuts fram och tillbaka mellan positioner. Komplementära datorberäkningar (densitetfunktionalteori) stöder dessa fynd och indikerar att ligandens form och volym ändrar energin hos konkurrerande väteöverföringsvägar och hur radikalen sedan kombinerar med koppar och cyanid för att ge en föredragen spegelbild.
Vad detta betyder för framtida läkemedelsdesign
Sammanfattningsvis introducerar detta arbete en flexibel strategi för att omkonstruera vanliga amingrupper vid två nära besläktade platser, på begäran, med noggrann kontroll över molekylär handighet. Genom att enbart byta ligand på en kopparkatalysator kan kemister välja om en cyano grupp ska placeras på en liten N‑metylenhet eller på den intilliggande kolatomen i en annan sidokedja, och detta kan göras över många komplexa, läkemedelsliknande molekyler. Eftersom cyanogrupper är värdefulla mellanprodukter till många andra funktionella grupper bör denna ”välj‑plats” och ”välj‑hand”‑metod göra det enklare att utforska och optimera nya läkemedel byggda på samma grundläggande aminskyltfonder.
Citering: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Nyckelord: aminfunktionalisering, väteatomöverföring, kopparkatalys, enantioselektiv cyanering, läkemedelskemi