Clear Sky Science · sv
Ett mycket dynamiskt mononukleärt icke‑hem‑järnenzym för tvåstegs biosyntes av isonitriler
Hur bakterier bygger exotiska kemiska verktyg
Isonitriler är små men kraftfulla kemiska grupper som fungerar som en schweizisk armékniv: de kan binda metaller, reagera på många olika sätt och fungerar ofta som "spränghuvudet" i potenta naturliga antibiotika och toxiner. Vissa sjukdomsframkallande bakterier, inklusive tuberkulospatogenen Mycobacterium tuberculosis, fäster isonitriler på fettsyror för att hjälpa dem ta metaller från värden. Den här artikeln undersöker hur ett av deras enzymer, kallat Rv0097, utför denna ovanligt krävande kemi i två noggrant koreograferade steg.
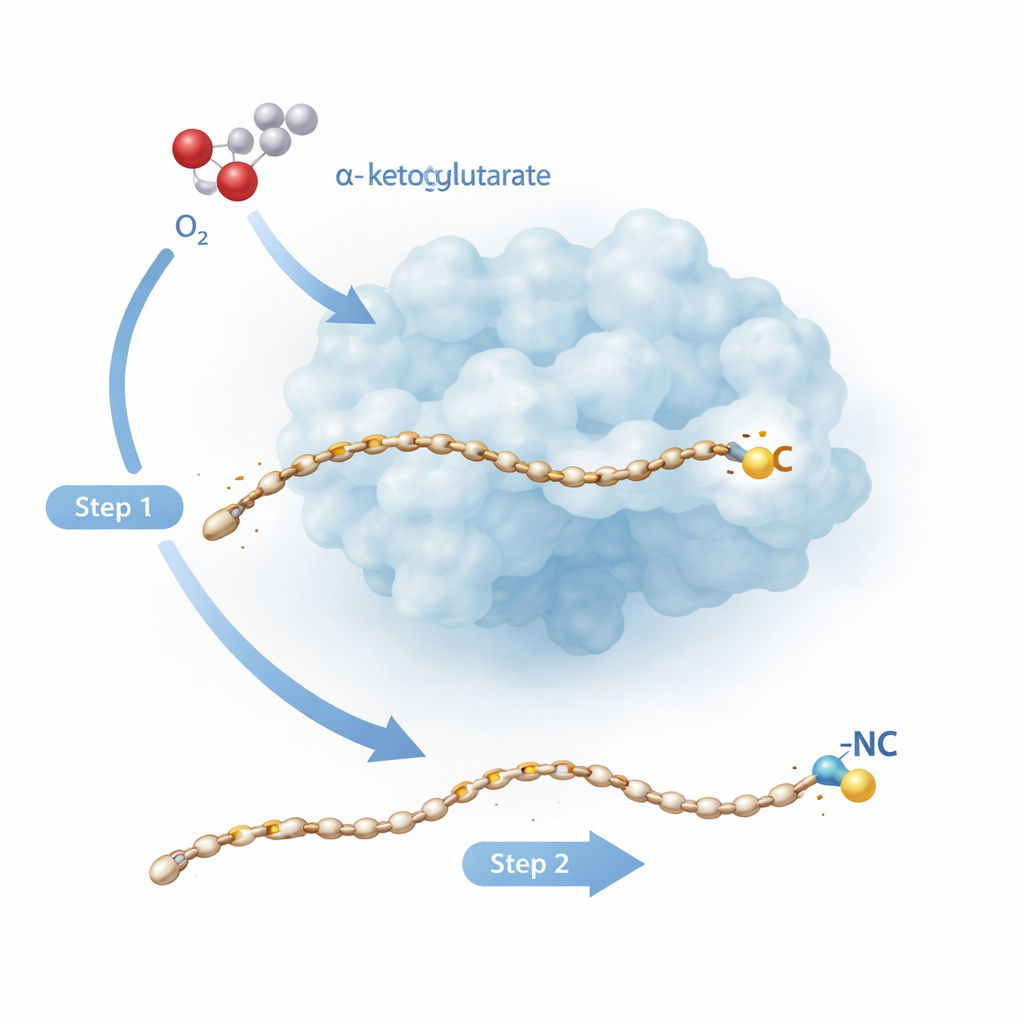
En tvåstegs molekylär omvandling
Rv0097 tillhör en stor familj järnberoende enzymer som normalt utför enklare uppgifter, som att tillsätta syre på en enskild plats i en molekyl. Här är uppgiften svårare: utifrån ett "glycyl–fettsyra"‑byggblock måste enzymet skapa en helt ny isonitrilgrupp, där båda dess viktiga atomer — kolet och kvävet — kommer från samma lilla glycinfragment. Tidigare arbete på ett närbesläktat enzym, ScoE, föreslog att detta inte kan göras i ett enda steg. Istället behövs två separata reaktions"halvcykler", vardera drivna av en järn–syre‑art som bildas när enzymet klyver en hjälpmolekyl, α‑ketoglutarat, och kombinerar den med luftens syre. Den nya studien riktar in sig på tuberkulosenzymet Rv0097 för att i atomär detalj se hur ett enzym kan koppla ihop dessa två radikala steg på samma substrat utan att tappa kontrollen.
Frysa enzymet i akten
Med hjälp av röntgenkristallografi fångade forskarna sexton högupplösta ögonblicksbilder av Rv0097 i olika tillstånd: tomt, bundet till sitt fettsubstrat (en tio‑kols molekyl kallad CADA), bundet till hjälparen α‑ketoglutarat, och i kombinationer som efterliknar flyktiga reaktionsintermediärer. Dessa strukturer visar att Rv0097 har en uppdelad personlighet. I vila är dess aktiva yta mestadels avstängd, med en nyckelaminosyra (fenylalanin 102) som växlar mellan två orienteringar som håller det långa fettsyransfacket torrt och redo för hydrofobt bindande. När CADA binder, snäpper denna rest över i en enda orientering och substratets polära "huvud" förankras av laddade sidokedjor medan dess oljiga svans vilar i en åtsittande tunnel. Mutation av detta grindande par av rester (F102 och en närliggande glycin, G204) blockerar antingen fickan eller släpper in för mycket vatten, vilket skarpt minskar aktiviteten och förändrar vilka kedjelängder enzymet föredrar.
Rörliga lock och dynamiska slingor
Bortom substratfickan beter sig Rv0097 som en liten maskin med rörliga dörrar. Teamet observerade "öppna" och "stängda" konformationer där två lock‑liknande regioner svänger isär eller tillsammans över den aktiva ytan. Öppning blottar järncentret och skapar en väg för α‑ketoglutarat och substratet att komma in; stängning skyddar kemin från omgivande vatten när reaktionen väl är igång. Två flexibla ytslingor, kallade His‑slingan och Arg‑slingan efter histidin respektive arginin de bär, fungerar som en ytterligare grind. I vissa strukturer svänger dessa slingor inåt så att argininresiduen kan gripa α‑ketoglutarat; i andra svänger de utåt och tycks skapa en sidokanalsväg genom vilken använda hjälparfragment (succinat och koldioxid) kan lämna och ett färskt α‑ketoglutarat kan glida in för andra steget — allt medan substrat‑härledda intermediären hålls fast på plats.
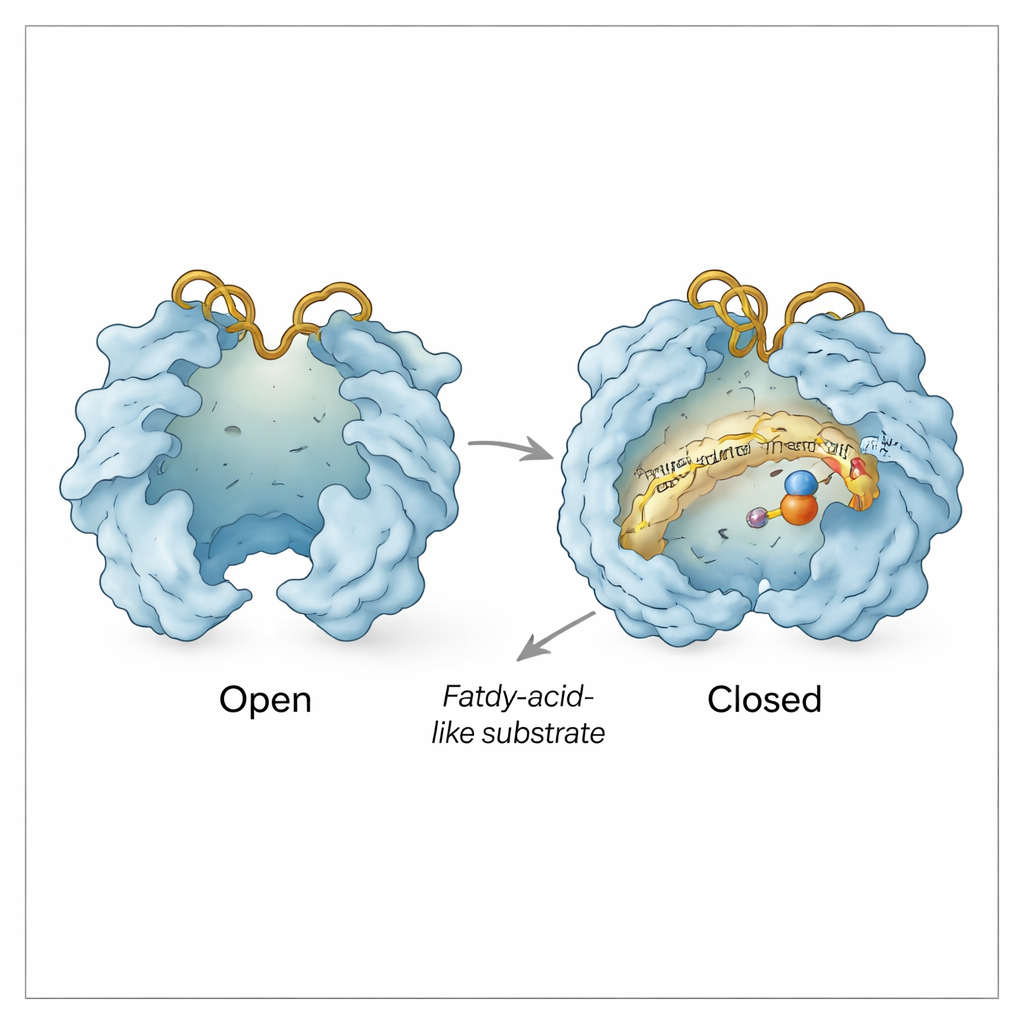
Skydda en skör intermediär
Biokemiska tester stöder denna strukturella bild. Den första halvan av reaktionen omvandlar CADA till en mycket reaktiv iminin‑intermediär som snabbt skulle falla sönder om den drev ut i lösningen. Genom att kemiskt fånga dess sönderfallsprodukt visar författarna att det mesta av denna intermediär endast detekteras när enzymet fortfarande är närvarande, vilket antyder att den förblir bunden och skyddad inne i Rv0097 mellan de två halvreaktionerna. Strukturerna förklarar hur: subtil ompositionering av His‑ och Arg‑slingorna, tillsammans med små förskjutningar av närliggande rester, verkar försegla intermediären i en skyddad kavitet samtidigt som små molekyler som α‑ketoglutarat, succinat och koldioxid kan utbytas genom kontrollerade kanaler.
Varför detta spelar roll för TB och vidare
Tillsammans avslöjar dessa resultat Rv0097 som en starkt dynamisk, en‑proteins monteringslina som använder järnbaserad kemi två gånger i följd på samma substrat utan att någonsin släppa ut en farlig halvprodukt. För tuberkulosbakterier ligger denna precision bakom tillverkningen av isonitril‑dekorerade molekyler som hjälper dem att skaffa nödvändiga metaller i kroppen, och genetiska studier pekar på att vägen är viktig för deras överlevnad under infektion. För kemister och läkemedelsutvecklare ger arbetet en ritning för att konstruera närliggande enzymer som kan bygga nya isonitrilhaltiga föreningar, och antyder att störningar av Rv0097:s rörliga lock och grindar kan vara ett sätt att utveckla nya antibiotika.
Citering: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Nyckelord: biosyntes av isonitriler, icke‑hem‑järnenzym, Mycobacterium tuberculosis, enzymdynamik, metall‑kelaterande naturprodukter