Clear Sky Science · sv
Störning av järnhomeostas ökar känsligheten hos pankreascancer för irreversibel elektroporation
Att vända elektricitet och järn mot en dödlig cancer
Pankreascancer är en av de svåraste cancerformerna att behandla, och även aggressiva lokala behandlingar misslyckas ofta med att hindra att den kommer tillbaka. Denna studie undersöker ett nytt sätt att göra en befintlig procedur — irreversibel elektroporation, som dödar tumörer med korta, kraftiga elektriska pulser — mer effektiv och säkrare. Genom att listigt störa hur cancerceller hanterar järn visar forskarna att de kan pressa överlevande celler in i en destruktiv dödsform, vilket potentiellt minskar risken att tumören återkommer.
Varför elektriska pulser ensamma inte räcker
Irreversibel elektroporation (IRE) behandlar tumörer genom att föra in tunna elektroder i eller runt cancern och avfyra snabba, högspänningspulser. Dessa pulser slår permanenta hål i cellmembran, dödar många cancerceller och väcker en immunrespons. Men det elektriska fältet är inte helt jämnt. Områden som får något svagare pulser kan lämna cancerceller vid liv, och dessa överlevare kan så småningom ge upphov till en ny tumör. När teamet granskade pankreascellinjer och musstumörer som utsatts för ett subletalt elektriskt fält fann de att i stället för att dö via en järndriven process kallad ferroptos, slog dessa celler på ett brett antioxidantförsvar. Nyckelgener för skydd, inklusive de som hjälper till att neutralisera järnrelaterade skador, ökade i uttryck, vilket gjorde det möjligt för cellerna att stå emot och återhämta sig.
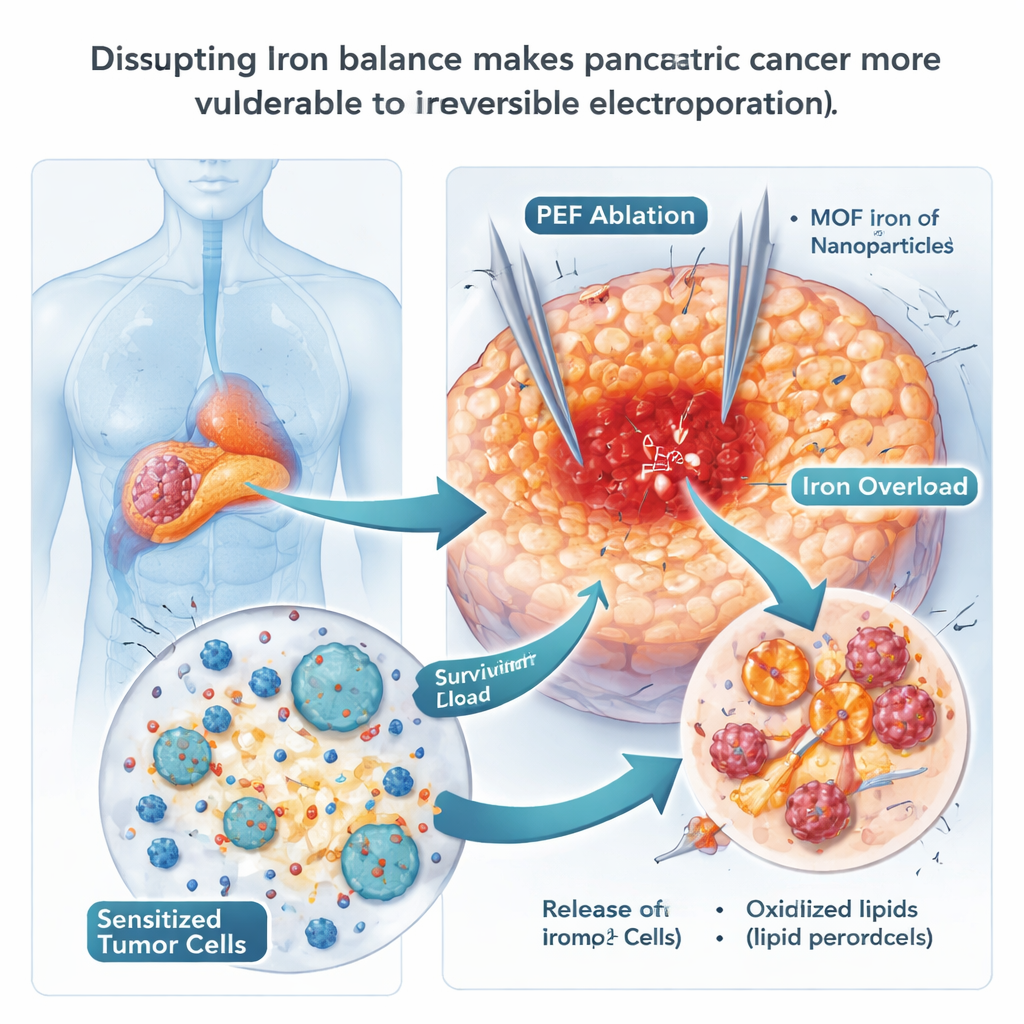
Använda järn-nanopartiklar för att pressa celler mot destruktion
Eftersom ferroptos är beroende av järn testade forskarna om järnrika nanopartiklar kunde tvinga cancerceller över gränsen. De använde specialdesignade metall–organiska ramverkspartiklar innehållande järn (MOF-Fe), som snabbt frisätter järn inne i cellernas sura compartment. I odlingar ackumulerade pankreasceller som tog upp dessa partiklar fritt järn och oxiderade fetter i sina membran — klassiska kännetecken på ferroptos — och bildade mycket färre kolonier. I möss fördröjde kombinationen av MOF-Fe och IRE tumöråterväxt längre än någon av behandlingarna ensam, och tumörerna visade fler tecken på oxidativ skada. Denna fördel var dock tillfällig: efter cirka tre veckor började tumörerna återhämta sig, vilket tyder på att cancern hittat ett sätt att anpassa sig till järnöverskottet.
Att rikta in sig på cellens järn«vals»
För att förstå denna resistens analyserade teamet vilka proteiner som förändrades efter MOF-Fe-behandling. En framträdande kandidat var ferritin heavy chain 1 (FTH1), en del av cellens järnlagringskomplex — det molekylära motsvarigheten till ett brandsäkert kassaskåp för överskott av järn. När FTH1-nivåerna experimentellt höjdes blev cancerceller mer motståndskraftiga mot ferroptos; när FTH1 sänktes blev de mer sårbara. Det pekade på FTH1 som en central sköld mot järndriven död. Forskarna skapade därefter en designer-molekyl, C20U4V, byggd av arakidonsyra (en mycket oxiderbar fett) kopplad till ett PROTAC-stomme som riktar specifika proteiner till cellens avfallshanteringsmaskineri. I närvaro av MOF-Fe bundet C20U4V ferritin och rekryterade det för att märkas och brytas ned, vilket kraftigt minskade FTH1-nivåerna och förhindrade att cellen säkert låste in järnet.
Från cellodlingar till mini-tumörer och möss
När MOF-Fe och C20U4V kombinerades visade pankreasceller högre oxidativ stress, mer skadade membranfetter, sjukare mitokondrier och kraftigt minskad förmåga att återväxa. Denna synergi framträdde också i tredimensionella patienthärledda organoider — små tumörliknande strukturer odlade från verkliga patienter — där läkarkombinationen kollapsade organoidernas storlek och antal. Eftersom C20U4V är oljig och inte löser sig i vatten paketerade teamet den i små, reaktiva-oxygen-känsliga miceller (M-C20U4V) som cirkulerar i blodet och kan frisätta läkemedlet i stressat, skadat tumörvävnad. I musmodeller med pankreastumörer under huden och i själva bukspottkörteln krympte en trippelbehandling med IRE, MOF-Fe och M-C20U4V tumörer mycket mer effektivt och förlängde överlevnaden jämfört med någon enstaka eller dubbel behandling. Behandlade tumörer visade färre delande celler, fler markörer för ferroptos och kraftigare infiltration av T‑celler och andra immunceller, vilket tyder på att strategin inte bara dödar cancerceller direkt utan också hjälper immunsystemet att känna igen och angripa tumören.
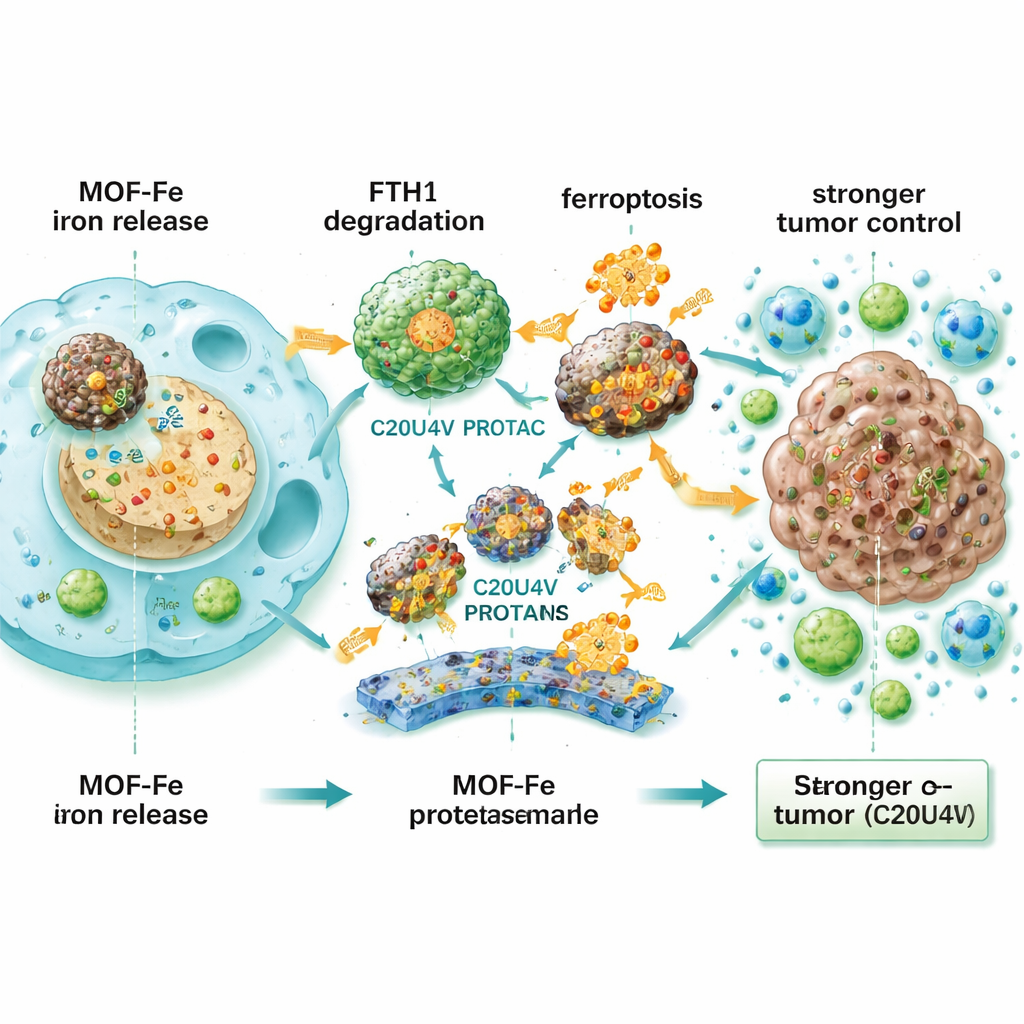
Vad detta kan betyda för patienter
För en icke-specialist är huvudidén enkel: pankreastumörer undkommer ofta efter elektrisk borttagning eftersom vissa cancerceller överlever och snabbt anpassar sig. Detta arbete visar att att lasta dessa celler med järn och samtidigt inaktivera deras järn«valv» kan tvinga dem in i ett självdestruktivt tillstånd som de inte lätt kan motstå. Trots att detta tillvägagångssätt fortfarande är experimentellt och skulle kräva omfattande tester för säkerhet och genomförbarhet hos människor, antyder det att finjustering av hur tumörer hanterar ett grundämne som järn skulle kunna förvandla en ofullkomlig lokal behandling till ett mer avgörande slag mot en av de dödligaste cancerformerna.
Citering: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Nyckelord: pankreascancer, irreversibel elektroporation, ferroptos, järn-nanopartiklar, PROTAC-terapi