Clear Sky Science · sv
Identifiering av Chlamydia pneumoniae och NLRP3-inflammasomaktivering i näthinnan vid Alzheimers sjukdom
Varför bakterier i ögat spelar roll för minnet
Alzheimers sjukdom betraktas vanligtvis som ett problem med plack och trassel i hjärnan. Denna studie antyder att en vanlig lunginflammationsframkallande bakterie, Chlamydia pneumoniae, kan slå sig ner i det ljuskänsliga vävnadsskiktet längst bak i ögat — näthinnan — och bidra till den inflammation och nervskada som ses vid Alzheimers. Eftersom näthinnan kan avbildas icke‑invasivt antyder arbetet att ögonundersökningar en dag skulle kunna hjälpa till att upptäcka infektionskopplade hjärnsjukdomar och styra tidig behandling.
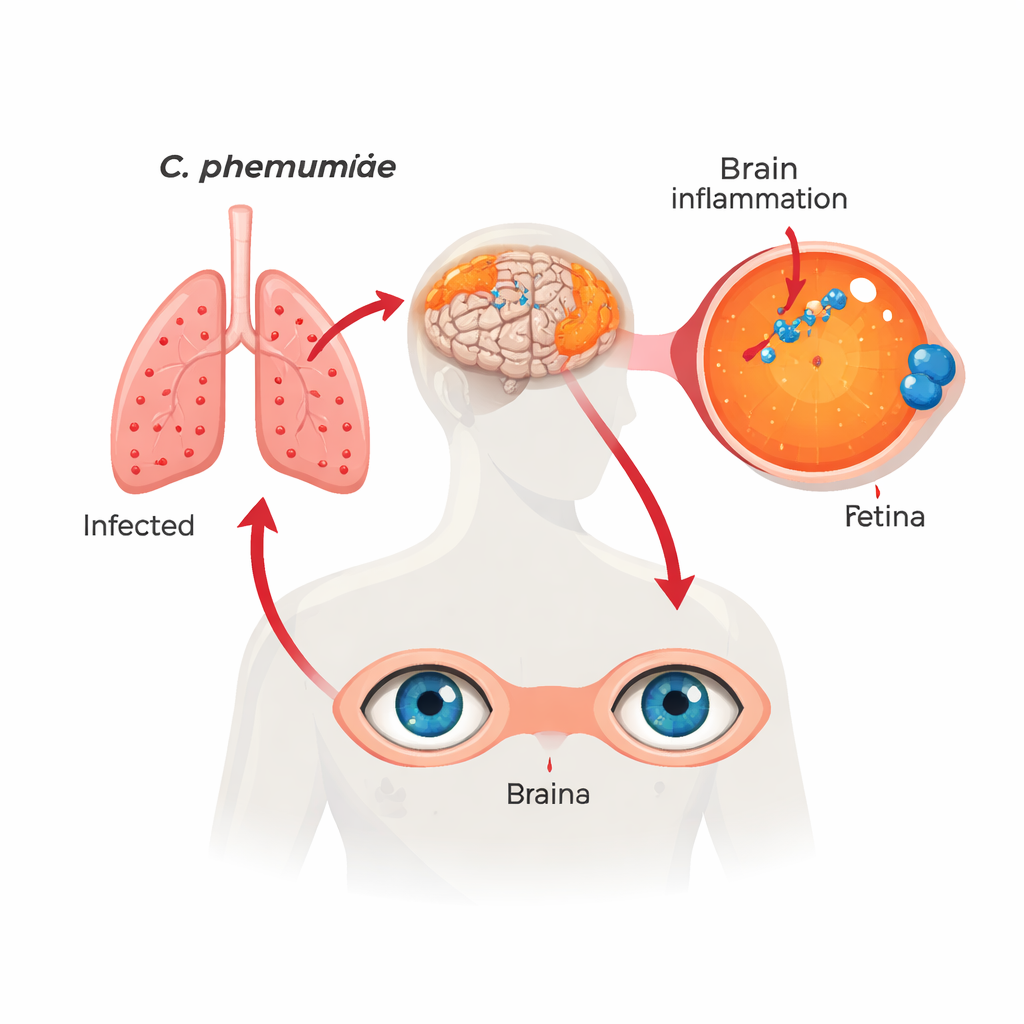
En bekant infektion på en oväntad plats
Forskarna undersökte näthinnor och matchande hjärnprover från över 100 avlidna personer som haft normal kognition, mild kognitiv störning eller Alzheimers demens. Med flera oberoende tekniker — inklusive specifika antikroppar, genetiska prob, färgningsmetoder och DNA‑tester — fann de tydliga tecken på Chlamydia pneumoniae inne i näthinnans celler. Dessa bakteriella ”inklusioner” var vanligast och mest rikliga hos personer med Alzheimers, mindre uttalade hos dem med milda störningar och minst hos dem som förblivit kognitivt normala. Mängden bakterier i näthinnan speglade starkt mängden funnen i hjärnan, vilket tyder på att både öga och hjärna är del av samma långvariga infektion.
Kopplingar mellan bakterier, plack och kognitiv förmåga
Att hitta bakterien var bara det första steget; den avgörande frågan var om den spelade någon roll för sjukdomen. Teamet mätte klassiska Alzheimersmarkörer i samma vävnader. De såg att högre bakteriell belastning i näthinnan sammanföll med fler amyloid‑beta‑avlagringar — det klibbiga proteinet som bildar plack — samt vissa onormala former av tau‑protein. Personer vars hjärnor bar mer bakteriesignal hade också fler nervfibertrassel, sämre total Alzheimers patologi och mer hjärnatrofi. Kliniskt tenderade de med högre bakteriebörda i näthinnan att få sämre resultat på minnes‑ och tänkandetester och hade mer avancerad demens. Bärare av APOE ε4‑genvarianten, en stark genetisk riskfaktor för Alzheimers, hade mer av bakterien i både näthinna och hjärna, vilket antyder en gen‑infektions‑interaktion.
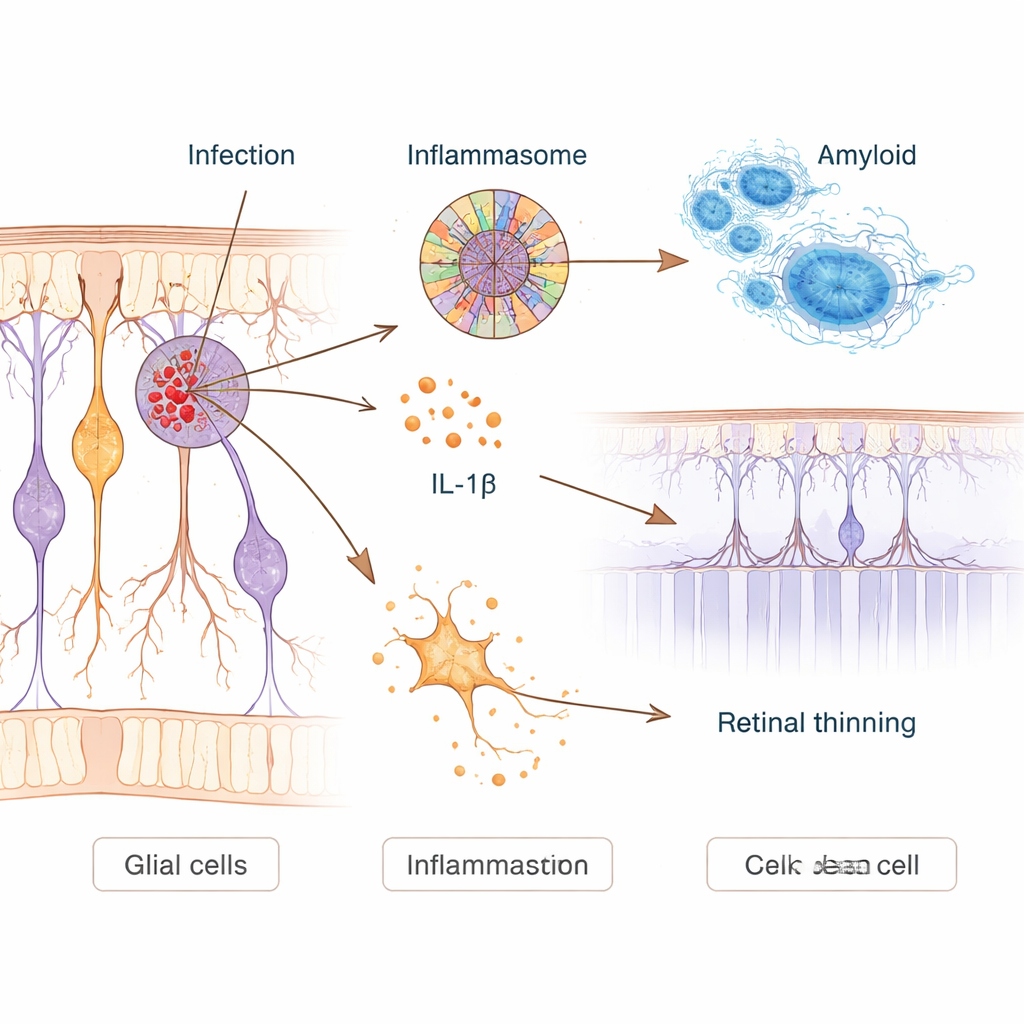
Hur infektion kan utlösa toxisk inflammation
För att undersöka orsak och verkan infekterade forskarna människoliknande nervceller i labbet och Alzheimersmodellmöss med Chlamydia pneumoniae. I odlade neuroner ökade infektionen produktionen av amyloid‑beta och aktiverade ett molekylärt larm som kallas NLRP3‑inflammasom. Detta system fungerar som en cellulär snubbeltråd: när det utlöses släpper det ut inflammatoriska budbärare som interleukin‑1β och kan skapa hål i cellmembran, vilket leder till en explosiv form av celldöd. Infekterade neuroner visade tydliga tecken på membranskador och aktivering av dessa vägar. Hos möss räckte en enda näsdos av bakterien för att den skulle nå hjärnan, där den ökade amyloidplack, aktiverade immunceller och försämrade prestation i minnes‑ och synbaserade labyrintuppgifter månader senare.
Immunförsvaret i näthinnan under press
I mänskliga ögon kartlade teamet hur infektionen interagerade med de lokala stödjeceller som normalt skyddar neuroner. Stjärnformade astrocyter och Müllerceller, liksom mikroglia — hjärnans och näthinnans egna ”städceller” — samlades runt infekterade områden. Kemiska signaturer för NLRP3‑inflammasomet och dess nedströms dödsvägar var starkt förhöjda i näthinnor från personer med Alzheimers och höjdes redan hos dem med mild kognitiv störning. Många infekterade celler bar markörer för både hetsiga ”pyroptotiska” dödsprocesser och mer välkänd apoptos. Även om fler mikroglia rekryterades i Alzheimersnäthinnor verkade varje bakterie vara i kontakt med eller uppslukad av färre mikroglia än i friska ögon, vilket tyder på att städsystemet blir överbelastat eller nedsatt när sjukdomen framskrider.
Använda ögat för att avläsa hjärnhälsa
Eftersom näthinnan är tillgänglig för högupplöst avbildning hos levande personer undersökte forskarna om näthinnemått relaterade till Chlamydia pneumoniae kunde hjälpa att förutsäga Alzheimersstatus. De använde maskininlärningsmodeller för att kombinera retinala infektionsnivåer med markörer såsom amyloid‑beta‑avlagringar, inflammation och lokalt vävnadstunnande. Vissa kombinationer — särskilt retinala bakterier tillsammans med amyloid — särskilde Alzheimerspatienter från kontrollpersoner med hög noggrannhet och korrelerade med sjukdomsstadium och kognitiva testpoäng. Även om mer arbete och större studier behövs tyder resultaten på att ett enkelt ögonbaserat test en dag skulle kunna avslöja inte bara klassiska Alzheimersförändringar utan också en dold infektiös komponent, vilket öppnar för tidigare användning av antibiotika eller läkemedel som dämpar inflammasomet hos personer i riskzonen.
Vad detta kan innebära för patienter
För icke‑specialister är huvudbudskapet att Alzheimers kanske inte enbart drivs av felaktigt beteende hos proteiner; långvariga infektioner kan fungera som bränsle som hälls på en långsam brand. Denna studie ger starka bevis för att en vanlig luftvägsbakterie kan slå sig ner i näthinnan och hjärnan, väcka skadlig inflammation och förvärra minnesförlust hos mottagliga individer. Om framtida kliniska prövningar bekräftar att behandling av sådana infektioner eller blockering av inflammasomvägen bromsar försämringen, skulle rutinmässig näthinneavbildning och riktade terapier kunna bli en del av en mer proaktiv, individualiserad strategi för att förebygga eller skjuta upp demens.
Citering: Gaire, B.P., Koronyo, Y., Vit, JP. et al. Identification of Chlamydia pneumoniae and NLRP3 inflammasome activation in Alzheimer’s disease retina. Nat Commun 17, 771 (2026). https://doi.org/10.1038/s41467-026-68580-4
Nyckelord: Alzheimers sjukdom, näthinna, Chlamydia pneumoniae, neuroinflammation, amyloid‑beta