Clear Sky Science · sv
HIF upprätthåller en transkriptionell regleringskrets för EPAS1-uttryck vid klarcelligt njurcancer
Varför njurcancer kräver närmare granskning
Klarcellig njurcellscancer är den vanligaste formen av njurcancer, och många patienter behandlas i dag med läkemedel som blockerar ett protein kallat HIF‑2α. Dessa läkemedel kan krympa tumörer, men de fungerar inte lika bra för alla. Denna studie ställer en enkel men viktig fråga: vad gör att vissa njurtumörer producerar så mycket HIF‑2α, och kan förståelsen av denna "på-slå-knapp" hjälpa oss att förutsäga vilka som får mest nytta av behandlingen och hur nya terapier kan utformas?
Syresensorn som går ur sitt esse
Friska njurceller använder ett säkerhetsprotein kallat VHL för att hålla syresensorer, kända som HIF:er, under noggrann kontroll. När syre finns i överflöd markerar VHL HIF-proteiner för nedbrytning och förhindrar att de aktiverar gener som främjar blodkärlsbildning och celldelning. Vid klarcellig njurcancer förloras eller skadas VHL vanligen. Som en följd undkommer en medlem i HIF-familjen, HIF‑2α (kodad av genen EPAS1), nedbrytning och ansamlas. Tidigare arbeten visade att hög HIF‑2α-aktivitet kopplas till snabbare tumörtillväxt och sämre prognos, och att blockad av HIF‑2α kan bromsa eller stoppa tumörer hos vissa patienter. De molekylära stegen som ökar EPAS1-genens aktivitet i njurtumörer var dock inte väl förstådda.
En dold DNA-strömbrytare för en cancergen
Genom att använda tumörprover från patienter, enkelcellsdata och cancercellmodeller visar författarna att HIF‑2α-messenger-RNA är avsevärt högre i klarcellig njurtumör än i normalt njurvävnad eller andra njurtumörtyper. De skannar sedan EPAS1-regionen i genomet efter kemiska och strukturella markörer som signalerar aktiv reglerande DNA. Detta avslöjar en kraftfull enhancer — en sorts långdistans genströmbrytare — belägen cirka 70 000 DNA-bokstäver uppströms om EPAS1 som är specifikt aktiv i klarcellig tumörer. I tumörceller är kromatinet vid denna enhancer öppet, dekorerat med aktiveringsmarkörer och fysiskt loopar det för att kontakta EPAS1-promotorn, medan denna region i normala njurtubuliceller är till största delen tyst. Aktivitet vid denna enhancer korrelerar med högre EPAS1-nivåer i stora cancer-dataset. 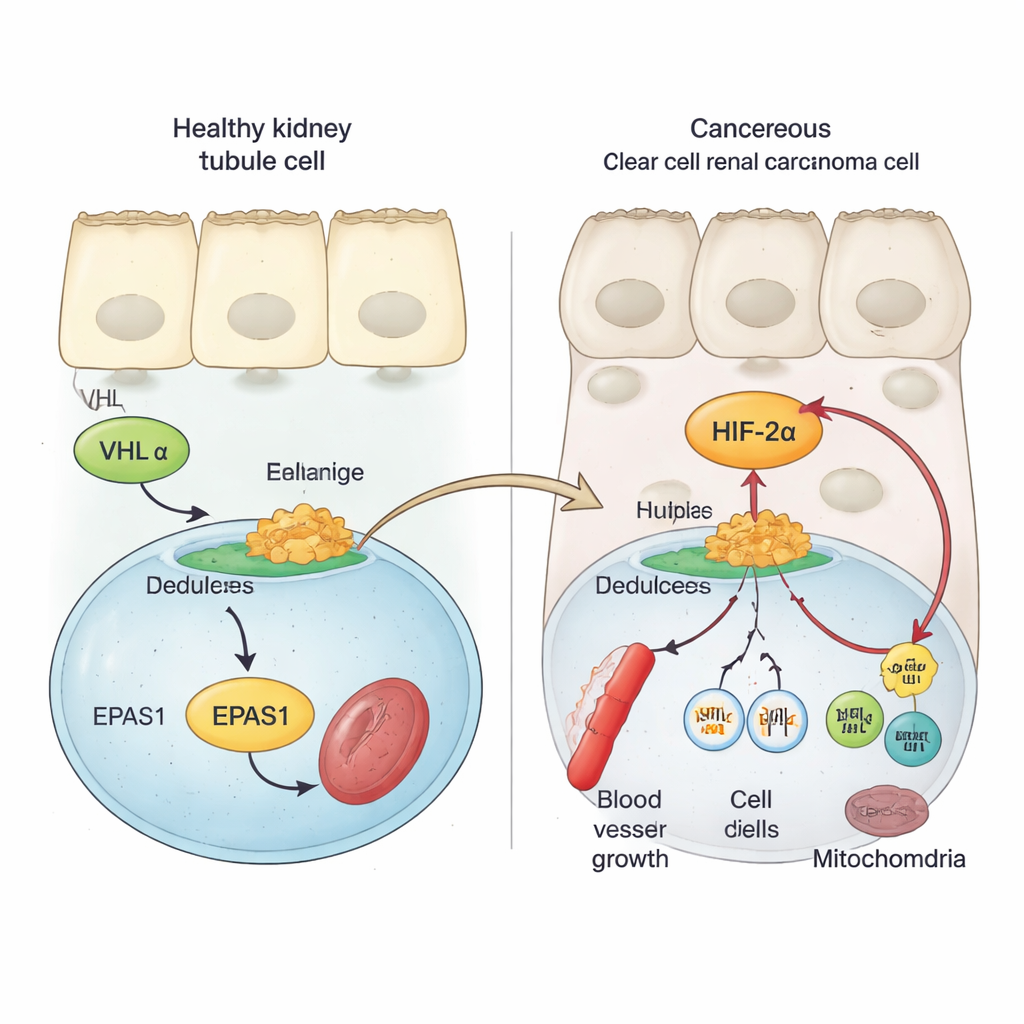
En självförstärkande slinga driven av njuridentitetsfaktorer
Studien visar att HIF-proteiner gör mer än att bara svara på låg syrehalt — de hjälper faktiskt till att driva sin egen produktion. När forskarna återställer VHL eller tar bort en viktig HIF-partner (HIF‑1β) sjunker EPAS1-nivåerna och enhancern blir mindre åtkomlig. Direkt kartläggning av protein–DNA-kontakter visar att HIF binder till två enhancerregioner uppströms om EPAS1, inklusive den klarcellsspecifika enhancern. I njurtumörceller är denna enhancer även ockuperad av PAX8 och HNF‑1β, transkriptionsfaktorer som bidrar till njurcellens identitet och som är kända för att stödja tumörtillväxt. Att störa PAX8 eller HNF‑1β, eller mutera deras bindningsställen inom enhancern, minskar HIF‑2α-RNA och protein samt försvagar enhanceraktiviteten. Tillsammans avslöjar dessa fynd en auto-reglerande krets: HIF‑2α, i samverkan med njurursprungsfaktorer, ökar aktiviteten i en EPAS1-enhancer, vilket i sin tur driver fram mer HIF‑2α-produktion.
Genetisk risk och tumörbeteende möts i samma krets
EPAS1-regionen har länge pekats ut i genome-wide studier som en het punkt för risk för njurcancer, med vissa ärftliga varianter kopplade till högre cancerrisk och till VHL-mutationer i tumörer. Genom att kombinera genetiska data med genuttrycksmätningar visar författarna att individer som bär den högriskvariant av en nyckelvariant i EPAS1 tenderar att ha högre HIF‑2α-nivåer i sina tumörer — och till och med i normala njurtubuliceller när HIF experimentellt stabiliseras. Detta tyder på att ärftliga DNA‑skillnader kan ställa in hur kraftigt enhancern svarar, och på så vis förbereda vissa njurar att öka HIF‑2α mer när VHL går förlorad. Experiment i glioblastomceller visar att samma enhancer också kan aktiveras i vissa hjärntumörer, vilket antyder att denna regleringsmodul kan återanvändas i andra cancerformer där HIF‑2α är viktig. 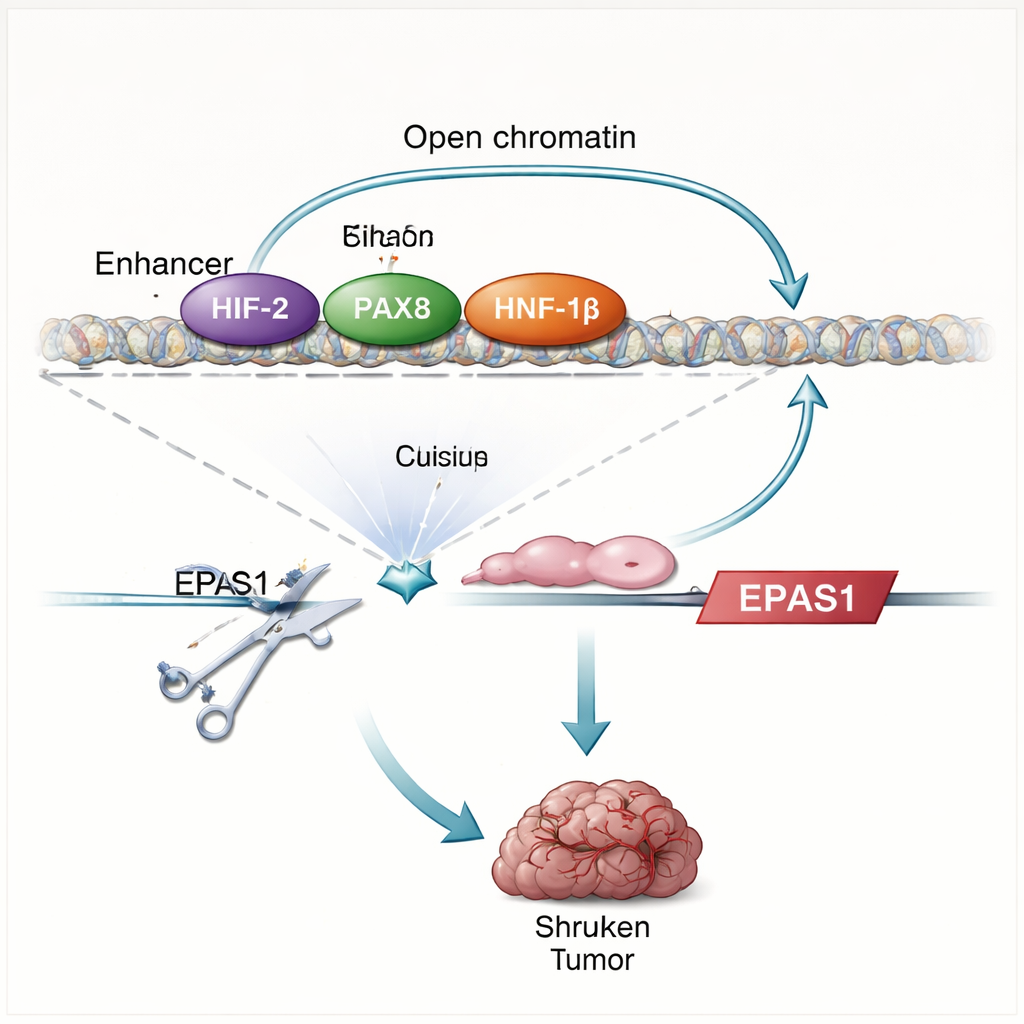
Att bryta slingan för att stoppa tumörtillväxt
För att testa hur avgörande denna enhancer är använder teamet CRISPR-genomredigering för att skada HIF-bindningsmotiven inom den i njurcancercellinjer och färska patienttumörceller. Detta nedskär HIF‑2α-RNA med ungefär en tredjedel till hälften, sänker nivåerna av välkända HIF‑2α-målgener som CCND1 och VEGFA, och försvagar det bredare hypoxi-genprogrammet. När redigerade celler implanteras i möss bildar de i stort sett inga tumörer, i skarp kontrast till kontrollceller. Mönstret av genförändringar efter enhancerstörning speglar nära effekterna av att direkt blockera HIF‑2α med ett kliniskt läkemedel, vilket understryker att detta enda DNA-element är en huvuddrivkraft i HIF‑2α-vägen i dessa cancerformer.
Vad detta betyder för patienter och behandlingar
För icke-specialister är huvudbudskapet att författarna har identifierat en självförstärkande DNA-strömbrytare som håller ett centralt cancerfrämjande protein, HIF‑2α, aktivt i klarcellig njurtumör. Denna strömbrytare beror både på förlusten av VHL-säkerhetsbromsen och på njurspecifika hjälpproteiner, och påverkas av ärftliga genetiska varianter. Eftersom enhancern är starkt aktiv i många klarcelligtumörer och är tätt kopplad till hur intensivt HIF‑2α‑vägen drivs, skulle mätning av dess aktivitet — eller direkt targeting av den — kunna hjälpa till att identifiera patienter som får mest nytta av nuvarande HIF‑2α‑hämmare och erbjuda nya sätt att slå ner denna väg när tumörer blir läkemedelsresistenta.
Citering: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Nyckelord: klarcellig njurcancer, HIF-2α, EPAS1-enhancer, VHL-mutation, njurcancergenetik