Clear Sky Science · sv
Atroposelektiv avbruten CuAAC-reaktion med cykliska diaryliodonier
Varför denna nya kemi är viktig
Kemister har länge förlitat sig på en enkel ”click”-reaktion för att snabbt och rent koppla samman molekylära byggstenar — ett knep som stöder allt från läkemedelsforskning till självhelande material. Den här artikeln beskriver en smart variant av den klassiska click-reaktionen som gör det möjligt för forskare att bygga mer komplexa, tredimensionella molekyler med precis handighet — strukturer som värderas högt inom moderna läkemedel och avancerade material.
Ge en klassisk click-reaktion ett nytt uppdrag
Utgångspunkten är kopparkatalyserad azid–alkyn-cykloaddition, ofta kallad CuAAC. Den förenar två små komponenter — en azid och en alkyn — till en femledad ring kallad triazol under milda förhållanden och med anmärkningsvärd tillförlitlighet. Traditionellt upphör reaktionen när kopparen hjälper till att bilda triazolringen. Under de senaste åren har kemister emellertid lärt sig att ”avbryta” denna process, genom att fånga ett flyktigt koppar–triazol-intermediat med en tredje partner för att bygga mer utsirade produkter. Hittills har dessa avbrott inte kunnat styra molekylär handighet (kiralitet) på ett generellt sätt, vilket begränsat deras användbarhet för att göra sofistikerade, kirala molekyler.
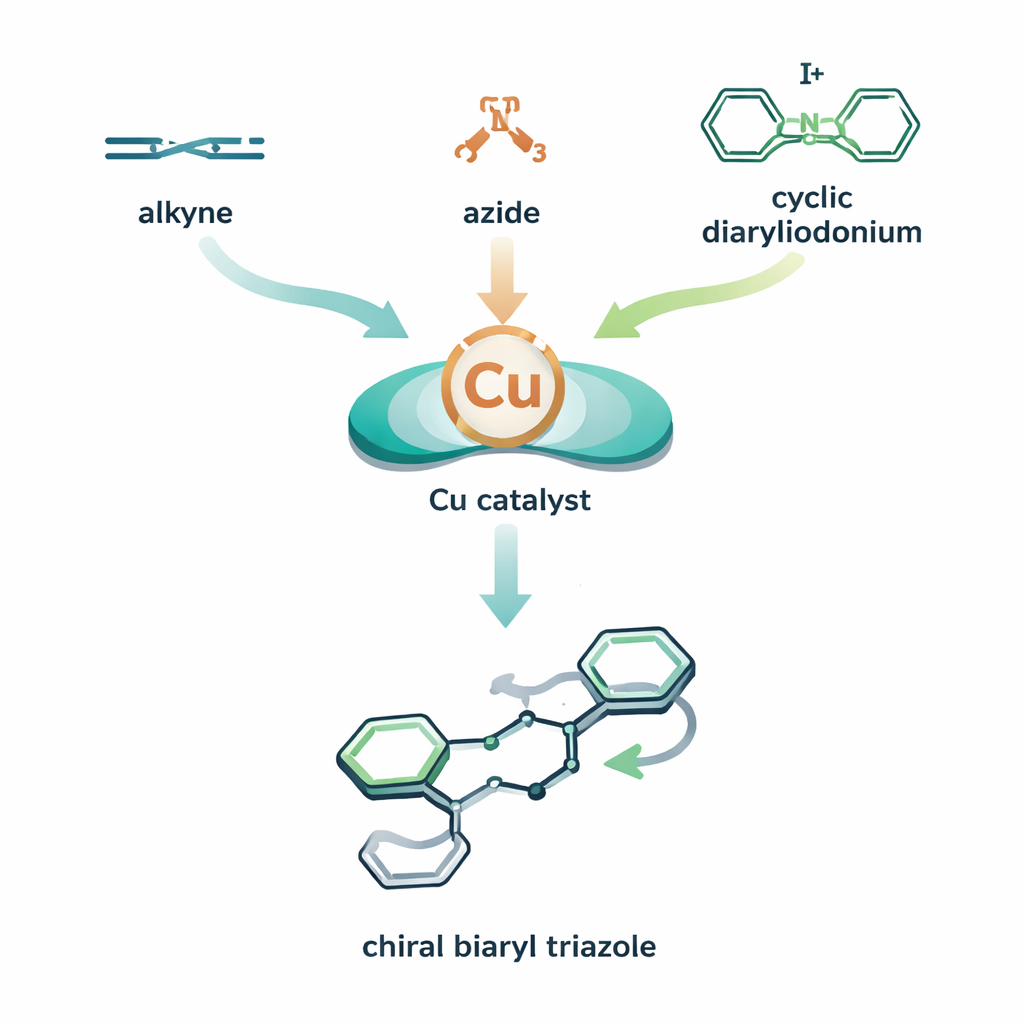
Pussel i tre delar med en vridning
Författarna kombinerar två kopparbaserade reaktionscykler till en enhetlig, orkestrerad process. I deras upplägg hjälper en kopparkatalysator först alkynen och aziden att bilda ett koppar–triazol-intermediat. Innan detta intermediat neutraliseras tillsätts en tredje komponent — en ringformad, mycket reaktiv jodinnehållande molekyl kallad cyklisk diaryliodonium. Koppar införs i denna ring och öppnar den, och fäster en av sina aromatiska ringar vid triazolen. Resultatet är en biaryltriazol: två ringsystem förenade runt en bindning som kan fungera som en kiral axel, ungefär som en propeller som kan vrida åt vänster eller höger. Genom att para kopparn med en noga utvald kiral ligand styr teamet processen så att en vridning bildas mycket mer än den andra, vilket uppnår hög atroposelektivitet (kontroll över vilken axial ”hand” som bildas).
Testa metodens flexibilitet och pålitlighet
För att förstå hur generell reaktionen kan vara varierade forskarna systematiskt varje av de tre byggstenarna. De visade att många olika alkyns, inklusive sådana med elektronrika, elektronfattiga och heteroaromatiska ringar, kan delta och ändå ge goda utbyten och stark preferens för en kiral form. Vissa skrymmande substitutioner förbättrade selektiviteten men kunde minska utbytet, vilket visar en avvägning mellan steriskt hinder och effektivitet. Azidpartnerna fungerade bäst när de härstammade från enkla ester- eller amidgrupper eller från benzyla positioner, och en rad sådana azider gav högt berikade kirala produkter. Den cykliska diaryliodonium-komponenten kunde också justeras: vissa substitutioner bevarade både utbyte och selektivitet, medan andra, särskilt nära den reaktiva jodcentret, fördröjde reaktionen eller försämrade dess prestanda. Sammantaget levererade studien en bred samling nya atropoisomera biaryltriazoler åtkomliga i ett enkelt steg.
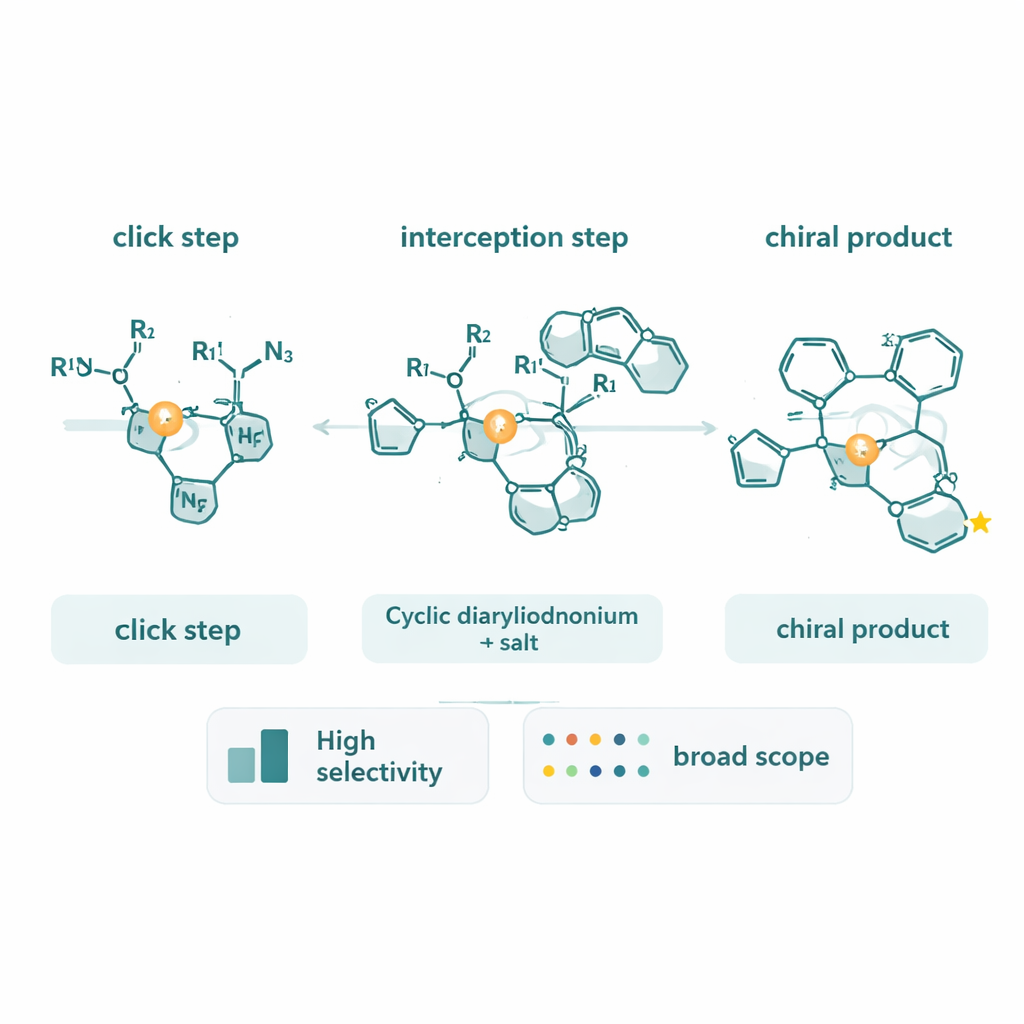
En titt under huven på reaktionen
Utöver att skapa nya molekyler lade teamet ner betydande ansträngning på att ta reda på hur reaktionen faktiskt fungerar. Med hjälp av deuteriummärka alkyns observerade de en ovanlig invers kinetisk isotopeffekt, vilket pekar på ett hastighetsbestämmande steg där alkynkolt ändrar sin bindningskaraktär snarare än att enbart bryta en C–H-bindning. Kalorimetri-baserad analys av reaktionsförlopp visade att reaktionshastigheten är starkt beroende av koncentrationerna av alkyn och azid, men endast svagt beroende av den cykliska diaryliodoniumen. Dessa mätningar stöder en bild där bildning och omvandling av koppar–triazolkomplexet, och dess oxidativa addition in i diaryliodoniumringen, tillsammans bestämmer reaktionens tempo. De fann också att de kirala triazolprodukterna själva kan fästa vid koppar och sakta ner katalysatorn, vilket antyder sätt att ytterligare optimera systemet.
Vad detta innebär framöver
I vardagliga termer har forskarna lärt en välkänd click-reaktion ett nytt trick: istället för att bara snappa ihop två delar hjälper den nu till att montera tre komponenter till komplexa, propellerliknande molekyler samtidigt som den nästan uteslutande väljer en föredragen vridning. Detta ger en skalbar väg till kirala biaryltriazoler, strukturer som är värdefulla som potentiella läkemedel, katalysatorer och funktionella material. De mekanistiska insikterna — särskilt hur det nyckelintermediatet fångas och hur produkten kan förgifta katalysatorn — erbjuder en färdplan för att konstruera ännu mer effektiva och selektiva versioner av denna kemi. För icke-specialister är huvudpoängen att ett redan kraftfullt molekylärt ”Lego”-verktyg precis blivit mer mångsidigt, vilket möjliggör att kemister kan bygga mer intrikata och användbara former med fin kontroll över deras tredimensionella utformning.
Citering: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Nyckelord: click-kemi, kopparkatalys, kiral biaryl, atropisomer, triazol