Clear Sky Science · sv
Bryta cellväggen för effektiv DNA‑leverans till kiselalger
Alger som små gröna fabriker
Kiselalger — mikroskopiska alger som driver i havet — producerar tyst omkring en femtedel av planetens organiska kol och hjälper till att föda marina näringskedjor och binda koldioxid. Forskare vill omvandla dessa tåliga, snabbst växande organismer till små gröna fabriker för att tillverka bränslen, livsmedel och specialkemikalier. Men en stor bromskloss har funnits: det är förvånansvärt svårt att få in nytt DNA i kiselalgsceller på ett tillförlitligt sätt. Denna studie tar itu med det praktiska problemet direkt och beskriver nya sätt att smuggla genetiska instruktioner och verktyg för genredigering förbi kiselalgens tuffa yttre skal.
Mjukning av havsmikrobens skal
Arbetet kretsar kring modellkiselalgen Phaeodactylum tricornutum, en favorit i laboratorier eftersom dess genom är väl kartlagt och det redan finns grundläggande genetiska verktyg. Författarna antog att cellväggen, den första fysiska barriären som allt DNA måste korsa, utgjorde en viktig flaskhals. Genom att behandla cellerna med ett enzym kallat alcalase avlägsnades denna vägg delvis eller helt, vilket skapade sköra ”sferoplaster” och ”protoplaster” som är mycket lättare att tränga igenom. När de sedan använde elektroporering — korta elektriska pulser som öppnar tillfälliga porer — ökade antalet lyckade transformanter dramatiskt, med ungefär två storleksordningar jämfört med tidigare metoder. Även mycket små mängder DNA, så lite som en nanogram, räckte för att återfå konstruerade celler. 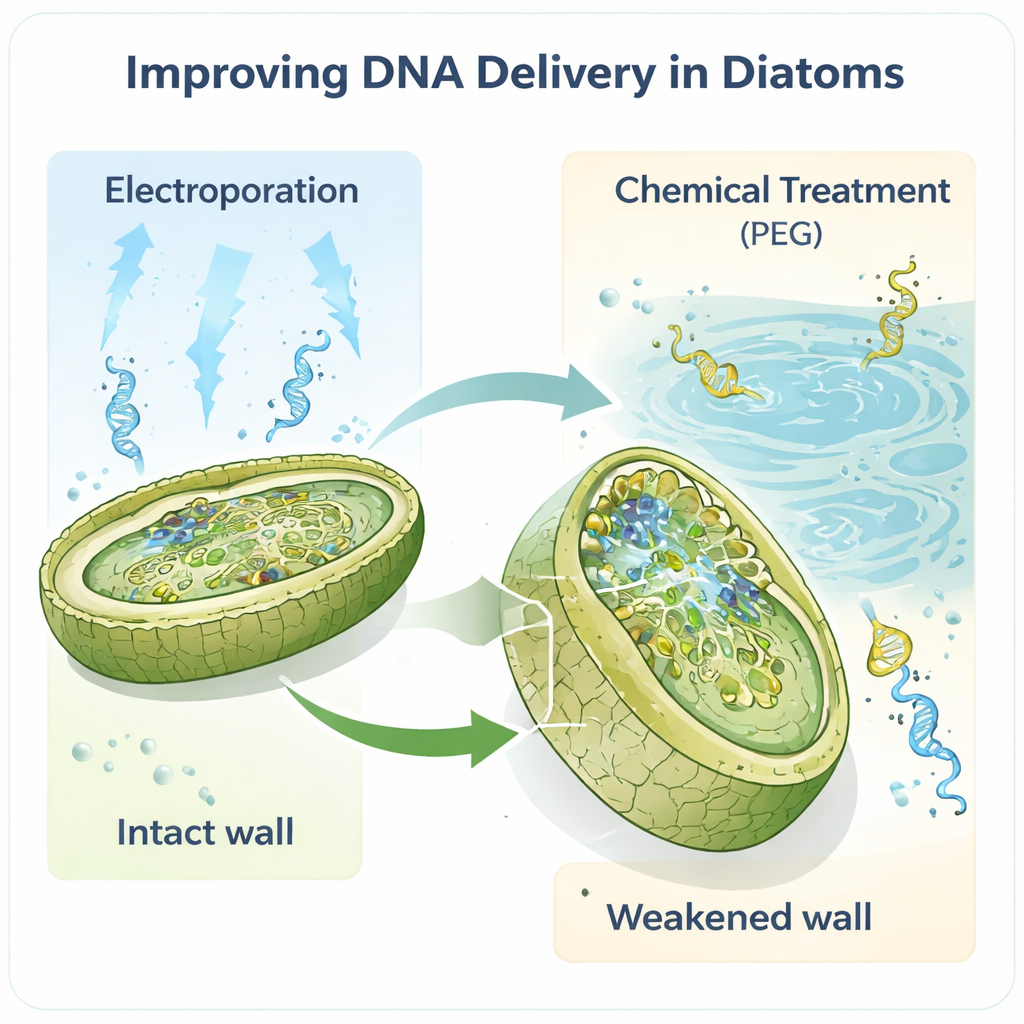
Snabb DNA‑leverans utan kringflytt via bakterier
Traditionella sätt att modifiera kiselalger förlitar sig ofta på bakterie‑”kurirer” som för stora cirkulära DNAmolekyler, så kallade episomer, in i algerna. Även om det fungerar är den metoden långsam, tekniskt krävande och kan göra känsliga DNA‑konstruktioner instabila. De nya protokollen visar att både elektroporering och en förfinad kemisk metod med polyetylenglykol (PEG) kan föra episomer direkt in i kiselalger, utan bakteriesteg. Anmärkningsvärt nog levererades och kunde återhämtas episomer upp till 55,6 tusen baspar långa i intakt form. Samma strategier fungerade också i en andra art, Thalassiosira pseudonana, som har en mer kraftigt mineraliserad vägg, vilket tyder på att detta är en allmänt användbar verktygslåda snarare än ett art‑specifikt knep.
Låta cellen bygga sina egna genetiska cirklar
När teamet undersökte hur det elektroporerade DNA:t betedde sig inuti cellerna snubblade de över en överraskande förmåga: kiselalger kan själv sammanfoga DNA‑fragment. Linjära delar av episomer gick in i cellen och reparerades till cirklar antingen genom oprecis ”icke‑homolog” sammanfogning eller genom mer noggrann, överlappningsstyrd ”homologi‑dirigerad” reparation. Författarna kallade denna process ”diatom in vivo assembly”, eller DIVA. Genom att designa överlappande fragment lockade de cellerna att sätta ihop två, tre eller fyra bitar till fullständiga episomer med höga framgångsfrekvenser, ibland även genom att infoga små syntetiska kassett‑bitar som lägger till fluorescerande taggar eller nya funktioner. Denna förmåga förvandlar kiselalgsnukleus till en miniatyr verkstad för DNA, vilket potentiellt kan ersätta arbetsintensiva monteringssteg som normalt görs i jäst eller E. coli.
Redigera genom med endast proteinkomplex
Utöver att lägga till episomer visade forskarna att de kunde leverera färdiga CRISPR–Cas9 protein‑RNA‑komplex direkt in i kiselalgsceller med hjälp av sin optimerade elektroporationsmetod. Genom att rikta in sig på en gen kallad PtAPT, som styr känslighet för en giftig adenininliknande förening, frambringade de tusentals resistenta mutantkolonier utan att införa något extra DNA i genomet. Många av dessa mutanter bar små insättningar eller deletioner vid målplatsen; några få fångade till och med bitar av ”bärar‑DNA” som hade tillsatts för att buffra det elektriska stöten. Teamet samtidiglevererade sedan CRISPR‑komplex och episomer i ett steg och fann att ungefär en av tio kolonier bar både en genomisk edit och en selekterbar episom — ett effektivt sätt att följa annars osynliga genförändringar. 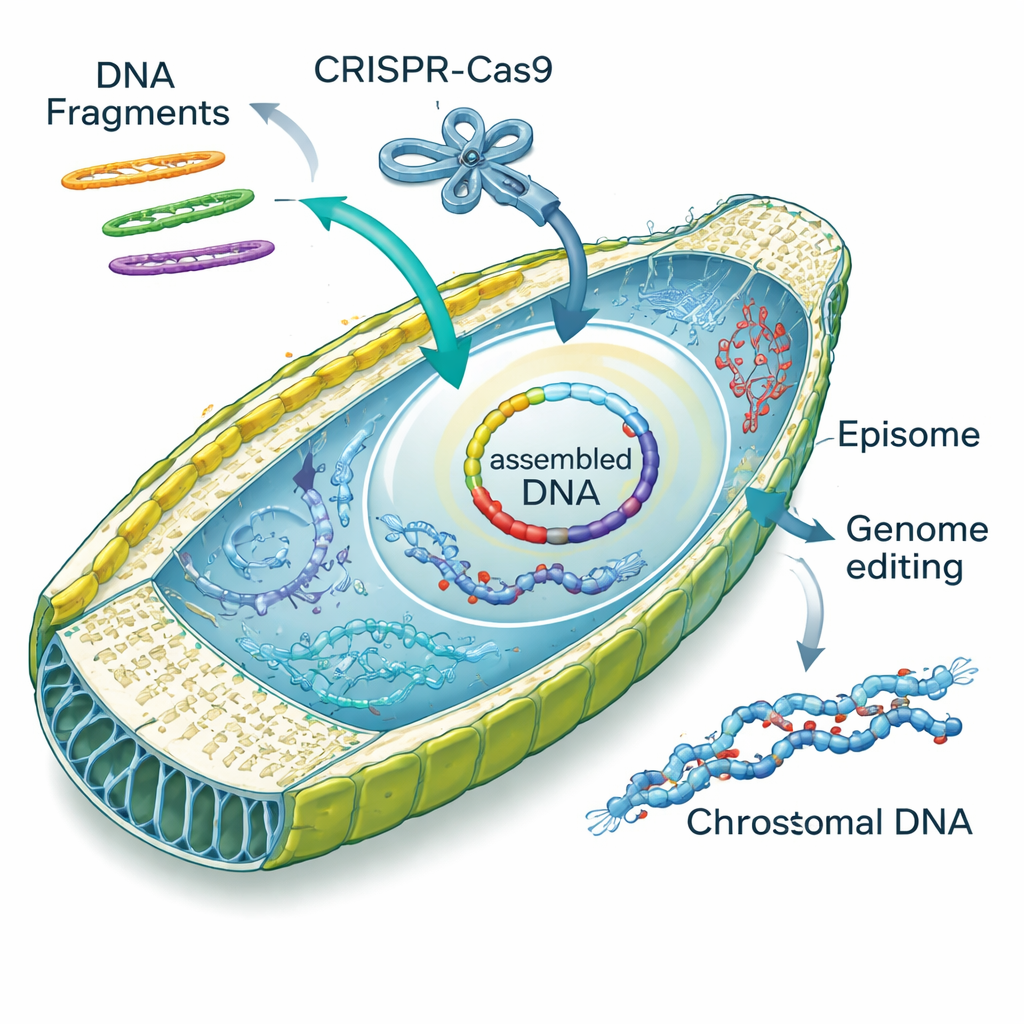
Mot designade kiselalger för en hållbar framtid
För icke‑specialister är huvudbudskapet att kiselalger nu ligger mycket närmare att bli praktiska, programmerbara organismer. Genom att varsamt bryta eller mjuka upp cellväggen förvandlade författarna en kinkig, lågavkastande process till en robust arbetsgång som använder små mängder DNA, fungerar med stora genetiska konstruktioner och till och med låter cellen montera och redigera sitt eget DNA. Dessa framsteg förkortar vägen från en dator‑designad sekvens till en levande, testad stam. I längden kan sådana verktyg snabba arbetet med att bygga kiselalger med helt syntetiska kromosomer och utnyttja dessa havs‑mikrober för renare bränslen, klimatvänlig kemi och nya biologiska upptäckter.
Citering: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
Nyckelord: kiselalgsbioteknik, genetisk omvandling, CRISPR genredigering, syntetisk biologi, mikroalgsingenjörskonst