Clear Sky Science · sv
Strukturer av nukleotidbundet mänskligt telomeras vid flera steg i dess cykel för tillsats av telomeriskt DNA
Varför ändarna på våra kromosomer spelar roll
Varje gång en cell delar sig blir de skyddande mössorna på kromosomändarna — kallade telomerer — en aning kortare. Om de blir för korta upphör cellerna att dela sig eller fungerar dåligt, vilket bidrar till åldrande och sjukdom. En molekylär maskin som kallas telomeras kan återskapa dessa mössor och är ovanligt aktiv i de flesta cancerformer. Denna studie visar, med en enastående detaljnivå, hur mänskligt telomeras greppar och förlänger telomererna steg för steg, vilket ger ledtrådar till hur vi en dag skulle kunna finjustera detta enzym vid åldersrelaterade sjukdomar och cancer.
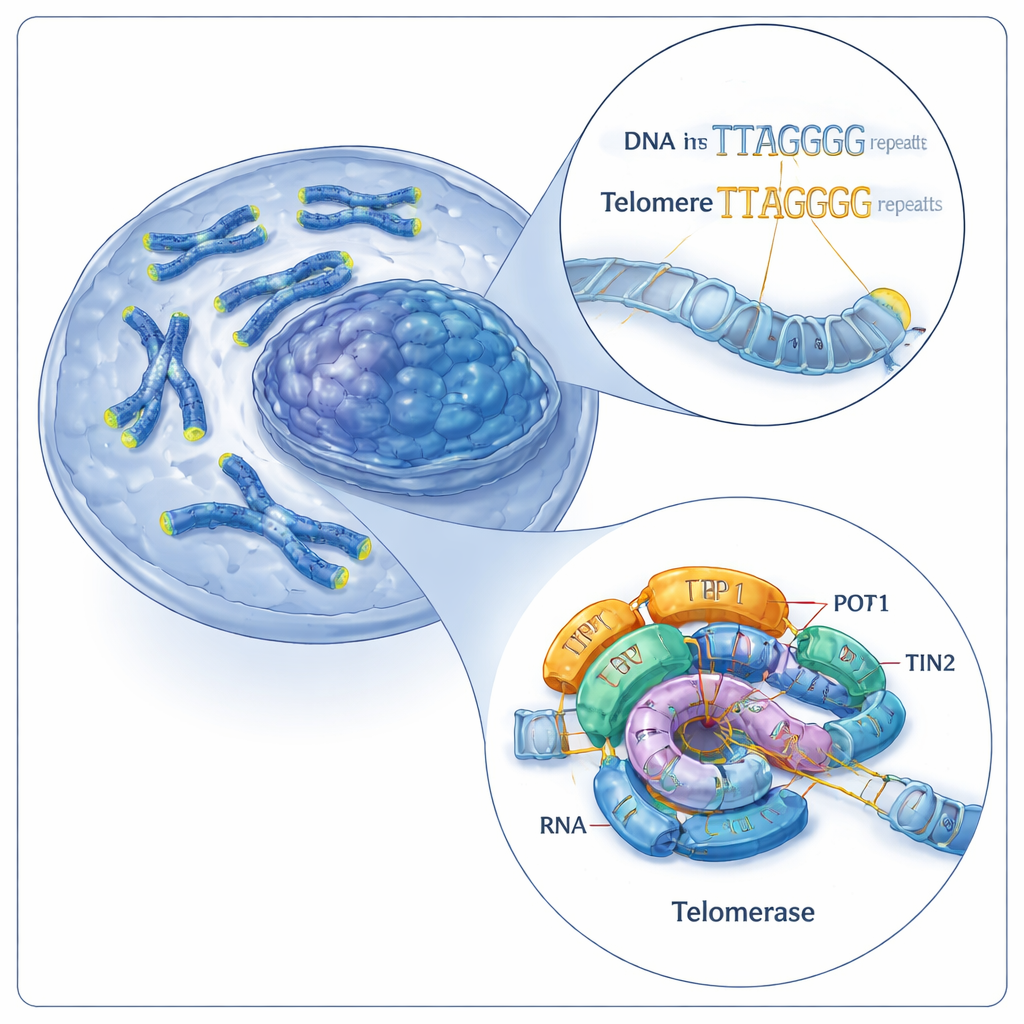
Cellens reparationsbesättning för kromosomändar
Telomerer består av korta, upprepade DNA‑sekvenser (hos människor ett sexbokstavsmönster: TTAGGG). Telomeras förlänger telomererna genom att lägga till fler av dessa repetitioner på kromosomändarna. Det gör detta med två huvuddelar: ett protein kallat telomeras revers transkriptas (TERT) och en inbyggd RNA‑molekyl (hTR) som fungerar som mall. Tillsammans bildar dessa komponenter en katalytisk kärna som vidare stöds av hjälpproteiner kända som shelterin, inklusive en trio kallad TPP1–POT1–TIN2. Tidigare arbete hade visualiserat mänskligt telomeras i endast ett arbetsläge, vilket lämnade en viktig fråga öppen: hur kan denna maskin upprepade gånger lägga till nya repetitioner utan att släppa taget om DNA:t?
Frysa telomeras i arbete
Forskarna återuppbyggde mänskligt telomeras i humana celler och monterade det därefter med noggrant utformade bitar av telomeriskt DNA och icke‑reaktiva nukleotidanaloger — molekyler som liknar DNA‑bokstäver men inte kan införlivas fullt ut. Med hjälp av högupplöst kryo‑elektronmikroskopi fångade de ögonblicksbilder av telomeras i tre nyckelstadier av dess cykel för tillsats av repetitioner: starten (initiering), mitten av kopieringen (elongation) och precis innan en repetition avslutas (pre‑terminering). Varje ögonblicksbild visade den katalytiska kärnan av telomeras omsluta ett kort hybridpar av DNA och RNA, med en inkommande nukleotid i beredskap i det aktiva sätet, redo att adderas till den växande DNA‑strängen.
En liten dragkedja som styr en stor process
I samtliga tre stadier framträdde ett överraskande tema: DNA–RNA‑hybriden inne i telomeras förblir i huvudsak samma längd — endast fyra baspar lång, tillfälligt utsträckt till fem när en ny nukleotid kommer in. En specifik aminosyra i TERT, kallad en ”dragkedjehuvud”, markerar konsekvent slutet på denna korta hybrid och förhindrar att den växer längre. När nya DNA‑bokstäver läggs till smälter ett baspar i den fjärra änden bort, så hybridens längd aldrig överstiger detta snäva fönster på fyra till fem par. Denna kompakta design underlättar sannolikt att strängarna separeras och förskjuts, vilket tillåter enzymet att förflytta sig och påbörja nästa repetition utan att fullständigt släppa DNA:t. Subtila skillnader i vilka DNA‑ och RNA‑bokstäver som upptar denna korta hybrid förklarar varför vissa telomeriska ändsekvenser binder starkare till telomeras än andra.
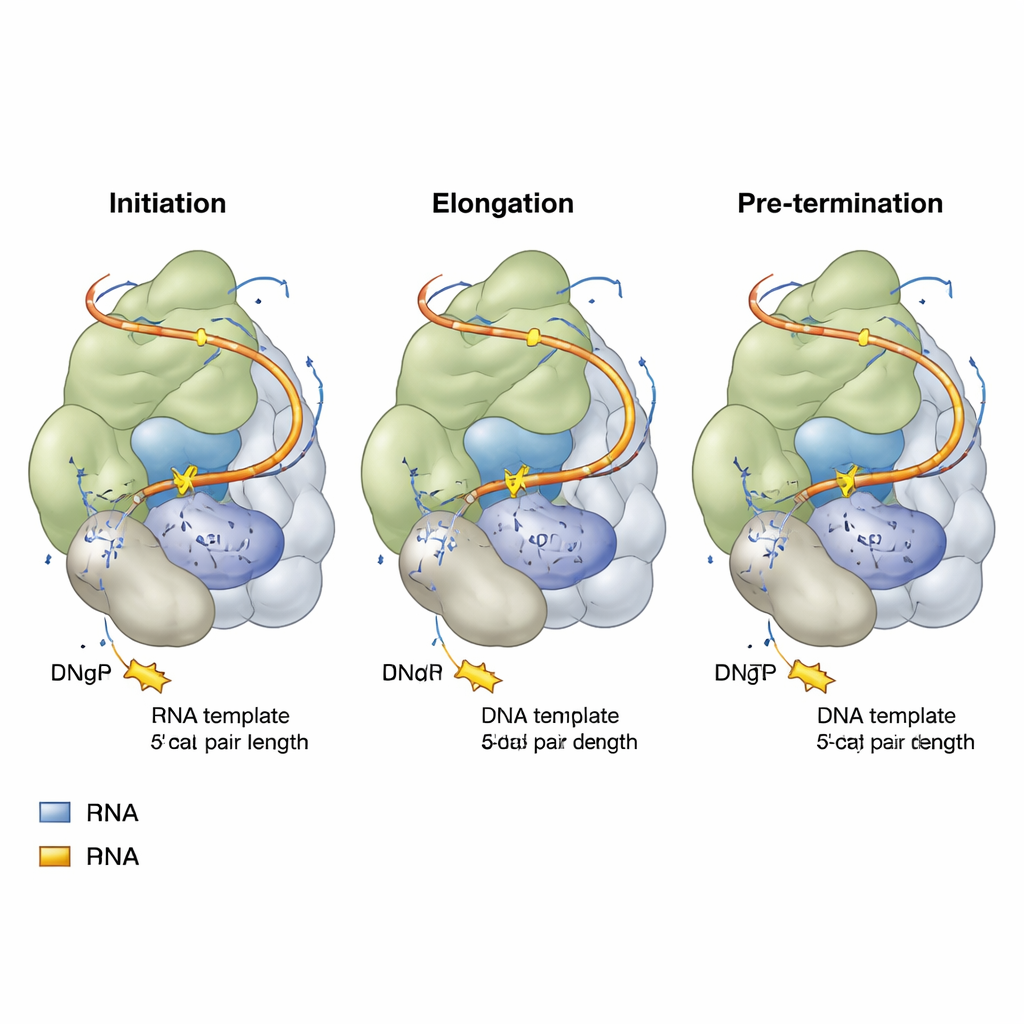
Flexibla RNA‑länkar och rörliga delar
RNA‑mallen inom telomeras flyter inte fritt; den är förankrad av flexibla sträckor på båda sidor, kallade 5′‑ och 3′‑templatlänkar. När telomeras går från initiering till pre‑terminering dras den uppströms (5′) länken ut som ett gummiband och når så småningom ett fullt utsträckt tillstånd som hjälper till att signalera slutet av en repetition. Samtidigt buktar den nedströms (3′) länken utåt och närmar sig en annan RNA‑struktur (P6.1‑stam‑loop) och närliggande proteinregioner. Om dessa länkar blir för korta eller för långa, eller om P6.1 förändras, minskar telomeras förmåga att lägga till repetition efter repetition kraftigt. Viktigt är att vissa proteinregioner — TEN‑domänen och ett telomeras‑specifikt inskott kallat TRAP‑kil — fungerar som justerbara guider som kontaktar både DNA och dessa RNA‑länkar. Mutationer som minskar volymen av TRAP‑kilen kan faktiskt göra enzymet mer processivt, vilket tyder på att denna kil normalt fungerar som en kontrollerad barriär som tajmar mallens förflyttning.
Nya insikter i ett terapeutiskt mål
Genom att kombinera strukturella ögonblicksbilder med funktionella tester av riktade mutationer föreslår studien en detaljerad mekanisk modell för hur mänskligt telomeras upprepade gånger förlänger telomerer. Enzymet håller en mycket kort DNA–RNA‑hybrid, använder en dragkedje‑liknande rest för att upprätthålla den längden och förlitar sig på flexibla RNA‑länkar och rörliga proteinlement för att avancera mallen och hålla DNA:t förankrat under flera kopieringsomgångar. För icke‑specialister är huvudbudskapet att telomeras inte fungerar som en statisk kopieringsmaskin utan som en finjusterad, fjäderladdad enhet vars geometri och rörliga delar bestämmer hur länge och hur effektivt den kan upprätthålla telomererna. Att förstå denna koreografi öppnar dörren för läkemedel som antingen kan dämpa telomeras i cancer eller stabilisera dess funktion i sjukdomar med förtida åldrande.
Citering: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Nyckelord: telomeras, telomerer, kryo‑EM, genomstabilitet, cancerbiologi