Clear Sky Science · sv
DNA-metylering och lncRNA styr asynkron DNA-replikation i specifika imprintade genområden
Varför cellens DNA-kopieringsschema spelar roll
Varje gång en cell delar sig måste den kopiera sitt hela DNA, men inte alla regioner dupliceras vid samma tidpunkt. Vissa sträckor kopieras tidigt, andra sent, enligt ett precist genomiskt "tidschema". Denna artikel undersöker varför, i ett fåtal speciella genkluster som minns vilken förälder de kommer från, moderns och faderns kopior kopieras vid olika tidpunkter. Att förstå denna ovanliga timing ger insikt i hur kemiska märkningar på DNA och långa icke-kodande RNA (lncRNA) hjälper till att organisera genomet och kan påverka utveckling och sjukdom.
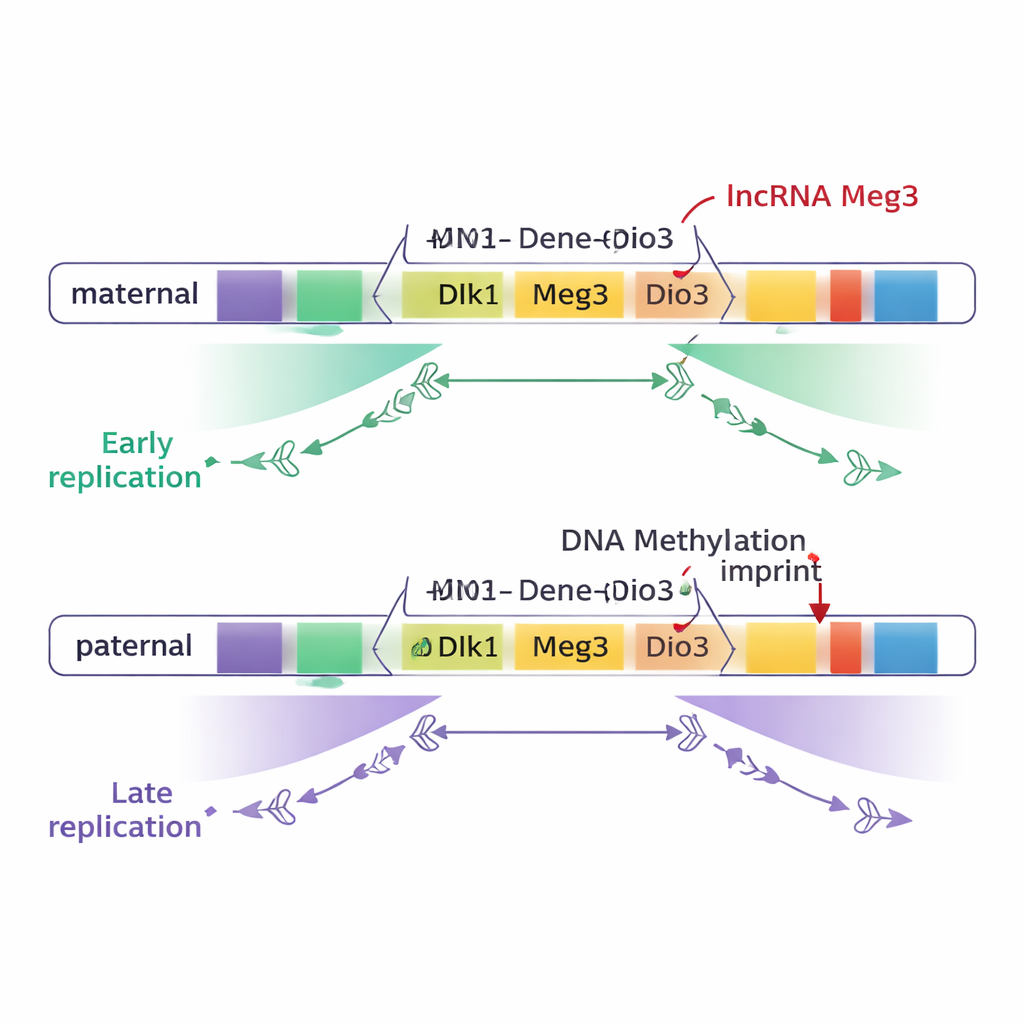
Föräldrarnas minnen skrivna på DNA
I däggdjur beter sig ett litet antal "imprintade" gendomäner olika beroende på om de ärvts från modern eller fadern. Denna föräldraursprungetffekt styrs av DNA-metylering—små kemiska märken som läggs till specifika regioner kända som differentialt metylerade regioner (DMR)—och av förändringar i kromosomvikning. Författarna studerade musens embryonala stamceller, som liknar mycket tidiga embryonala celler. De jämförde celler med endast maternella genom, endast paternella genom och normala hybrider med ett av varje. Genom att spåra när delar av DNA kopierades under cellcykeln kartlade de replikationstiming över genomet och zoomade in på kända imprintade regioner.
Två imprintade regioner bryter mot reglerna
Största delen av genomet, inklusive de flesta imprintade domäner, visade sig kopieras samtidigt på maternella och paternella kromosomer. Dock stack två stora imprintade regioner ut: Dlk1–Dio3-domänen på kromosom 12 och Snrpn-regionen på kromosom 7. I dessa områden kopierades en vidsträckt DNA-sträcka—ungefär tre fjärdedels miljon baspar i Dlk1–Dio3—tidigt på ena föräldrakromosomen och sent på den andra. Viktigt är att denna skillnad följde föräldraursprung, inte stam: den maternella kopian av nyckelgener som Dlk1 och lncRNA-genen Meg3 replikerade konsekvent tidigt, medan de paternella kopiorna replikerade sent.
DNA-metylering ställer in tidbytaren
För att testa vad som orsakar denna tidsskillnad konstruerade forskarna stamceller där den normala metyleringsmönstret vid DMRs antingen raderades eller påtvingades på båda föräldrakromosomerna. När båda föräldrakopiorna av Dlk1–Dio3 DMR var metylerade replikerade hela regionen sent på båda kromosomerna. När metyleringen i stor utsträckning togs bort från båda kopior replikerade samma region tidigt på båda. Liknande experiment vid Snrpn ledde också till en förlust av tidsskillnader. Dessa resultat visar att föräldrarspecifik DNA-metylering är nödvändig för att skapa kontrasten tidigt–vs–sent mellan maternella och paternella kromosomer, åtminstone i dessa två domäner.
En lång RNA finjusterar tidig replikation
DNA-metylering ensam var dock inte hela förklaringen. Dlk1–Dio3-regionen producerar också ett långt icke-kodande RNA kallat Meg3 som del av en stor RNA "polycistron". På den maternella kromosomen tillåter ometylerade DMR att Meg3 uttrycks; på den paternella kromosomen håller metylering det tyst. Genom att skapa precisa deletioner som avstängde Meg3 samtidigt som DNA-metyleringen lämnades intakt visade författarna att förlust av Meg3-RNA fick vissa delar av den maternella domänen att skifta från tidig till senare replikation. Med andra ord hjälper Meg3-RNA till att främja tidig kopiering över närliggande sträckor av den maternella kromosomen och lägger till ett andra kontrollager ovanpå DNA-metylering.
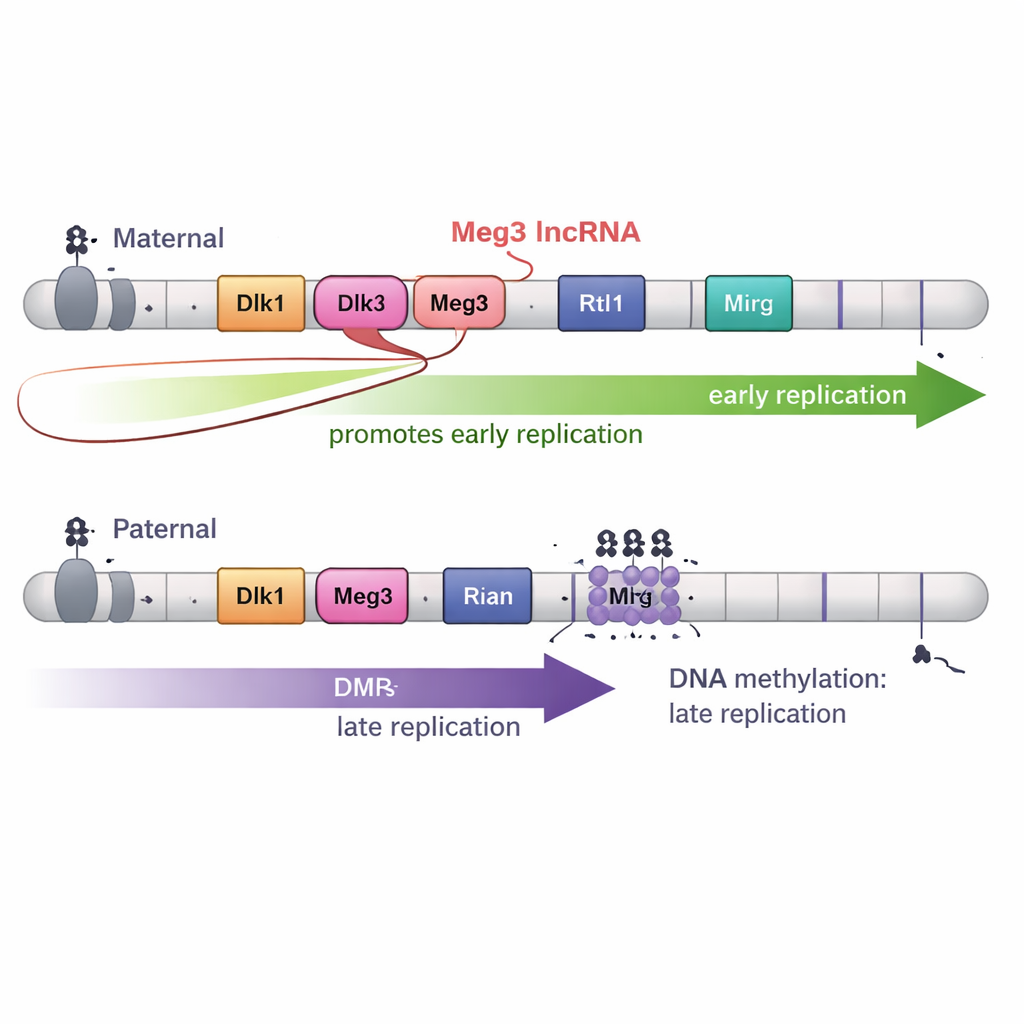
3D-veckning och utveckling ger ytterligare nyanser
Eftersom genomets vikning ofta är kopplad till replikationstiming kartlade teamet också kromosomarkitektur i 3D med hög detaljgrad. Överraskande nog stämde inte gränserna för 3D-domäner i Dlk1–Dio3-regionen överens med gränserna för tidig och sen replikation. Även när metyleringsmönstren förändrades och replikationstiming skiftade, förändrades de grundläggande vikningsenheterna—topologiskt associerande domäner—på andra sätt. Slutligen, när stamcellerna differentierades till neurala progenitorceller försvann de markanta tidsskillnaderna mellan maternella och paternella kopior till stor del, trots att imprintningsmärken och många aspekter av 3D-strukturen kvarstod. Detta tyder på att utvecklingssignalering kan åsidosätta det speciella tidigt–vs–sent-mönstret som ses i stamceller.
Vad detta betyder i enkla termer
Denna studie visar att i ett fåtal speciella genområden som minns vilken förälder de kom från styrs cellens DNA-kopieringsschema av en kombination av kemiska märkningar på DNA och långa icke-kodande RNA. DNA-metylering vid imprintningskontrollregioner sätter en grundläggande tidigt-eller-sent-timing för varje föräldrakromosom, och Meg3-lncRNA skjuter ytterligare på så att närliggande maternellt DNA kopieras tidigare. Dessa effekter verkar i stor utsträckning oberoende av hur kromosomen viks i 3D. Under utvecklingen, när celler specialiserar sig, bleknar denna ovanliga timing och visar att det är ett kännetecken för pluripotenta stamceller. Tillsammans förklarar arbetet hur föräldraepigenetiska "minnen" och icke-kodande RNA lokalt kan åsidosätta genomet vanliga replikationstidschema.
Citering: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Nyckelord: genomisk imprintning, DNA-metylering, replikationstiming, långa icke-kodande RNA, embryonala stamceller