Clear Sky Science · sv
Mikrobiell aktivering av GLP-2R dämpar mag-tarminflammation
Varför tarmvänligt protein spelar roll
När världen söker hållbara sätt att föda en växande befolkning vänder sig forskare bortom gårdar och fält till stora ståltankar där mikrober odlas för mat. Denna studie undersöker om ett sådant mikrobaserat protein kan göra mer än att bara näras oss. Forskarna frågade: kan ett protein framställt av ofarliga bakterier både tillgodose näringsbehov och aktivt skydda tarmen från inflammation, ett centralt problem vid sjukdomar som inflammatorisk tarmsjukdom och kemoterapiinducerade tarmskador?
En ny sorts protein från mikrober
Proteinet i centrum för detta arbete kommer från en jordbakterie kallad Methylococcus capsulatus Bath (McB). Istället för att ätas som levande bakterier bearbetas McB till ett mikrobiellt lyserat—i praktiken ett pulver av sönderrivna bakterieceller—som kommersiellt produceras under namnet FeedKind®. Möss fick dieter där detta lyserat stod för större delen av proteinet, antingen i en enkel eller i en mer människolik "komplex" diet. Teamet följde sedan hur denna kost förändrade sammansättningen av tarmens mikrober, immuncellerna som patrullerar tarmen, och hur väl tarmen tålde olika typer av skador.
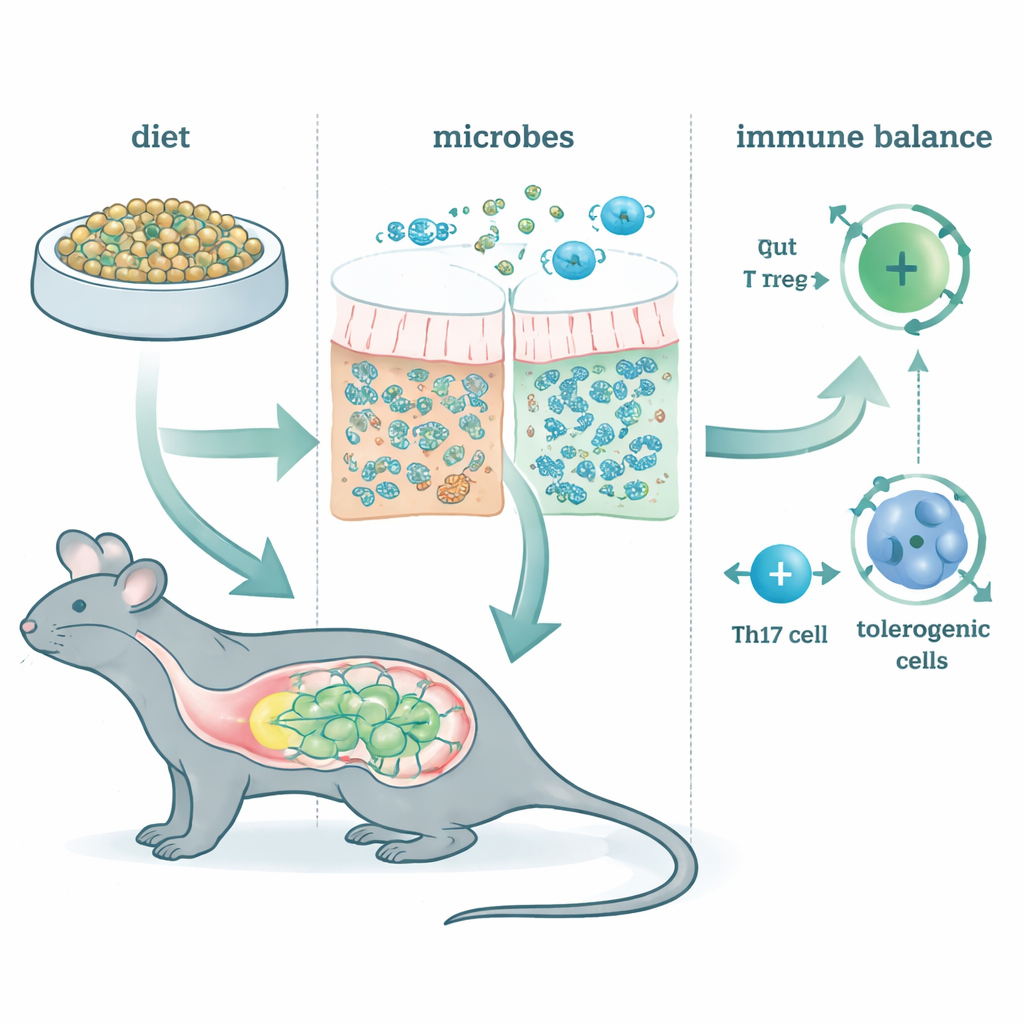
Omformning av det mikrobiella grannskapet
Att mata med McB förändrade snabbt och beständigt tarmmikrobiotan, oavsett vilken bakgrundsdiet djuren åt. Endast en mycket liten andel av McB i sig visade sig i avföringen, vilket betyder att materialet nästan helt användes upp i tarmen. Istället frodades ett fåtal bakteriearter från familjer som Lachnospiraceae och Bacteroidaceae. Genetiska analyser visade att dessa samhällen var berikade för fermentationsvägar som producerar kortkedjiga fettsyror—små molekyler som redan är kända för att ge näring åt tarmceller och påverka immuniteten. Med andra ord fungerade McB mindre som ett konventionellt protein och mer som ett riktat bränsle som omdefinierar vad de boende mikroberna gör.
Lära immunförsvaret tolerans
Författarna undersökte därefter nyckeltyper av T‑celler som hjälper avgöra om tarmen reagerar lugnt eller aggressivt på det som passerar igenom den. En grupp, perifert inducerade regulatoriska T‑celler (pTregs), hjälper till att förhindra överreaktion mot föda och vänliga mikrober. En annan grupp, Th17‑celler, kan antingen driva skadlig inflammation eller bidra till att upprätthålla en frisk barriär, beroende på deras "sinne". McB‑matning ökade starkt pTregs längs hela tarmen, även när större delen av tarmmikrobiotan utplånades med antibiotika. Däremot berodde McB:s effekter på Th17‑celler på närvaro och normal funktion av tarmbakterier. I mikrobiellt intakta möss försköts Th17‑celler av McB mot ett mer lugnande tillstånd, som producerar IL‑10 och är mindre inflammatoriskt. När fermentationen blockerades försvann denna tolerogena förskjutning, vilket understryker att McB delvis verkar genom att omdirigera mikrobi–immun‑samtal.
Skydd av tarmen vid skada
För att se om dessa förändringar omsattes i verkligt skydd utmanade forskarna möss med två hårda tarminsult. Det ena var ett cytostatikum, 5‑fluorouracil, som orsakar omfattande skada och förkortning av de fingersmala villi som absorberar näring. Det andra var en kemikalie (DSS) som framkallar kolit, en modell för inflammation i tjocktarmen. Möss på McB‑dieten förlorade mindre vikt, bibehöll längre villi och kolonlängd, visade färre blödande lesioner och hade lägre mikroskopiska skadescore i båda modellerna. Dessa fördelar kvarstod även när CD4‑T‑celler experimentellt avlägsnades, vilket tyder på att McB:s tarmbeskyddande effekter inte enbart beror på adaptiva immunceller utan också involverar direkta effekter på tarmens epitel.
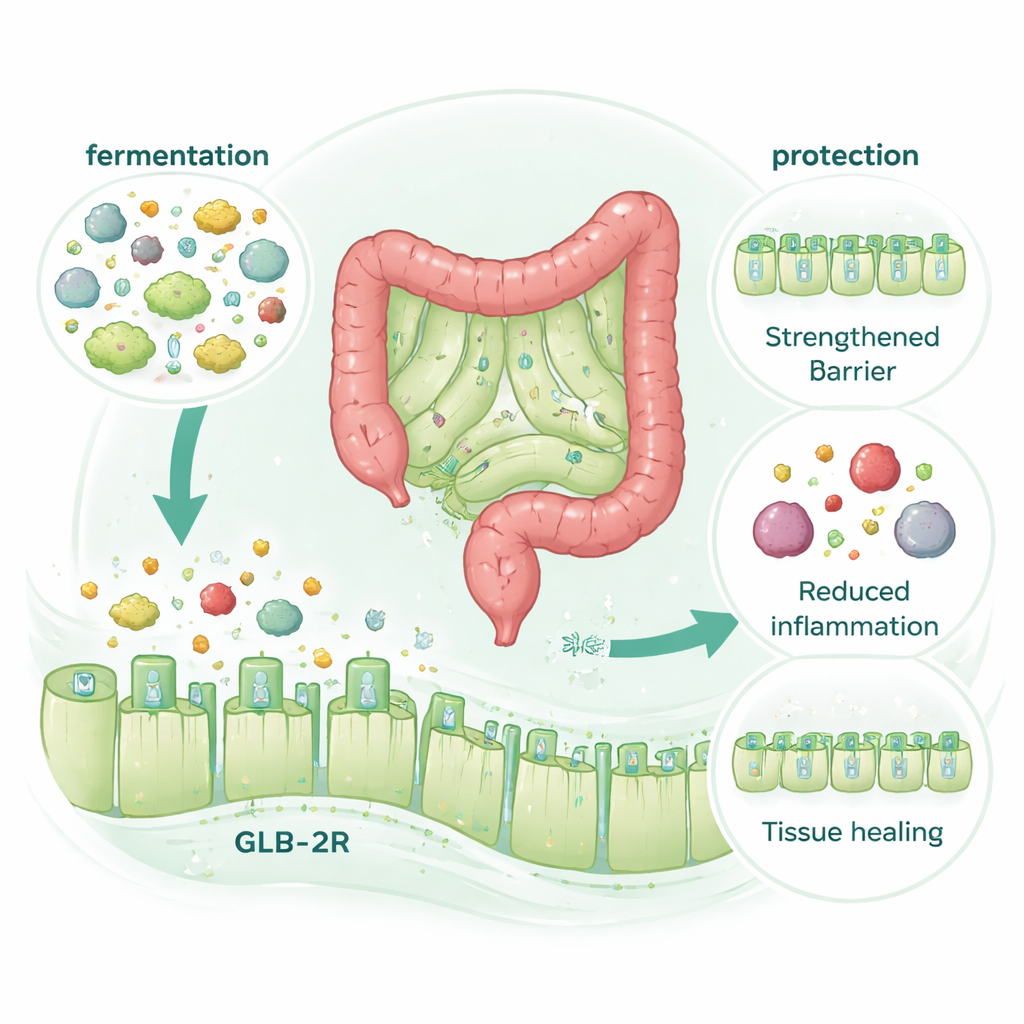
En hormonreceptor, men inget extra hormon
En överraskande vändning var upptäckten att McB:s skyddande effekt absolut krävde tarmens receptor för ett reparationsfrämjande hormon kallat GLP‑2 (GLP‑2‑receptorn, eller GLP‑2R), men inte den närbesläktade GLP‑1‑receptorn. När möss saknade GLP‑2R skyddade McB dem inte längre från skador orsakade av kemoterapi eller kolit. Ändå ökade inte McB själv GLP‑2‑nivåerna i blodet, även när matsmältning och hormonupplösning noggrant kontrollerades. Istället försvann fördelarna när mikrobiell fermentering i tjocktarmen kemiskt blockerades, även om den övergripande mikrobiotasammansättningen förändrades mycket lite. Detta pekar på en mekanism där mikrobiell nedbrytning av McB generar små föreningar som beter sig som GLP‑2‑"mimetika", aktiverar dess receptor för att stärka barriären och främja reparation utan extra hormonfrigöring.
Vad detta kan betyda för framtidens livsmedel
För en lekmannaläsare är huvudbudskapet att vissa framtida proteinkällor kanske kan utformas inte bara för att vara klimatvänliga, utan också för att aktivt stödja tarmhälsa. Hos möss omkopplade ett kommersiellt skalbart McB‑lyserat både immuniteten mot tolerans och hjälpte tarmen att stå emot svåra skador, genom två delvis oberoende vägar: en direkt förstärkning av regulatoriska T‑celler och en fermentationsdriven aktivering av GLP‑2‑receptorer som underlättar vävnadsreparation. Även om studier på människor fortfarande krävs, antyder arbetet att mikroberedda proteiner skulle kunna bilda en ny klass av "smarta" livsmedel—som kan föda oss, samarbeta med våra egna mikrober och tyst förstärka tarmens naturliga försvar mot inflammation.
Citering: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
Nyckelord: tarminflammation, mikrobiellt protein, mikrobiom, GLP-2-receptorn, regulatoriska T‑celler