Clear Sky Science · sv
Endotelial FUNDC1 reglerar metabolisk omprogrammering och övergången från fetma till diabetes via SIRT3/GATA2/endotelin-1-axeln
Varför blodkärlsceller spelar roll för fetma och diabetes
Fetma och typ 2-diabetes pekas ofta ut som följder av fettvävnad, levern eller bukspottskörteln. Den här studien lyfter fram en överraskande bov: det tunna cellskiktet som klär våra blodkärl, så kallade endotelceller. Forskarna visar att ett litet mitokondriellt protein i dessa celler, kallat FUNDC1, kan driva kroppen från enkel viktuppgång till fullt utvecklad diabetes genom att förändra hur blodkärlen kommunicerar med metabola organ.
Stress på kroppens inre "hud"
Endotelceller bildar ett omfattande och känsligt nätverk som kontrollerar blodflöde, näringstillförsel och signaler till intilliggande vävnader. Under friska förhållanden balanserar de avslappnande faktorer som kväveoxid mot sammandragande faktorer som endotelin-1 (ET-1). Vid fetma och tidig diabetes förskjuts denna balans mot ET-1, som inte bara drar ihop blodkärlen utan också stör hur fett-, muskel- och leverceller hanterar socker och fett. Författarna visar först i möss att kärldysfunktion uppträder redan efter bara två månader på en högfettkost, före tydlig insulinresistens, vilket tyder på att skadat endotel kan bidra till att utlösa metabol sjukdom snarare än bara svara på den.
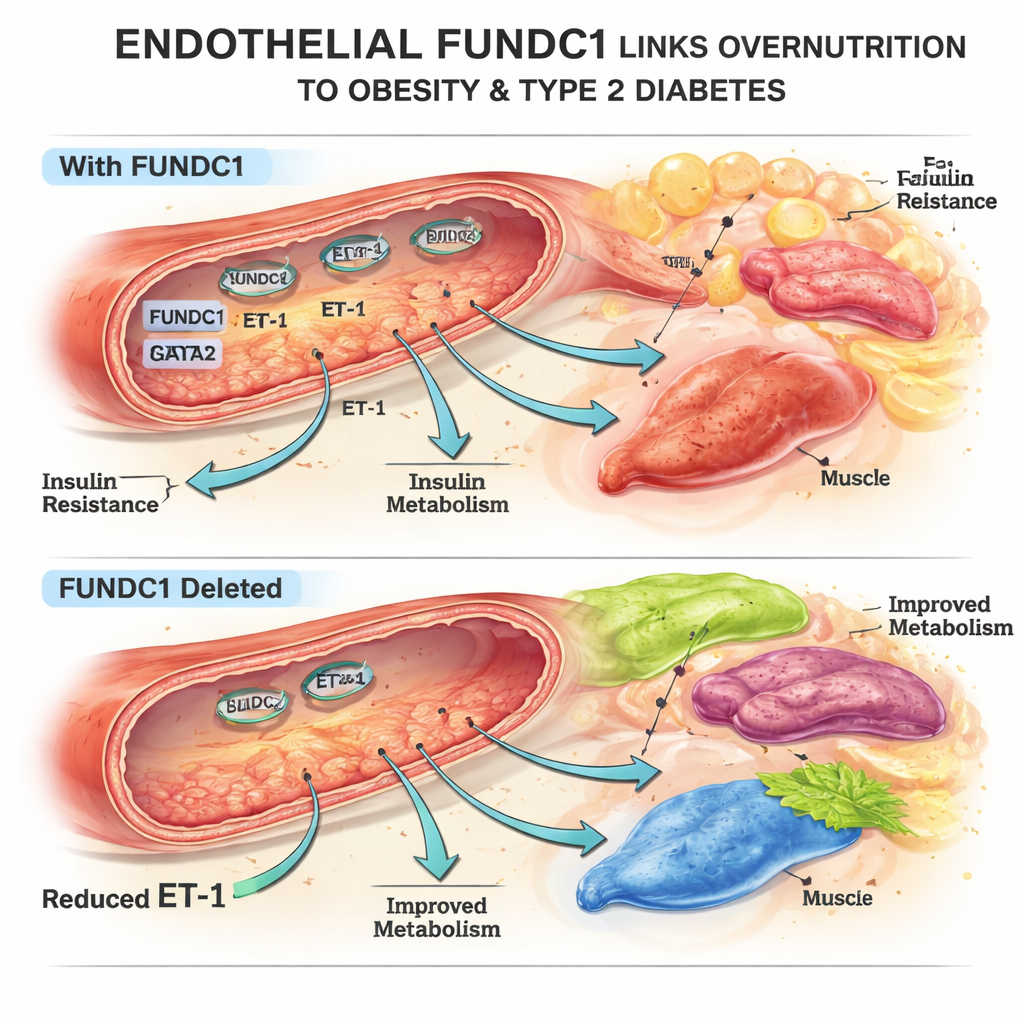
En mitokondriell brytare som formar kroppsfett
Teamet fokuserade på FUNDC1, ett protein på mitokondriernas yta, cellens energifabriker. I mus- och humana endotelceller utsatta för överskott av fett förändrades FUNDC1-nivåerna över tid: de sjönk först, för att sedan stiga kraftigt vid långvarig övernäring. Genom genetiskt modifierade möss som saknar FUNDC1 endast i endotelceller upptäckte forskarna att dessa djur delvis skyddades mot viktuppgång vid högfettkost, hade mindre kroppsfett, mindre fettceller och bättre blodsockerkontroll. Deras fett-, lever- och bruna fettvävnader svarade starkare på insulin, även om insulinnivåerna i sig inte var högre. Dessa förändringar kunde inte förklaras av skillnader i födointag eller aktivitet, utan pekar istället på hur kärlsystemet påverkar ämnesomsättningen.
En kemisk budbärare som driver insulinresistens
För att ta reda på hur endotelial FUNDC1 påverkar avlägsna organ screenade författarna flera ämnen som utsöndras av endotelceller. Ett framträdde: ET-1. När FUNDC1 togs bort i endotelceller sjönk ET-1-produktionen i blodkärlen och i blodbanan markant, både under normala och högfettkostförhållanden. Experiment i odlade adipocyter, leverceller och muskelceller visade att ET-1 främjade förfettcellstillväxt, förändrade fettlagring och nedbrytning samt förvärrade fettansamling i lever och muskel vid hög fettbelastning — ett mönster som är känt för att främja insulinresistens. I levande möss suddade infusion av ET-1 i början av en högfettkost ut de skyddande effekterna av endotelial FUNDC1-borttagning: kroppsvikt, fettmassa, blodsockerkontroll och kärlfunktion försämrades alla, vilket understryker ET-1 som en viktig länk mellan endotelet och metabol sjukdom.
En intern signalaxel: FUNDC1, SIRT3 och GATA2
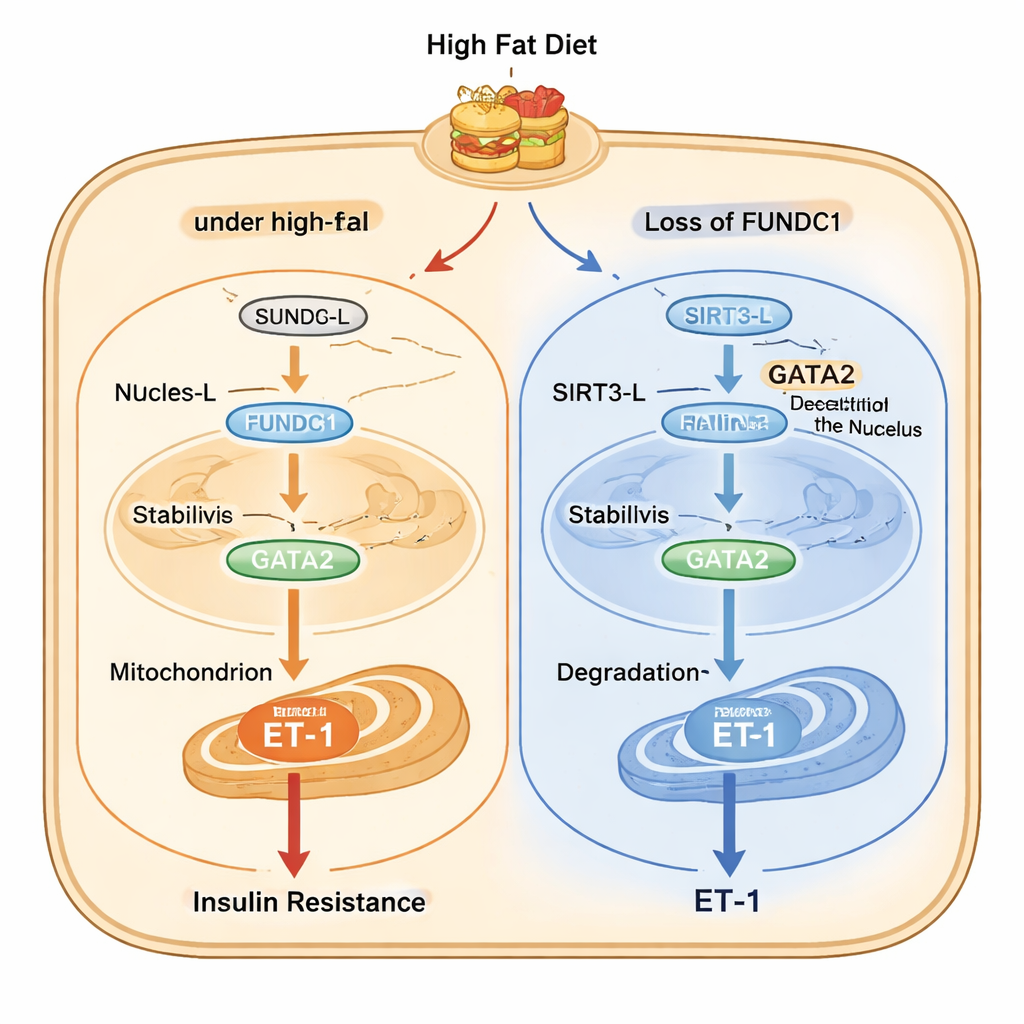
Studien kartlägger sedan en detaljerad molekylär kedja inne i endotelceller. Vid högfettstress flyttar en lång form av enzymet SIRT3 (SIRT3-L), som kan finnas både i kärnan och mitokondrierna, från kärnan in i mitokondrierna med hjälp av FUNDC1 och ett chaperonprotein kallat HSC70. När SIRT3-L fångas i mitokondrierna finns mindre SIRT3-L kvar i kärnan för att ta bort acetylgrupper från GATA2, en transkriptionsfaktor som ökar ET-1-genens aktivitet. Mer acetylerad GATA2 är mer stabil och driver mer ET-1-produktion. När FUNDC1 saknas stannar SIRT3-L i kärnan, där det deacetylerar GATA2, vilket leder till GATA2-nedbrytning och lägre ET-1-utflöde. Intressant nog främjar SIRT3 i sin tur FUNDC1-nedbrytning, vilket skapar en feedbackslinga som normalt håller vägen i schack men som blir dysreglerad vid kronisk övernäring.
Från modellmöss till mänsklig sjukdom
För att undersöka om denna mekanism är relevant hos människor analyserade forskarna blod och små artärer från individer med fetma och typ 2-diabetes samt från friska frivilliga. Patienter med båda tillstånden hade högre blodnivåer av ET-1 och högre uttryck av FUNDC1, GATA2 och ET-1-genen i sitt kärland. Mängden ET-1 i blod korrelerade tydligt med body mass index och långtidsblodsocker (HbA1c), och kärlets ET-1-gennivåer korrelerade starkt med FUNDC1 och GATA2. Dessa mönster speglar fynden hos mössen och stöder idén att en överaktiv FUNDC1–SIRT3–GATA2–ET-1-axel är verksam i mänsklig kärlvävnad under metabol stress.
En ny måltavla i kampen mot diabetes
För icke-specialister är huvudbudskapet att skador från överätande kan visa sig först i cellerna som klär våra blodkärl. Där hjälper ett mitokondriellt protein, FUNDC1, till att dirigera en reglerande enzym, SIRT3, bort från kärnan, vilket tillåter en annan faktor, GATA2, att öka produktionen av ET-1 — en stark hormonlik signal som främjar både kärlstelhet och insulinresistens. Att blockera denna väg — genom att minska endotelial FUNDC1-aktivitet eller dämpa ET-1 — skulle kunna hjälpa till att förhindra övergången från fetma till diabetes och samtidigt skydda blodkärlen.
Citering: Li, J., Li, D., Zhao, F. et al. Endothelial FUNDC1 regulates metabolic reprogramming and the obesity-diabetes transition through the SIRT3/GATA2/endothelin-1 axis. Nat Commun 17, 1836 (2026). https://doi.org/10.1038/s41467-026-68548-4
Nyckelord: endotelceller, mitokondrier, endotelin-1, fetma, typ 2-diabetes