Clear Sky Science · sv
Adipocytisk sclerostin loop3–LRP4-interaktion som krävs av sclerostin för att försämra kroppens lipid- och glukosmetabolism
Varför skelettet spelar roll för blodsockret
De flesta ser ben som livlös stomme, men benceller frisätter tyst hormoner som kommunicerar med resten av kroppen. Denna studie visar hur ett sådant benprotein, sclerostin, bidrar till kopplingen mellan två mycket vanliga problem hos äldre kvinnor: skört skelett (osteoporos) och typ 2-diabetes. Genom att blottlägga ett specifikt ”handslag” mellan sclerostin och fettceller beskriver forskarna en möjlighet att stärka benen och förbättra blodsockret och kolesterolet utan att belasta hjärtat mer.
En bensignal som går fel
Sclerostin är ett protein som främst bildas av benceller. Det bromsar normalt benbildning och – något överraskande – hjälper också till att skydda blodkärlen. Forskarna fokuserade på en liten del av proteinet, kallad loop3, och undersökte om den spelar roll i rubbad fett- och sockerhantering. De fann att kvinnor med postmenopausal osteoporos som också hade typ 2-diabetes, liksom personer nyupptäckta med diabetes, hade högre nivåer av sclerostin i blodet än jämförbara individer utan diabetes. Hos möss som matades med fettrik kost för att efterlikna metabol stress steg också sclerostinnivåerna i takt med viktuppgång, högre blodfetter och sämre blodsockerkontroll. Dessa mönster pekade på att överskott av sclerostin kan vara mer än en åskådare i metabol sjukdom.
Att dissekera en liten loop med stora effekter
För att förstå vad loop3 gör konstruerade forskarna möss där sclerostin var förändrat eller där dess loop3-segment togs bort. Möss som överproducerade normalt sclerostin samlade mer fett i vita fettdepåer, hade större fettceller, högre nivåer av cirkulerande fettsyror och sämre glukostolerans och insulinrespons än normala möss. När loop3 genetiskt togs bort eller subtilt muterades lättade dessa problem: fettvävnader blev mindre, fettceller krympte, blodfetter sjönk och sockerhanteringen förbättrades. Anmärkningsvärt nog uppstod liknande fördelar när möss behandlades med ett specialdesignat DNA-liknande läkemedel (en aptamer) som låser fast vid loop3 och förhindrar dess funktion, utan att ändra mängden sclerostin i blodet.
Hur fettceller ’hör’ bensignalen
Gruppen zoomade sedan in på fettceller för att se hur loop3 förmedlar sitt skadliga budskap. De riktade in sig på en receptor på fettcellens yta kallad LRP4, tidigare känd för att hjälpa sclerostin att verka på ben. Med cellkulturexperiment visade de att loop3 fysiskt binder till en specifik del av LRP4 på fettceller. Denna kontakt utlöste förändringar som ökade cellernas kapacitet att bygga upp och bryta ner fetter och att dra in mer glukos från blodet, vilket ledde till förstorade, överaktiva fettceller. När forskarna subtilt ändrade nyckelkomponenter i LRP4 så att loop3 inte längre kunde fästa, eller när de tillsatte en liten blockerande peptid som imiterade LRP4:s fästställe, minskade sclerostins effekt på fettansamling och glukosupptag kraftigt. Både i celler och i möss återställde blockering av loop3–LRP4-interaktionen mer normal fettcellstorlek och förbättrad glukostolerans.
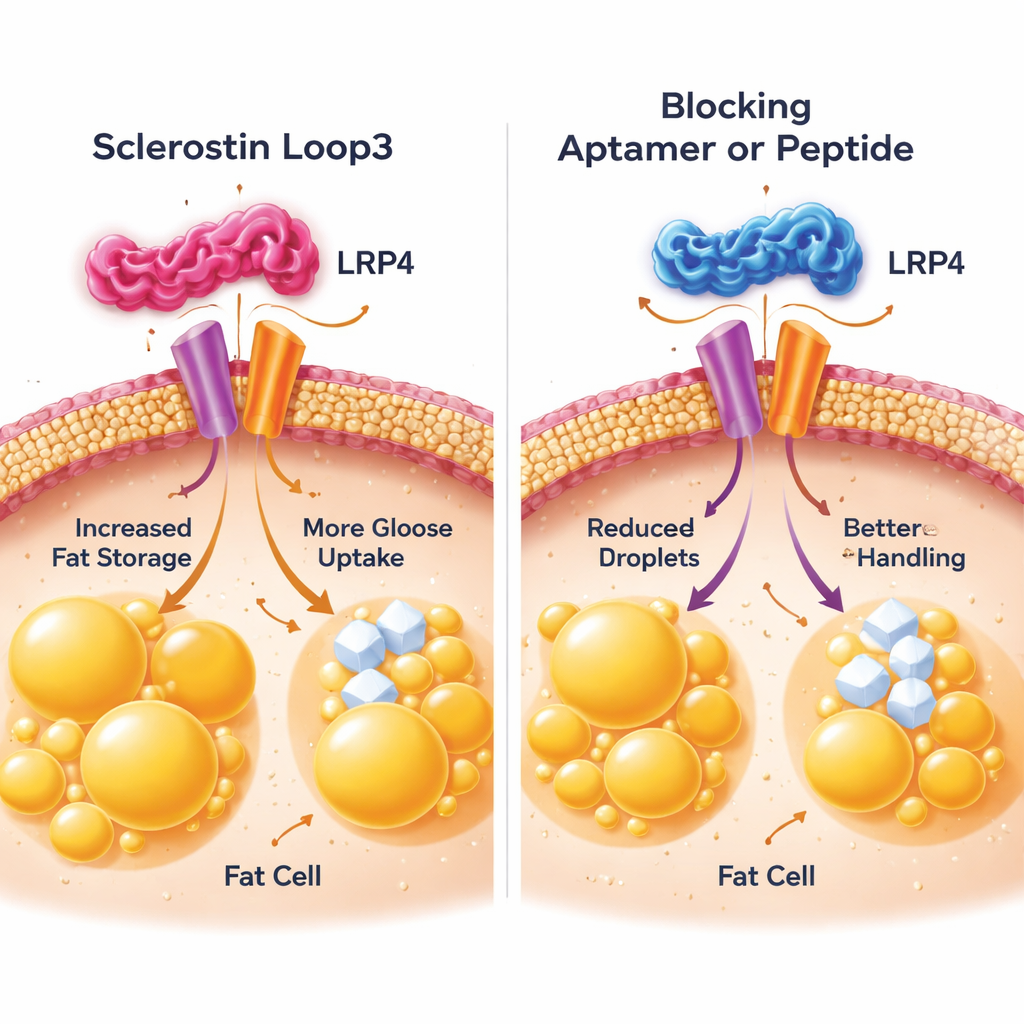
Starkare ben, hälsosammare ämnesomsättning
En viktig oro med befintliga sclerostin-blockerande läkemedel mot osteoporos är att även om de bygger upp ben och förbättrar metabolismen har tillsynsmyndigheter varnat för ökad risk för allvarliga hjärtproblem. Tidigare arbete från samma grupp visade att loop3 är avgörande för sclerostins broms av benbildning, men inte för dess hjärtskyddande funktioner. Här visar de vidare att inriktning på loop3 – antingen genom genetiska förändringar eller loop3-fokuserade läkemedel – förbättrar kroppens fett- och sockeromsättning i flera musmodeller samtidigt som benmassa och styrka ökar. Till skillnad från nuvarande mediciner utlöste denna strategi inte en kompensatorisk ökning av en annan benrelaterad inhibitor, DKK1, vilket kan dämpa långsiktiga fördelar.
Vad detta kan betyda för patienter
Enkelt uttryckt argumenterar studien för att en mycket liten del av ett benhormon hjälper till att driva både dålig benhälsa och metabol sjukdom genom att tala direkt med fettceller. Genom att avbryta samtalet mellan sclerostins loop3-segment och LRP4-receptorn på fettceller kan det bli möjligt att utforma behandlingar som stärker ben och normaliserar blodfetter och blodsocker, samtidigt som sclerostins hjärtskyddande funktioner lämnas intakta. För postmenopausala kvinnor som ofta ställs inför både osteoporos och typ 2-diabetes kan sådana loop3-riktade terapier en dag erbjuda ett säkrare, mer varaktigt sätt att hantera två tillstånd samtidigt.
Citering: Jiang, H., Tao, X., Yu, S. et al. Adipocytic sclerostin loop3-LRP4 interaction required by sclerostin to impair whole-body lipid and glucose metabolism. Nat Commun 17, 1812 (2026). https://doi.org/10.1038/s41467-026-68526-w
Nyckelord: sclerostin, loop3, LRP4, osteoporos, typ 2-diabetes