Clear Sky Science · sv
Palmitinsyra-utlöst B7H3-palmitoylering främjar immunsmitning
Varför denna forskning betyder något för cancerpatienter
De flesta har hört att nya immunterapiläkemedel kan hjälpa immunsystemet att angripa cancer, men många patienter med vanlig kolorektal (tarm) cancer får liten nytta. Denna studie avslöjar ett dolt biokemiskt knep som kolorektala tumörer använder för att skyla sig från immattack, och den pekar på en ny typ av läkemedel — en kort peptid — som skulle kunna få immunterapin att fungera bättre för dessa patienter.
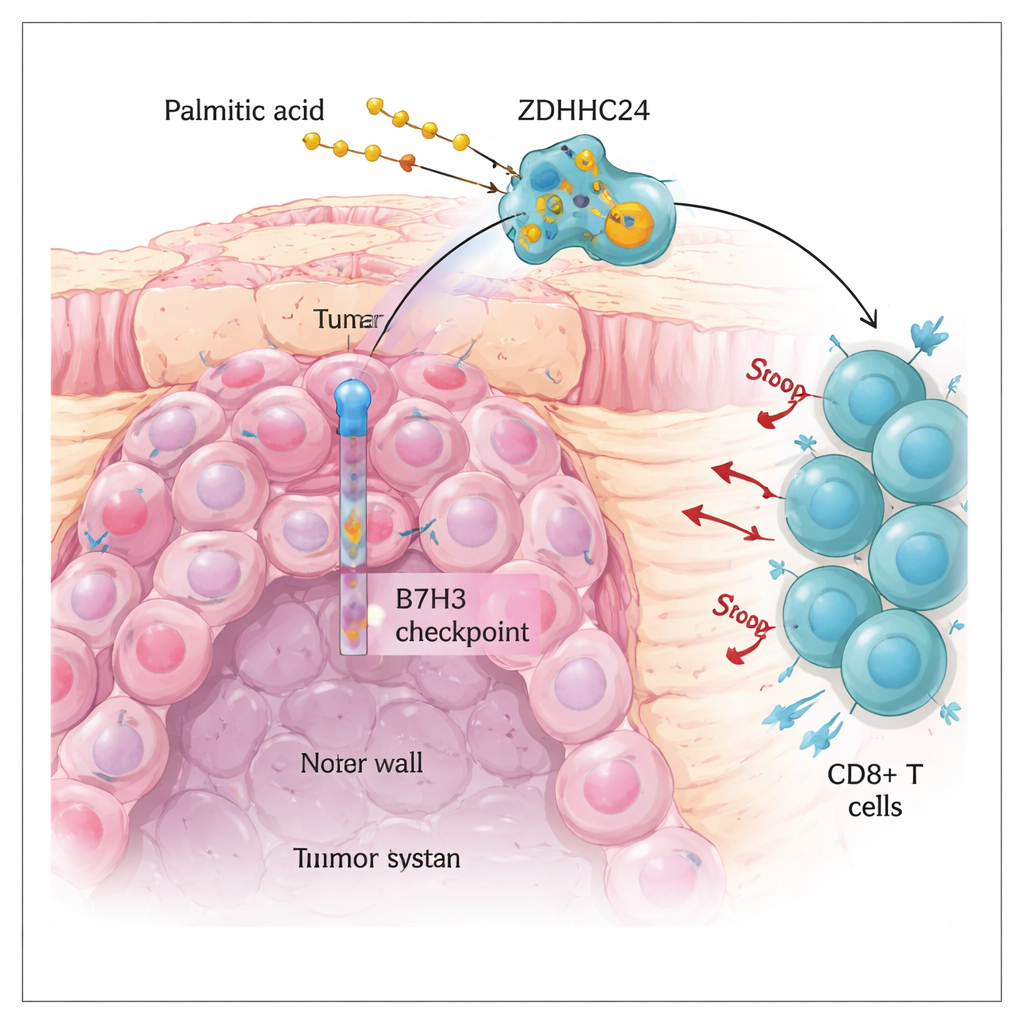
Ett hinder i dagens immunterapi mot tarmcancer
Kolorektal cancer är en av de vanligaste cancerformerna globalt. Immunterapier som släpper på immunsystemets ”bromsar”, såsom PD‑1‑ och PD‑L1‑hämmare, har förändrat vården för en minoritet av patienter vars tumörer bär många DNA‑fel (så kallade MSI‑H‑tumörer). Tyvärr är de flesta kolorektala tumörer mikrosatellitstabila (MSS) och svarar dåligt på dessa behandlingar. Författarna fokuserade på en annan bromsmolekyl kallad B7H3, som sitter på tumörcellens yta och dämpar aktiviteten hos mördande immunceller, särskilt CD8+ T‑celler. De fann att B7H3‑proteinet är starkt förhöjt i MSS‑tumörer och kopplat till sämre överlevnad, även om den underliggande B7H3‑genen inte är mer aktiv. Denna diskrepans pekade på en viktig fråga: vad håller B7H3‑proteinet så rikligt närvarande på tumörcellerna?
Hur ett vanligt fett hjälper tumörer att gömma sig
Forskargruppen misstänkte att tumörmetabolismen kan stabilisera B7H3. Genom att jämföra genaktivitet och småmolekylprofiler hos MSS‑ och MSI‑H‑kolorektala tumörer upptäckte de att många fettrelaterade vägar skiljer sig åt, där en fettsyra, palmitinsyra, stack ut. När de exponerade koloncancerceller för flera fettnedbrytningsprodukter i labbet orsakade endast palmitinsyra en tydlig ökning av B7H3‑proteinnivåer. Ytterligare experiment visade varför: palmitinsyra går in i en kemisk modifieringsprocess kallad palmitoylering, där en fettsvans fästs på specifika platser på proteiner. Denna modifiering, utförd av ett enzym som heter ZDHHC24 vid en enda cysteinposition i B7H3, gjorde B7H3 mer stabilt och mer rikt på tumörcellytan.
Blockera sopvägen för en immunbroms
Celler tar normalt bort oönskade eller skadade proteiner via system som fungerar som återvinning och sophantering. Forskarna visade att B7H3 huvudsakligen bryts ner via en cellulär ”självätande” väg kallad autofagi, som använder en receptorprotein SQSTM1/p62 för att märka last för destruktion. När B7H3 var palmitoylerat band det dåligt till denna receptor och undgick autofagisk nedbrytning, vilket ledde till ihållande höga nivåer av immunbromsen. När palmitoyleringsstället muterades så att det inte längre kunde bära fettetiketten, eller när enzymet ZDHHC24 togs bort, dirigerades B7H3 mer effektivt till cellens ”soppåsar” och bröts ner. I möss växte tumörer som saknade palmitoylerat B7H3 långsammare, ändrade inte sin inneboende tillväxthastighet i immundefekta djur, och visade dramatiskt fler CD8+ T‑celler och starkare tumör‑dödande aktivitet. Detta visade att modifieringen främst verkar genom att avväpna immuniteten, inte genom att ändra hur snabbt cancercellerna delar sig.
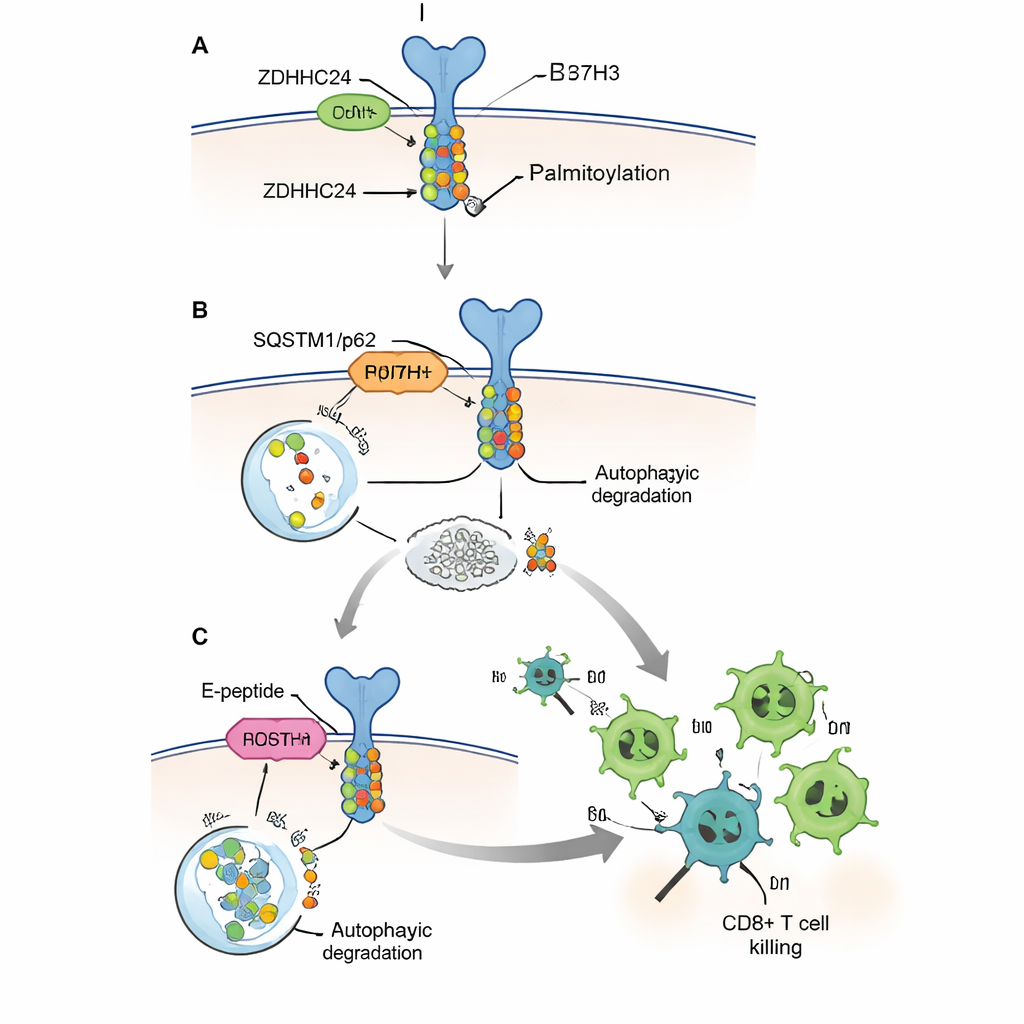
Sänka skölden och stärka T‑celler
Eftersom det inte är praktiskt att fullt ut eliminera ZDHHC24 eller B7H3 genetiskt hos patienter designade författarna en kort, cellpenetrerande peptid som de kallar E‑peptiden. Den imiterar en liten del av B7H3‑proteinet som normalt binder till ZDHHC24, och fungerar som en avledare som hindrar enzymet från att modifiera verkliga B7H3‑molekyler. I odlade celler minskade E‑peptiden B7H3‑palmitoylering och proteinnivåer, återställde dess igenkänning av autofagimaskineriet och möjliggjorde för mänskliga CD8+ T‑celler att döda tumörceller mer effektivt. I flera musmodeller, inklusive en humaniserad mus som bar mänskliga immunceller och mänskliga kolorektala tumörer, krympte injektioner av E‑peptiden tumörer, ökade antalet CD8+ T‑celler i dem och ökade produktionen av viktiga mördarmolekyler såsom granzym B och interferon‑gamma.
En ny partner för befintlig immunterapi
Slutligen undersökte forskarna om denna strategi kunde fungera tillsammans med standard PD‑1‑blockad. I musmodeller av kolorektal cancer gav både E‑peptid ensam och anti‑PD‑1‑antikropp ensam viss tumörkontroll. Men i kombination gav de två behandlingarna mycket kraftigare och mer långvarig tumörundertryckning, i vissa fall orsakade tumörerna att försvinna och mer än fördubblade den genomsnittliga överlevnaden jämfört med kontroller. Detta tyder på att avväpna B7H3‑skölden genom att kapa dess fett"anker" kan komplettera befintliga checkpoint‑läkemedel som riktar sig mot PD‑1‑vägen.
Vad detta betyder för framtida cancerbehandling
Enkelt uttryckt visar denna studie att en vanlig kostfett, palmitinsyra, kan hijackas av kolorektala tumörer för att kemiskt bepansra ett immunhämmande protein (B7H3) och hjälpa cancern att gömma sig. Genom att blockera just den kemiska fästningen kunde författarna avplåstra pansaret, låta cellens egna nedbrytningssystem ta bort B7H3 och åter öppna för CD8+ T‑celler att anfalla. Även om E‑peptiden själv är ett tidigt experimentellt verktyg identifierar arbetet B7H3‑palmitoylering — och dess enzym ZDHHC24 — som lovande läkemedelsmål. Om liknande medel visar sig säkra och effektiva hos människor, kan de en dag göra fler kolorektala tumörer från ”kalla” tumörer som ignorerar immunterapi till ”heta” tumörer som immunsystemet kan känna igen och förstöra.
Citering: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Nyckelord: immunterapi mot kolorektal cancer, B7H3-checkpoint, palmitinsyrametabolism, proteinputatoylering, CD8 T-cells tumörimmunitet