Clear Sky Science · sv
Guldfiskens makrofager omvandlar fysikaliska sårsignaler till snabb vaskulär permeabilisering
Hur en liten fisk lär oss om svullnad vid sår
När du skrapar upp knät blir området snabbt rött, svullet och läckande av vätska. Denna snabba förändring i närliggande blodkärl är avgörande för att bekämpa infektion och starta reparation, men exakt hur kroppen känner av skada och reagerar på några sekunder har varit svårt att se i realtid. Genom att använda genomskinliga zebrafisklarver och avancerad liveavbildning avslöjar den här studien hur specialiserade immunceller som omsluter blodkärlen omvandlar det fysiska stöten från ett sår till nästan omedelbar kärlläckage, vilket ger ny insikt i inflammation, läkning och till och med människans lungskador.
Att se hur skadan sprider sig genom kroppen
Forskarna arbetade med unga zebrafiskar vars genomskinliga kroppar lät dem iaktta celler och blodkärl i arbete under mikroskopet. De skar av spetsen av stjärtfenan och fyllde cirkulationen med ett lysande färgämne som stannar kvar i friska kärl. När de skadade fiskarna placerades tillbaka i normalt sötvatten skapade den plötsliga inflödet av vatten i vävnaderna ett ”osmotiskt chock” runt såret. Inom minuter vidgades närliggande kärl och började läcka det fluorescerande färgämnet ut i omgivande vävnad, vilket återskapar den svullnad och vätskning som sker runt mänskliga sår. Genom att växla fiskarna mellan vanlig och särskilt balanserade saltlösningar eller sockerlösningar visade teamet att denna snabba kärlpermeabilisering i hög grad beror på osmotiska förändringar snarare än enbart på mekanisk vävnadsskada.
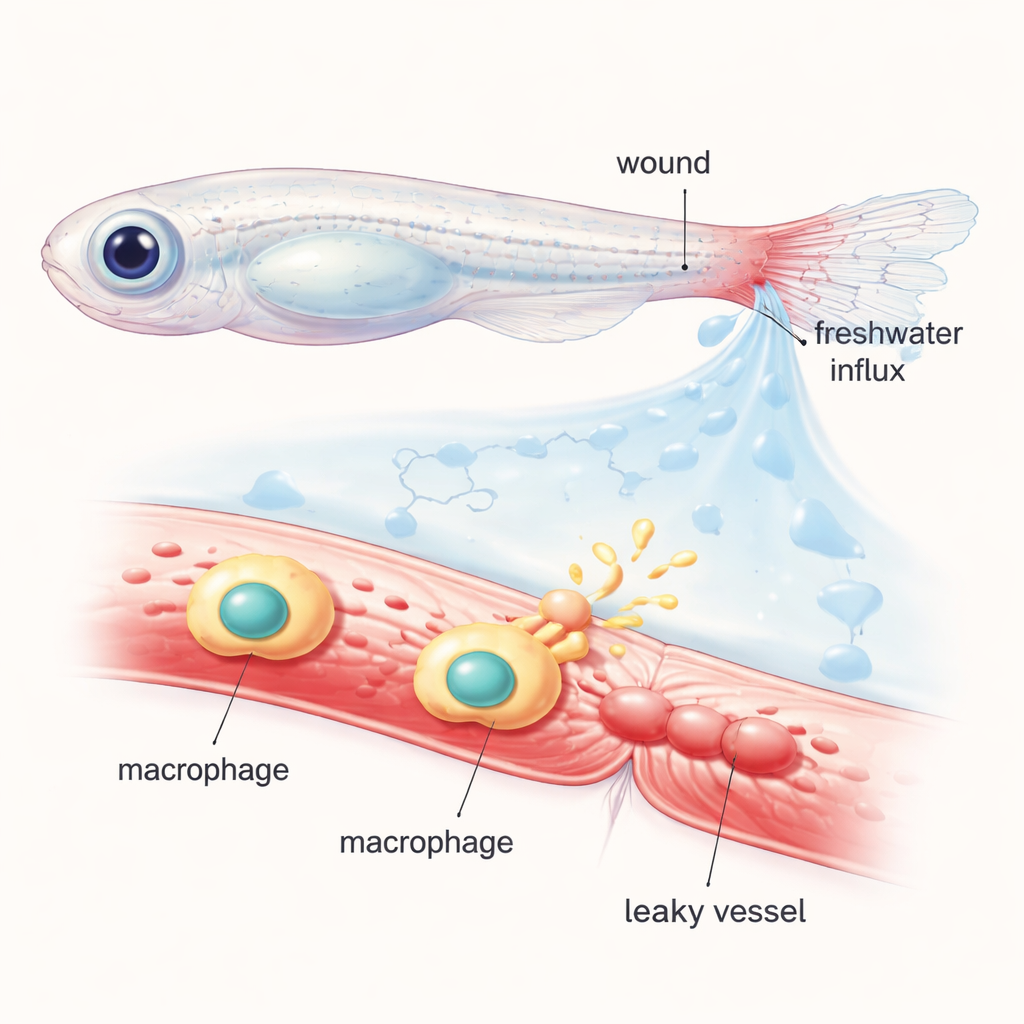
Att följa de kemiska budbärarna bakom läckaget
För att ta reda på vilka molekyler som förvandlar den fysiska chocken till en läcksignal undersökte forskarna en familj fettsyraderivat som kallas eikosanoider, härledda från arakidonsyra. Dessa lipider är välkända för sina roller i inflammation och blodflöde. Med genetiska mutanter och läkemedel stängde de selektivt av enskilda enzymer i eikosanoidvägen. Att blockera ett nyckelenzym som heter Alox5a (5-lipoxygenas) eller dess partner Lta4h minskade kraftigt hur mycket färgämne som läckte ut från blodkärlen efter osmotisk chock, utan att stoppa själva sårläkningen. Däremot hade störning av andra relaterade enzymer liten effekt. Detta pekade på en specifik gren av lipidvägen som en huvuddrivare av den snabba läcksvarsreaktionen, nästan som en kemisk ventil som kan öppnas eller stängas vid behov.
Den överraskande rollen hos kärlknutna immunceller
Blodet innehåller olika typer av immunceller, och hos zebrafisklarver är neutrofiler och makrofager de viktigaste aktörerna. Forskarteamet använde en smart genetisk metod för att selektivt förstöra antingen neutrofiler eller makrofager innan såret skapades. Att ta bort neutrofiler gav liten skillnad i kärlläckage. Men när makrofager utplånades sjönk läcksreaktionen med ungefär hälften, vilket speglade effekten av att blockera Alox5a–Lta4h-lipidvägen. Viktigt nog stoppade dessa manipulationer inte sårets snabba tillslutning, vilket visar att leukocytrekrytering och kärlläckage kan kontrolleras till viss del oberoende av varandra. Detta avslöjade perivaskulära makrofager—makrofager som sitter tätt längs utsidan av kärlen—som nyckelöversättare mellan fysisk skada och vaskulärt beteende.
Från nukleär töjning till kemisk signal
Hur upptäcker dessa perivaskulära makrofager ett sår som kan ligga en bit bort? Svaret ligger i hur deras cellkärnor reagerar på mekanisk stress. När den osmotiska chocken från såret sprider sig genom närliggande vävnad orsakar vatteninflöde subtil cellsvullnad och deformation av kärnan. Forskarna taggade ett mekanosensitivt enzym kallat cPla2 med en fluorescerande markör och uttryckte det specifikt i makrofager. Efter skada i normalt sötvatten flyttade cPla2 snabbt ut till den inre ytan av kärnmembranet i makrofager i en våg som svepte genom vävnaden med ungefär 50 mikrometer per sekund, i överensstämmelse med spridningen av upplösta salter. Denna translokation var beroende av hypotoniska förhållanden och var mycket svagare i isotona lösningar. Makrofager nära blodkärlen visade särskilt skarpa, reversibla pulser av nukleär cPla2-bindning, vilket i sin tur frigör arakidonsyra för omvandling till de läckinducerande lipiderna.
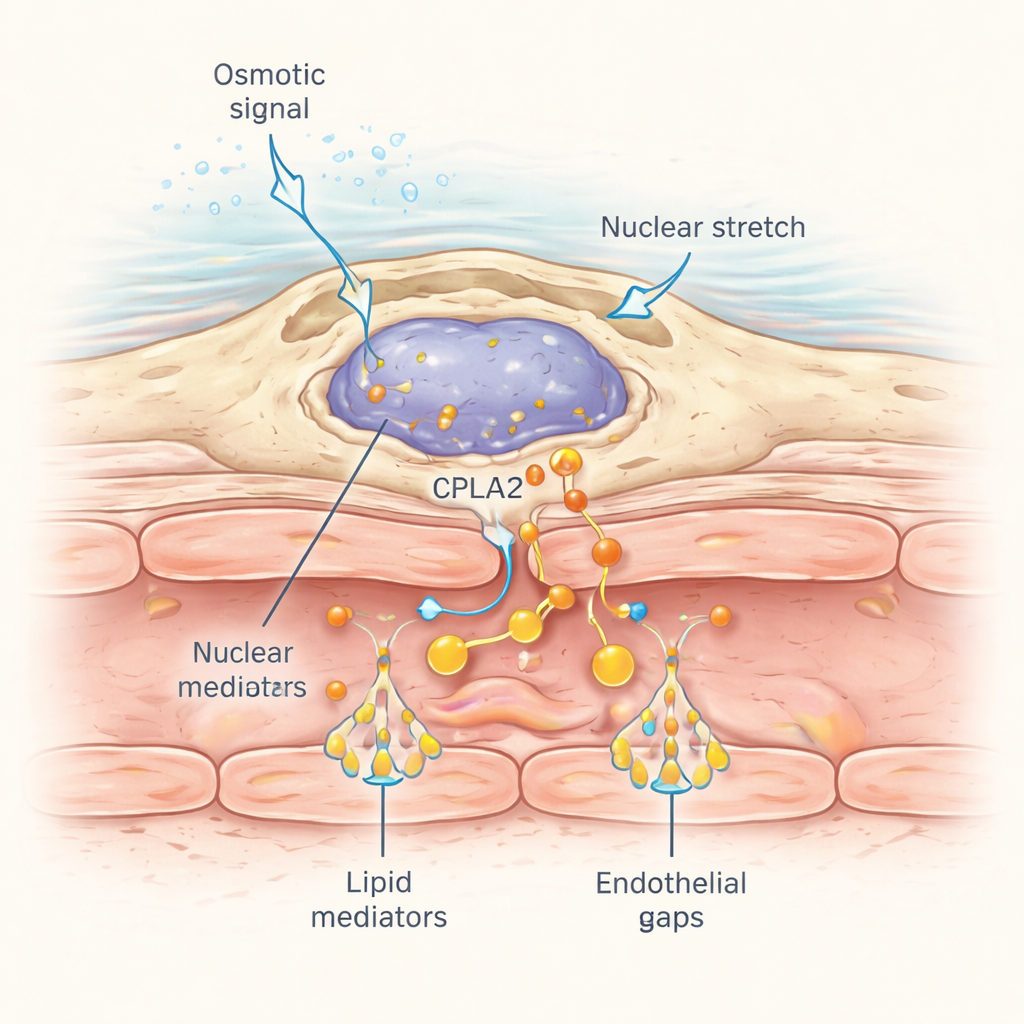
Varför detta spelar roll bortom fiskar
Kort sagt visar den här studien att vissa makrofager fungerar som fysiska väktare: de känner av töjningen i vävnad och kärnmembran orsakad av osmotiska förändringar vid ett sår, aktiverar cPla2 vid kärnans yta och producerar snabbt lipidbudbärare som får närliggande blodkärl att ”öppna grindarna” så att vätska och immunkomponenter kan strömma in. Även om zebrafiskar lever i sötvatten och möter unika osmotiska utmaningar, sannolikt finns liknande mekanosensitiva vägar i mänsklig vävnad som utsätts för varierande tryck och flöden, till exempel lungorna vid mekanisk ventilation. Att förstå hur nukleär töjning och lipidsignaler i realtid reglerar kärlpermeabilitet kan så småningom informera behandlingar som finjusterar inflammation—antingen genom att dämpa skadligt läckage vid tillstånd som akut lungsjukdom eller genom att förstärka hjälpsamma svar för att påskynda vävnadsreparation.
Citering: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Nyckelord: sårläkning, blodkärl, makrofager, inflammation, zebrafisk