Clear Sky Science · sv
Ultratunna vätskeceller för mikrosekundupplöst kryo‑EM
Titta på proteiner i arbete i realtid
Många av de maskiner som håller våra celler vid liv består av proteiner, och vi vet ofta hur dessa proteiner ser ut när de är frusna i viss position. Men det vi egentligen vill se är hur de förflyttar sig medan de utför sina uppgifter. Den här studien introducerar ett nytt sätt att iaktta dessa rörelser på otroligt korta tidsskalor — mikrosekunder — utan att offra den knivskarpa detaljnivå som modern kryo‑elektronmikroskopi (kryo‑EM) kan leverera.
En ny glugg mot den mikroskopiska världen
Kryo‑EM har revolutionerat strukturell biologi genom att avbilda blixtfrysta proteiner med nästan atomär upplösning. Traditionella metoder visar dock bara stillbilder. För att fånga rörelse utvecklade forskare "mikrosekundupplöst kryo‑EM", där en laser kort smälter en frusen provfilm så att proteinerna kan röra sig, och sedan fryses provet snabbt igen för att fånga dem i nya positioner. Problemet har varit att den tunna vätskefilm som lasern skapar tenderar att sönderfalla efter några tiotals mikrosekunder, vilket begränsar hur länge proteinerna kan observeras. Det nya arbetet löser denna flaskhals genom att innesluta provet i en ultratunn vätskecell, vilket håller det stabilt tillräckligt länge för att kunna följa långsammare, mer komplexa rörelser.
Bygga en ultratunn vätskecell
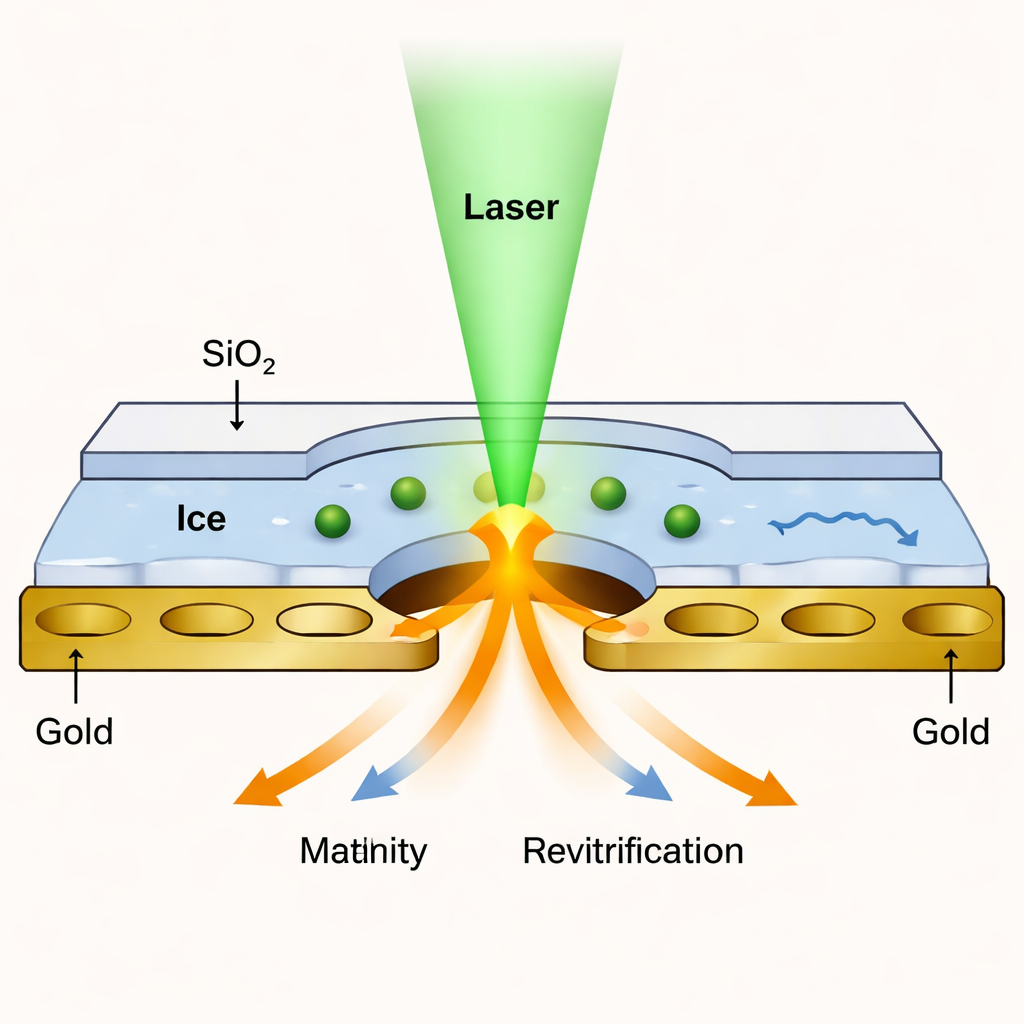
Gruppen skapade ett slags nanoskiktat smörgås: proteininnehållet fryses på ett standard perforerat guldraster, och båda sidor beläggs sedan med kiseloxidlager som är endast omkring 1,4 nanometer tjocka — bara några atomer. Dessa glasliknande lager fungerar som genomskinliga lock som hindrar vätskan från att avdunsta när lasern smälter isen. Korta laserpulser värmer det förseglade provet till en kontrollerad temperatur och tillåter det sedan att återfrysa inom mikrosekunder. Eftersom membranen är så tunna släpper de ändå igenom tillräckligt många elektroner för att mikroskopet ska kunna producera bilder med nästan samma upplösning som vid konventionell kryo‑EM, ner till cirka 1,7–1,8 ångström för ett testprotein kallat apoferritin.
Skarpare vyer och rättvisare vinklar
En dold utmaning i kryo‑EM är att proteiner tenderar att fastna vid luft–vatten‑gränssnittet i det tunna iskiktet, vilket får dem att rada upp sig i liknande orienteringar och försvårar rekonstruktionen av en fullständig 3D‑bild. Kiseloxidbeläggningarna i dessa vätskeceller ändrar ytan från vatten–luft till vatten–fast och gör den mer vattenvänlig. Som ett resultat är det mindre sannolikt att proteinerna klibbar fast i en enda ställning. När författarna testade en stor cellulär maskin kallad 50S‑ribosomsubenhet fann de att partiklarnas vinkelfördelning blev nästan helt jämn, vilket i praktiken eliminerar det långvariga problemet med "föredragen orientering" samtidigt som hög upplösning bibehölls i de slutliga rekonstruktionerna.
Tajma rörelsen hos en molekylär hävstång
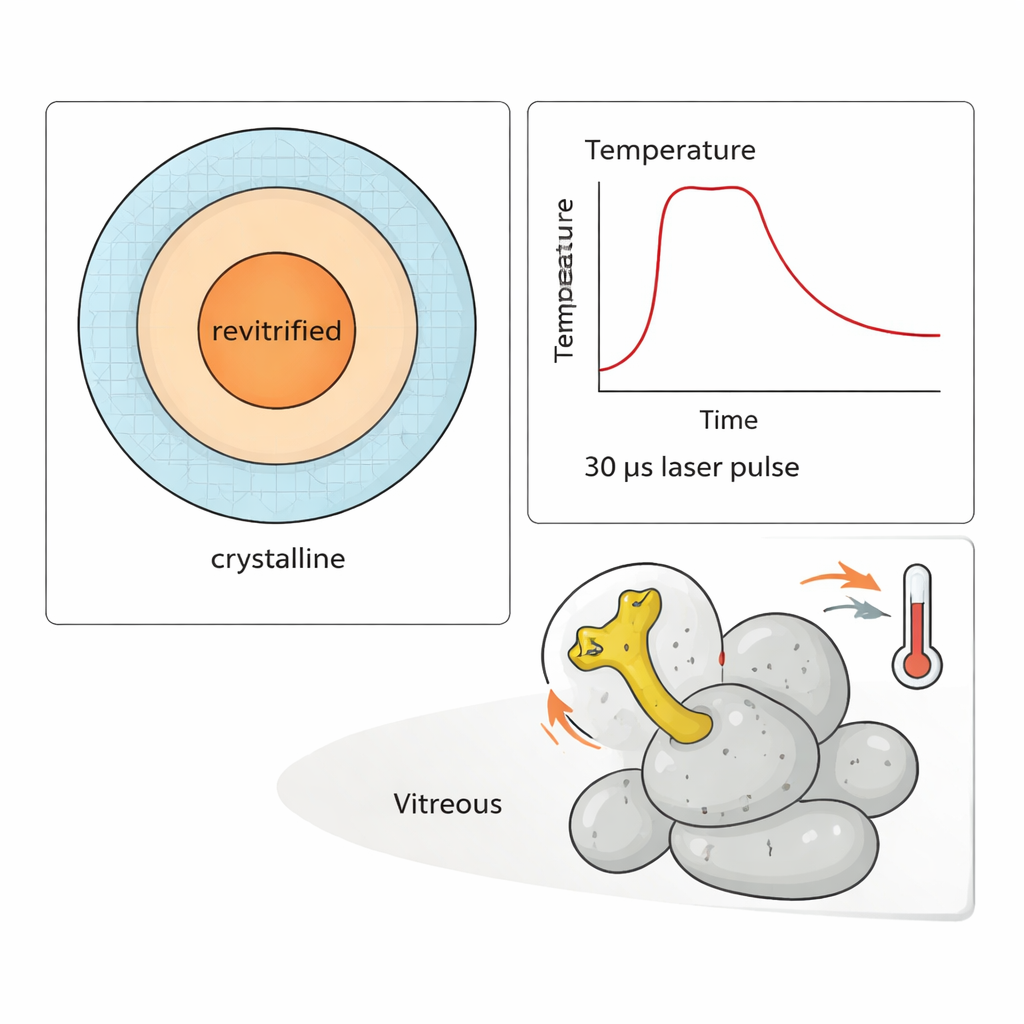
För att visa metodens styrka genomförde forskarna ett "temperaturhopp"-experiment på 50S‑subenheten. En flexibel arm på denna partikel, känd som L1‑stjälken, svänger som en hävstång under proteinsyntesen. Genom att leverera pulserade laserpaket om 30 mikrosekunder kunde de värma provet till olika temperaturer i upp till omkring 300 mikrosekunder och sedan återfrysa det. Simuleringar och mätningar av vilka regioner som återfrös som glas gjorde det möjligt att uppskatta temperaturen för varje observerad partikel. Genom att analysera tusentals bilder visade de att amplituden i L1‑stjälkens rörelse tydligt ökar med temperaturen — men först efter att hundratals mikrosekunder har förflutit. I de tidiga tidsfönstren speglar konformationsfördelningen fortfarande ursprungstillståndet vid rumstemperatur innan frysning.
Varför detta spelar roll för framtidens biologi
För icke‑specialister är huvudbudskapet att denna design av ultratunna vätskeceller dramatiskt förlänger hur länge proteiner kan observeras i rörelse utan att strukturella detaljer suddas ut. Den flyttar mikrosekundupplöst kryo‑EM från att bara fånga de allra snabbaste händelserna till att kunna undersöka långsammare, biologiskt viktiga omstruktureringar, som den fördröjda responsen hos L1‑stjälken till en värmepuls. Med ytterligare förfiningar skulle detta tillvägagångssätt kunna överbrygga klyftan till millisekundområdet och längre, och det erbjuder också nya sätt att förbereda prov, minska bildartefakter och trigga reaktioner direkt på rastritningen. I praktiska termer betyder det att forskare kommer närmare att skapa "molekylfilmer" som kopplar proteiners former till vad de faktiskt gör inne i levande celler.
Citering: Curtis, W.A., Wenz, J., Krüger, C.R. et al. Ultrathin liquid cells for microsecond time-resolved cryo-EM. Nat Commun 17, 1799 (2026). https://doi.org/10.1038/s41467-026-68515-z
Nyckelord: tidsupplöst kryo‑EM, proteindynamik, vätskecellselektronmikroskopi, ribosomens L1‑stjälk, ultratunna kiseloxidmembran