Clear Sky Science · sv
Mekaniska krafter från intercellulär peptidsjälvsammansättning driver sfäroidbildning
Bygger små vävnader i labbet
Forskare tävlar om att skapa miniatyrversioner av mänskliga vävnader som beter sig som originalet. Dessa levande modeller kan göra testning av cancerläkemedel säkrare och föra nya behandlingar för diabetes och andra sjukdomar närmare verklighet. Denna studie introducerar en smart metod för att få celler att bilda realistiska tredimensionella kluster, komplett med egna primitiva ”blodkärlsliknande” nätverk som förbättrar näringstillförsel och funktion.
Hjälper celler att känna sin omgivning
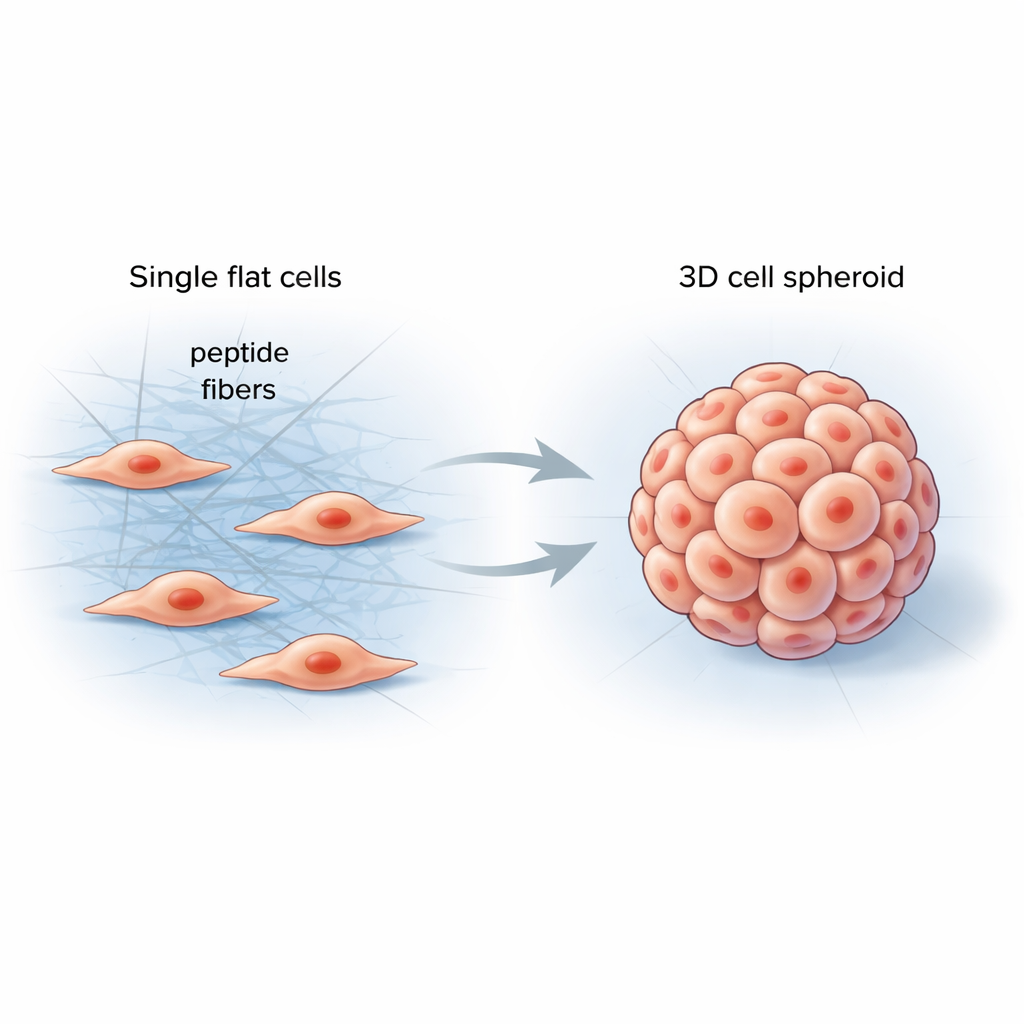
I våra kroppar lever celler i en mjuk men strukturerad omgivning kallad extracellulär matrix — ett nätverk av proteiner som stödjer vävnader och ger ständiga mekaniska signaler till cellerna. Konventionella laboratoriematerial har svårt att efterlikna denna komplexitet och ger ofta platta cellager som beter sig mycket annorlunda än riktiga organ eller tumörer. Forskarna ville konstruera ett enkelt, programmerbart material som bildas direkt mellan celler, hårdnar deras omgivning på ett kontrollerat sätt och skjuter dem mot mer naturliga tredimensionella former.
Smarta peptider som monterar sig mellan celler
Teamet skapade korta proteinkedjor, kallade peptider, som kan länka ihop sig till långa, tunna fibrer när de möter specifika enzymer på cellsystem. När dessa peptider tillsattes till cancerceller var de inaktiva först, som en klar lösning. När cellernas egna enzymer klippte bort en del av molekylen självmonterade peptiderna snabbt till ett fibröst nätverk som omslöt och låg mellan närliggande celler. Detta nya fibernät ändrade de lokala mekaniska krafterna, vilket uppmuntrade cellerna att dra i varandra, omforma sitt interna skelett och samla sig till runda 3D-sfäroider istället för att sprida ut sig i ett skikt.
Från cellkluster till kärl-liknande nätverk
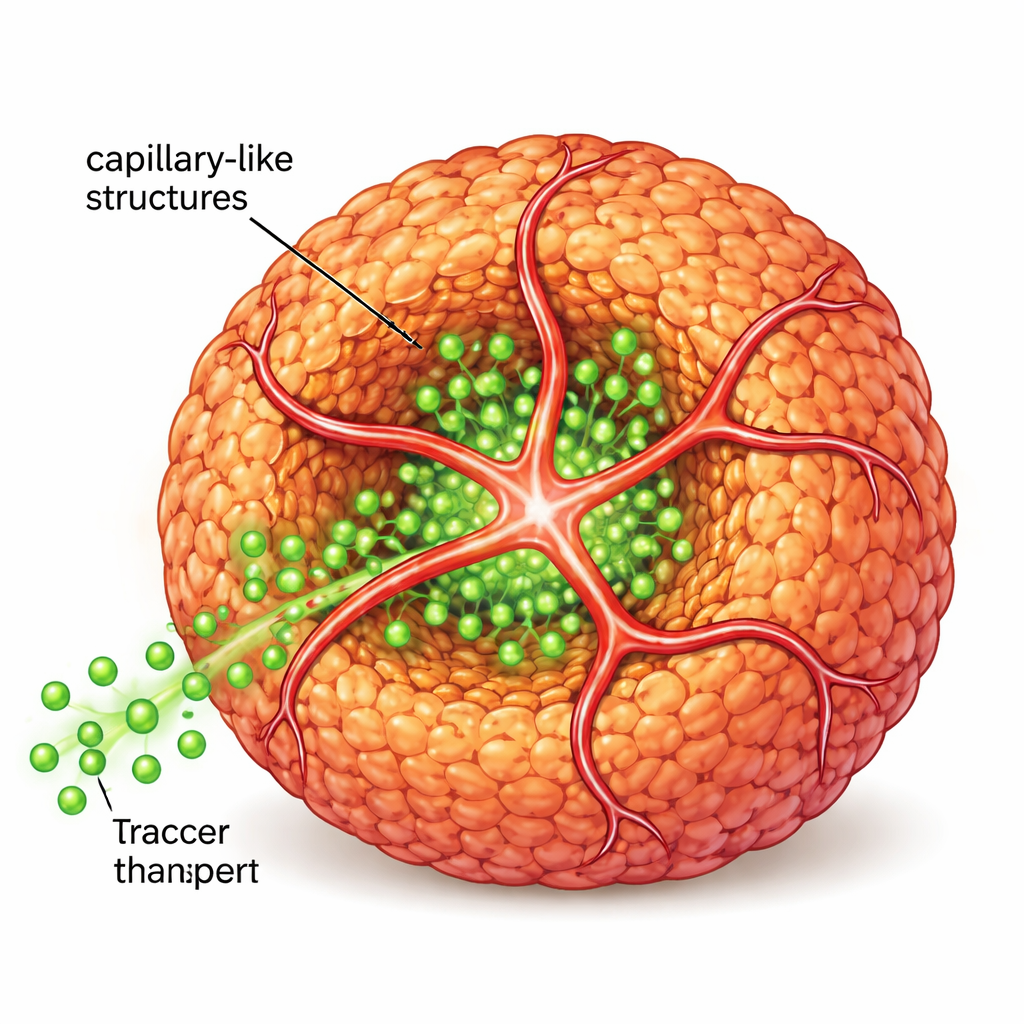
För att komma närmare riktig vävnad införde forskarna därefter humana endotelceller, den celltyp som normalt bekläder blodkärl, tillsammans med en andra peptid som bar en liten ”adressetikett” som attraherar dessa celler. Tillsammans bildade de ursprungliga och modifierade peptiderna ett gemensamt nanofibröst skelett. Endotelcellerna använde detta skelett för att skjuta ut rörliknande förgreningar som omslöt och trängde in i sfäroiderna, och skapade kapillär-liknande strukturer. När teamet flödade fluorescerande sockerliknande molekyler runt dessa strukturer såg de mycket djupare penetration in i sfäroidkärnan jämfört med sfäroider utan dessa inre rör, vilket visar att transporten av näringsämnen och signaler blev avsevärt förbättrad.
Närmare riktiga tumörer och fungerande öar
Genaktivitetens profilering visade att tumörsfäroider med kapillär-liknande strukturer mer liknade patientprover från glioblastom än traditionella platta kulturer eller icke-vasculariserade sfäroider. I möss växte sfäroider som innehöll dessa primitiva kärlnätverk till större, mer vaskulariserade tumörer, vilket indikerar att in vitro-modellen fångar centrala egenskaper hos verkligt tumörbeteende. Samma strategi tillämpades på pankreatiska betaceller, som normalt lever i mycket vaskulariserade öar och utsöndrar insulin som svar på glukos. När betacellsfäroider utrustades med kapillär-liknande strukturer med hjälp av peptidsystemet och endotelceller visade de mycket starkare och mer fint reglerad insulinfrisättning, vilket tyder på ett kraftfullt verktyg för diabetesforskning och regenerativ medicin.
Varför detta spelar roll för framtida terapier
Genom att låta enkla peptider självmontera mellan levande celler erbjuder detta arbete ett generellt recept för att bygga miniatyriserade, vaskulariserade vävnader som känns och fungerar mer som de i kroppen. De resulterande sfäroidena speglar patienttumörer och fungerande öar bättre, vilket gör dem värdefulla för läkemedelstestning, studier av sjukdomsmekanismer och utformning av nya cellbaserade terapier. För icke-specialister är huvudpoängen att ge labbodlade celler rätt ”känsla” och små kärl-liknande nätverk kan dramatiskt förbättra hur troget de efterliknar mänsklig vävnad, och potentiellt snabba på vägen från grundforskning till effektiva behandlingar.
Citering: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Nyckelord: vävnadsteknik, cancermodeller, angiogenes, organoider, peptidsjälvsammansättning