Clear Sky Science · sv
Intermittent fasta hämmar Tp53-drivet gliom genom tarmfloramedierad metionin‑m6A‑reglering
Varför en paus för tarmen kan sakta ner dödliga hjärntumörer
Glioblastom är en av de mest aggressiva hjärncancerformerna, och nuvarande behandlingar — kirurgi, strålning och cytostatika — förlänger ofta patienters livstid bara marginellt. Denna studie ställer en enkel men potenta fråga med stora konsekvenser för vardagen: kan vår ätstil, särskilt intermittent fasta, ändra tarmbakterier och blodkemi tillräckligt för att märkbart sakta vissa hjärntumörer?
Olika varianter av samma hjärncancer
Alla glioblastom är inte likadana. Författarna fokuserar på två huvudsakliga genetiska typer, definierade av förändringar i generna TP53 och CDKN2A. Dessa gener hjälper till att styra hur celler växer eller dör. Med mössmodeller som nära efterliknar varje mänsklig subtyp visar forskarna att intermittent fasta — 24 timmar utan mat följt av 24 timmar med mat — inte gynnar alla tumörer lika mycket. Möss med TP53‑typ tumörer levde längre och hade mindre tumörer när de fastade, medan möss med CDKN2A‑typ tumörer visade liten nytta. Det tyder på att fasta kan vara effektivt beroende på tumörens genetiska kopplingar.
Från ätmönster till tarmbakterier till hjärnkemi
Teamet undersökte hur fasta ger denna selektiva effekt. Eftersom den totala matmängden hölls densamma mellan grupperna var skillnaden tidpunkten för ätandet. Den tidpunkten omformade kraftfullt tarmmikrobiotan — den omfattande bakteriegemenskapen i tarmen. Hos fastande TP53‑möss minskade vissa bakteriegrupper som effektivt producerar aminosyran metionin, såsom specifika Alistipes‑ och Prevotella‑stammar. Eftersom metionin är ett essentiellt byggmaterial som djur måste få från kosten eller tarmbakterier innebar detta mikrobskift mindre metionin som flöt från tarmen till blodet och slutligen till hjärnan.
Hur en enda näringsämne finjusterar cancersignalering
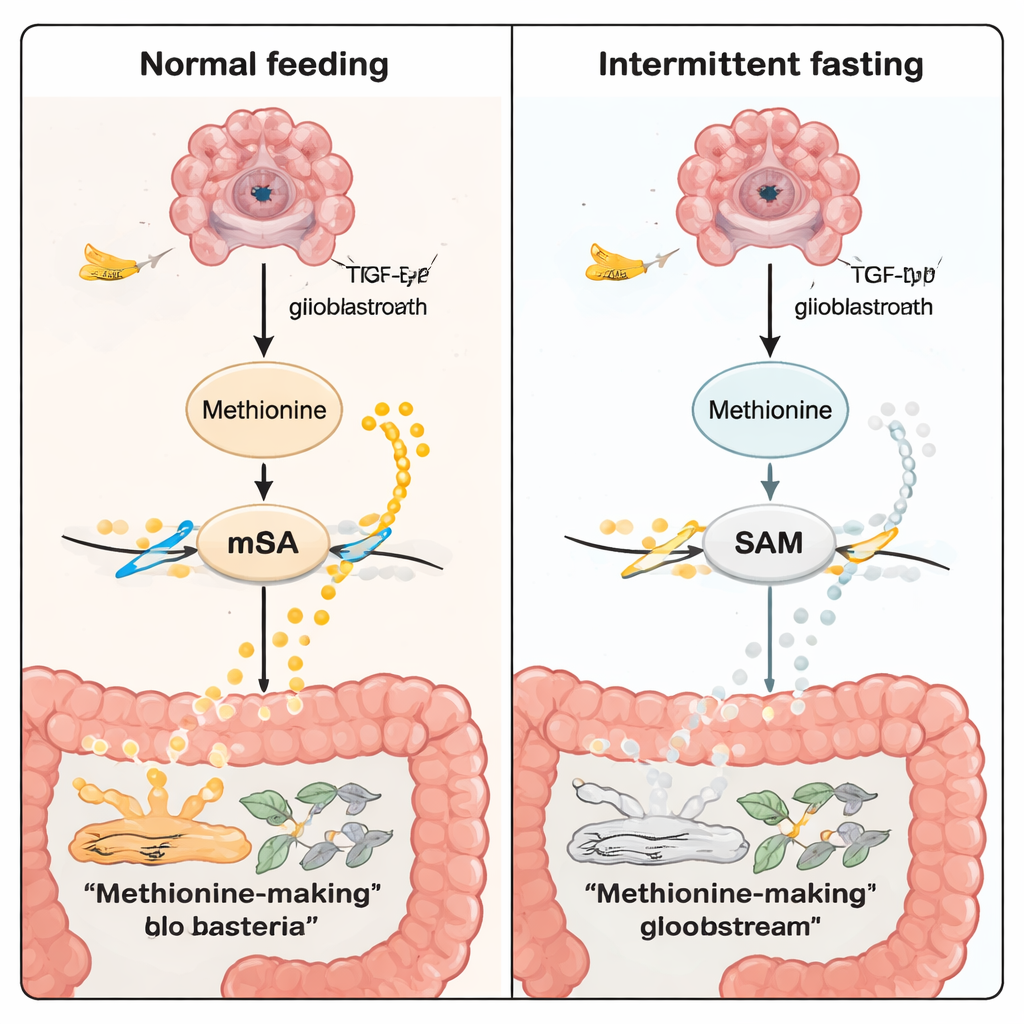
Metionin är inte bara ett näringsämne; det är också råmaterial för S‑adenosylmetionin (SAM), cellens universella “metylgivare.” SAM driver en kemisk märkningsprocess på RNA kallad m6A. Dessa markeringar hjälper till att reglera hur kraftigt vissa gener uttrycks. I TP53‑tumörmodellen sänkte fasta nivåerna av metionin och SAM i blodet och i hjärntumörområden. Genom flera lager av omikstekniker — standard RNA‑sekvensering, single‑cell RNA‑profilering och rumsliga kartor över både genaktivitet och metaboliter — fann forskarna färre m6A‑markeringar på viktiga cancerkopplade RNA under fasta. Ett viktigt mål var TGFB2, en gen i TGF‑β‑signalvägen, som är känd för att driva tumörtillväxt och invasion. Vid fasta minskade både enzymet METTL3 (som skriver m6A‑märken) och TGFB2, och TGF‑β‑signaleringen försvagades.
Bevisa orsak och verkan med riktade ingrepp
För att gå bortom korrelation utförde forskarna “räddnings”‑experiment. De blockerade METTL3 med ett läkemedel eller överförde tarmbakterier från fastande möss till normalt matade möss, och såg att tumörtillväxten avstannade även utan fasta — vilket stöder idén att både mikrobiotan och m6A‑maskineriet är viktiga aktörer. Omvänt, när fastande möss gavs extra metionin eller behandlades med ett läkemedel som ökar m6A‑märken, växte deras tumörer mer som hos normalt matade möss och överlevnadsfördelen försvann. Viktigt är att störning av tarmbakterier med bredspektrumantibiotika utsuddade många av de fasta‑relaterade förändringarna, vilket betonar att tarmgemenskapen är en central nod i denna kedja av händelser.
Vad detta betyder för människor och framtida behandlingar
För en lekmannaläsare är kärnbudskapet att inte alla cancerformer, eller ens alla glioblastom, kommer att reagera likadant på en koststrategi som intermittent fasta. I TP53‑typ gliom verkar fasta ”kommunicera” med hjärnan via tarmen: den omformar tarmbakterierna, vilket i sin tur minskar metioninproduktionen, reducerar kemisk märkning av RNA och dämpar kraftfulla tillväxtsignaler inne i tumörcellerna. Även om detta arbete är gjort i möss och kräver omsorgsfull klinisk översättning pekar det mot en framtid där enkla livsstilsmönster, tarmmikrobiota‑baserade behandlingar och läkemedel som riktar metionin‑ eller m6A‑vägar kan skräddarsys efter en patients tumörs genetiska subtyp.
Citering: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Nyckelord: intermittent fasta, glioblastom, tarmmikrobiom, metioninmetabolism, RNA m6A‑modifiering