Clear Sky Science · sv
Simultan svavelväteoxidation och sulfatreduktion för intracellulär redoxhomeostas under mycket sura förhållanden
Varför rengöring av giftiga gaser kräver kloka mikrober
Många industrier släpper ut svavelväte, en giftig gas som luktar ruttna ägg, kan korrodera utrustning, förorena luften och skada arbetare. För att sanera denna gas förlitar sig ingenjörer i allt högre grad på mikrober som omvandlar sulfider till mindre farliga svavelformer. Denna artikel avslöjar en oväntad mikrobiell strategi: en nyidentifierad Mycobacterium som driver två normalt motsatta kemiska vägar samtidigt för att både snabbt avgifta svavelväte och skydda sig från intern skada, även vid extremt sura förhållanden.
En dragkamp i svavelcykeln
I naturen drivs svavelcykeln av två motsatta reaktioner. Vissa mikrober oxiderar sulfider (den mest reducerade, giftiga formen) till mindre skadliga produkter som elementärt svavel eller sulfat och får energi i processen. Andra går åt motsatt håll och reducerar sulfat tillbaka till sulfiden för att bygga viktiga cellkomponenter som svavelhaltiga aminosyror. Eftersom dessa reaktioner tar ut varandra har biologer länge antagit att en och samma cell skulle undvika att köra båda samtidigt; att göra det verkar slöseri, ungefär som att värma och kyla ett hus med fönstren öppna. 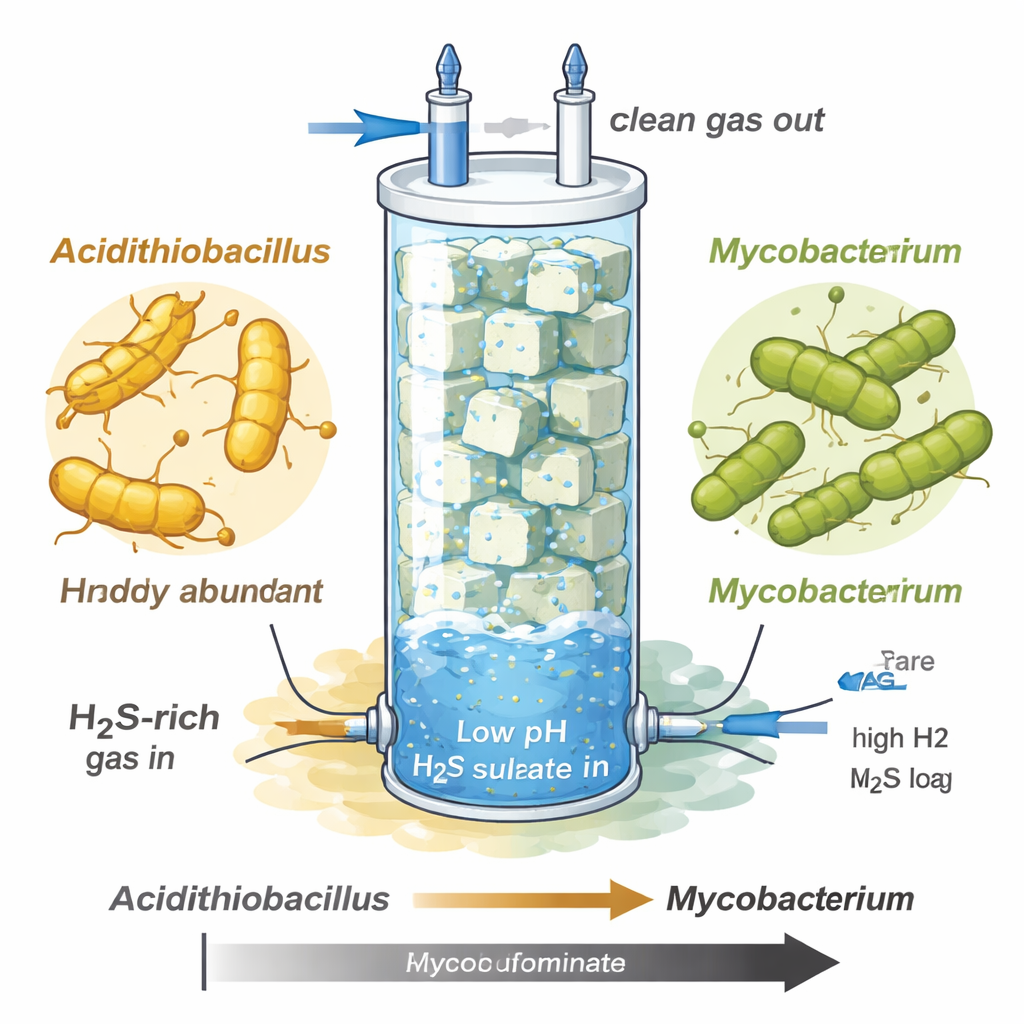
Att hitta en överlevare i en extrem reaktor
Forskarna studerade ett biotricklingfilter—en hög glaspelare fylld med skumkubbar—konstruerat för att rena svavelväte från gasströmmar liknande rå biogas eller naturgas. När de ökade sulfidhastigheten och höll systemet mycket surt (pH omkring 1–1,5) förändrades mikrobiella gemenskapen dramatiskt. Inledningsvis frodades en välkänd sulfidexiderare kallad Acidithiobacillus och omvandlade stora delar av sulfiden till sulfat, men den kollapsade senare under extrem sulfidsstress. Istället tog en tidigare okaraktäriserad Mycobacterium-art, betecknad MAG-M116, över nästan hela gemenskapen, trots att den växte långsammare under den tidiga, mildare fasen.
En mikrob som bryter de vanliga reglerna
Analyser på genetisk och proteinnivå visade att MAG-M116 har en ovanlig metabolism. Den bär ett nyckelenzym, sulfide:kinon-oxireduktas, som oxiderar sulfiden endast så långt som till fast elementärt svavel, vilket ackumuleras som små partiklar. Samtidigt har mikroben en full uppsättning gener för assimilativ sulfatreduktion, den väg som tar upp sulfat i cellen och reducerar det för att bygga aminosyror som cystein och metionin. Under höga sulfidsförhållanden var båda vägarna aktiverade samtidigt. Sulfidoxidation skickade elektroner in i cellens energimaskineri, medan sulfatreduktion fångade upp en del av denna elektronflöde och kopplade de två riktningarna i svavelcykeln inom en enda cell.
Att göra en ”slösaktig” cykel till en säkerhetsventil
Att köra båda vägarna samtidigt kan i teorin verka meningslöst—att bränna energi utan nettovinst. Men gruppen visar att för MAG-M116 fungerar det som en säkerhetsventil för överskottselktroner. Att oxidera stora mängder sulfider frigör en våg av elektroner in i cellens respiratoriska kedja, som kan läcka och generera reaktiva syreföreningar (ROS)—skadliga molekyler som angriper DNA, proteiner och membran. Genom att aktivt reducera sulfat till aminosyror dirigerar cellen 10–14 % av dessa elektroner till konstruktivt arbete, vilket minskar uppbyggnaden av ett överreducerat, läckagebenäget tillstånd. Experiment som jämförde förhållanden med och utan sulfat visade att aktiv sulfatreduktion minskade ROS-produktionen med upp till cirka 60 % och förhindrade ackumulering av reducerade kofaktorer som annars skulle driva oxidativ skada. 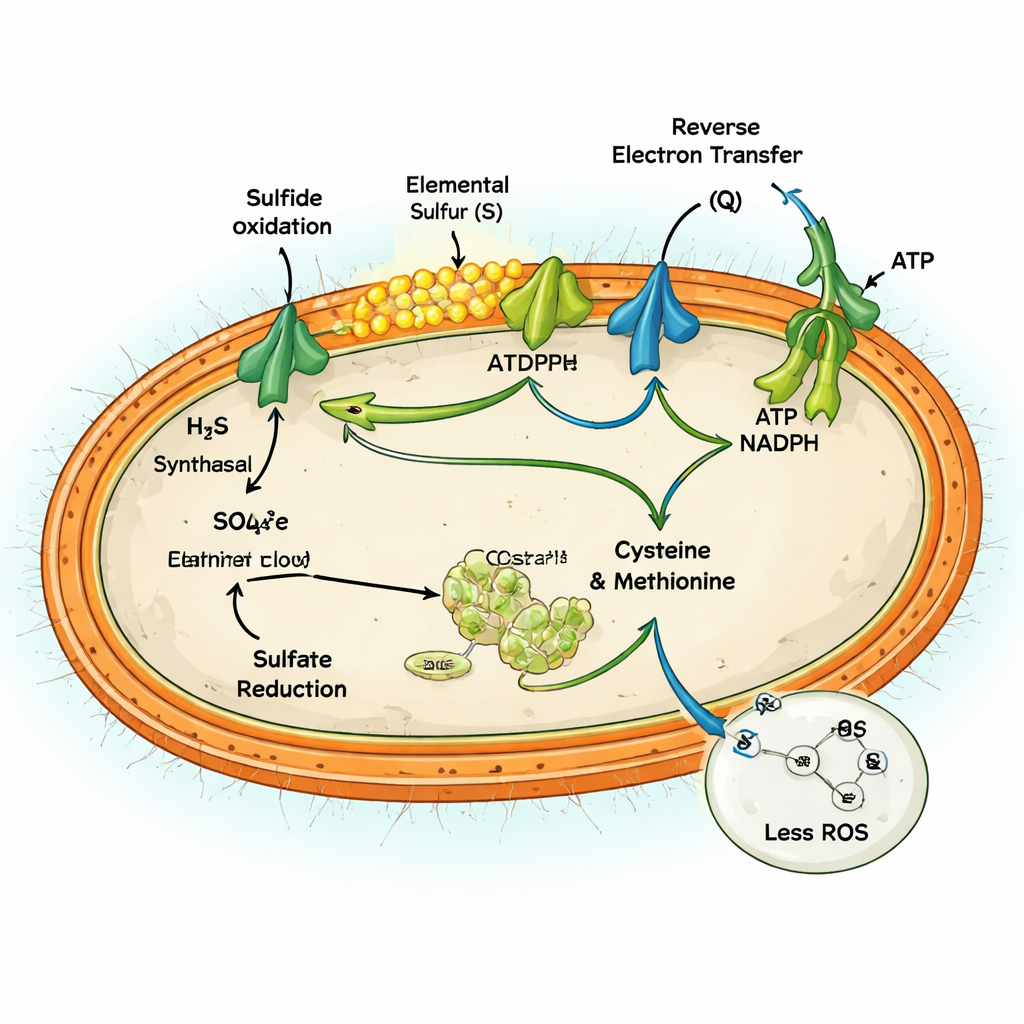
Från giftig gas till användbara produkter
I de senare skedena av reaktoroperationen, när MAG-M116 dominerade, omvandlades nästan allt inkommande svavelväte till fast elementärt svavel istället för till sulfat. Samtidigt upptäckte forskarna ökande nivåer av cystein och metionin i vätskefasen, vilket tyder på att mikroben frigjorde överskotts svavelrika aminosyror till omgivningen. Denna kombination—stabilt elementärt svavel plus värdefulla organiska svavelföreningar—omvandlar vad som tidigare var en farlig förorening till en blandning av återvinningsbara produkter med användning inom jordbruk, material och energisystem.
Vad detta betyder för hälsa och teknik
För en icke-specialist är huvudbudskapet att denna Mycobacterium har löst ett dubbelproblem: den kan sanera höga halter av en giftig gas samtidigt som den håller sin egen interna kemi i balans. Den gör det genom att driva ”push–pull”-svavelreaktioner som normalt hålls åtskilda och använder den till synes slösaktiga cykeln som en inbyggd stötdämpare för överskottselktroner och skadliga syreradikaler. Denna upptäckt antyder inte bara nya sätt att utforma robusta bioreaktorer med lågt pH för avlägsnande av sulfider och sulfat, utan antyder också att närbesläktade mikrober, inklusive sjukdomsframkallande Mycobacterium-arter, kan använda liknande knep för att överleva oxiderande attacker i människokroppen.
Citering: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Nyckelord: svavelcykeln, svavelväte, Mycobacterium, redoxhomeostas, biodesulfurisering