Clear Sky Science · sv
En artificiell cell kapabel till signaltransduktion medierad av ADRB2 för reglering av glykogenolys
Lära små bubblor att kommunicera
Föreställ dig en mikroskopisk tvålbubbla som kan känna av en hormonliknande signal utanför och sedan ”bestämma” sig för att förbränna lagrat bränsle inuti, ungefär som en riktig mänsklig cell. Denna studie bygger just den typen av artificiell cell och visar hur konstgjorda cellimiteringar kan ta emot ett kemiskt meddelande och omvandla det till kontrollerad energi‑relaterad kemi. Sådant arbete för oss närmare smarta läkemedelsbärare, laboratorieframställd vävnad och enkla syntetiska livsformer som kan reagera på sin omgivning.
Bygga en cell från utsidan och in
Riktiga celler lyssnar ständigt till sin omgivning via receptorer i sitt yttre membran. Författarna satte upp sig att kopiera en av dessa naturliga signalvägar med endast renade komponenter och enkla fettbubblor, så kallade jättelika vesikler. De fokuserade på en vanlig människoreceptor, β2‑adrenerga receptorn (ADRB2), som i våra kroppar hjälper till att reglera hjärtfrekvens, lungfunktion och bränsleanvändning. När denna receptor möter ett läkemedel som isoprenalin (ISO) triggar den normalt en intern kedja av händelser som producerar budbärarmolekylen cAMP, vilken i sin tur styr hur celler bryter ner glykogen, kroppens lagrade form av glukos. Att återge hela denna sekvens i en artificiell cell hade tidigare inte uppnåtts.
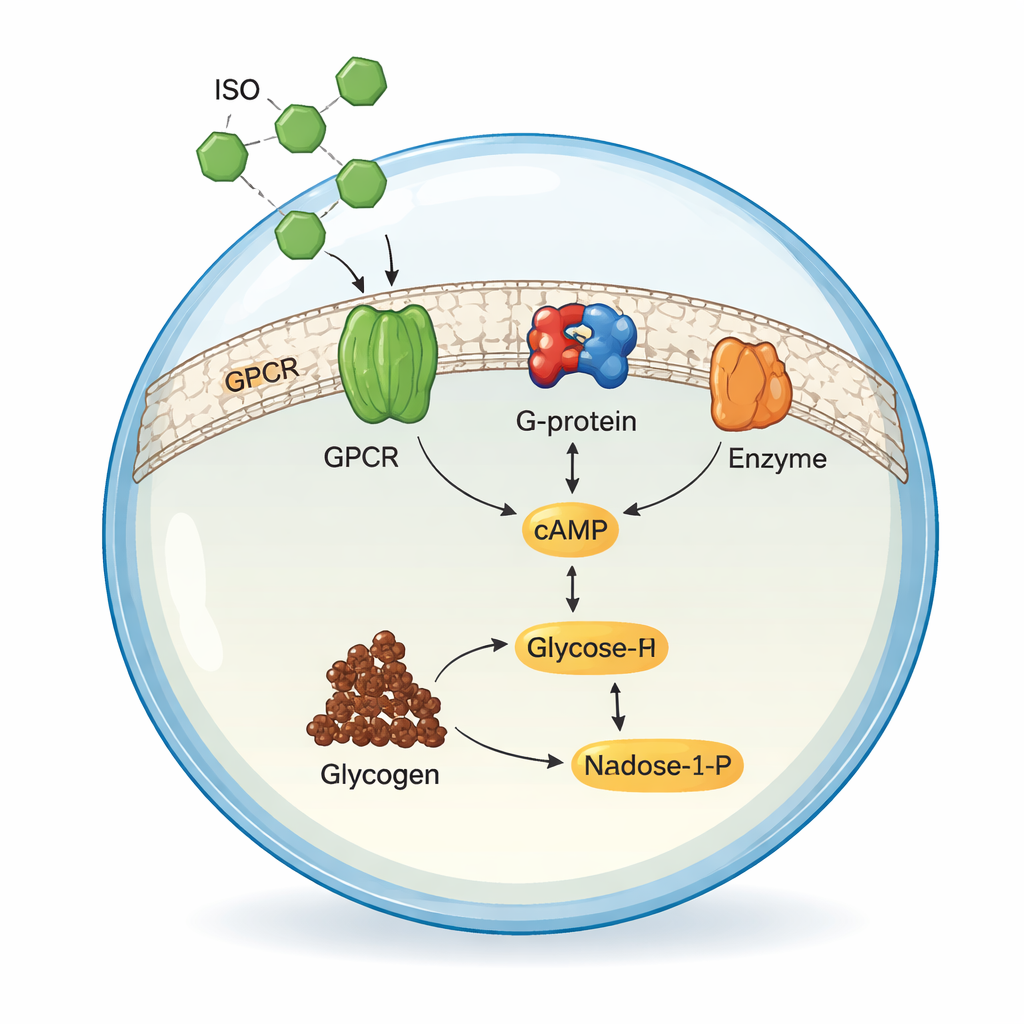
Återskapa den första signalreläet
Teamet återuppbyggde först de tidiga stegen i signalvägen i lösning, utanför något membran. De framställde tre humana proteiner i insektceller: ADRB2, dess partner G‑proteinsunderenhet (Gsα) och ett enzym kallat adenylatcyklas V (ADCY5), som gör cAMP från ATP. När de blandade dessa delar med ISO under noggrant avstämda förhållanden ledde aktivering av den adrenerga receptorn till att ADCY5 omvandlade ATP till cAMP. Genom att mäta cAMP med högpresterande vätskekromatografi optimerade forskarna pH, temperatur och magnesiumnivåer och fann att deras rekonstituerade system fungerade lika effektivt som, eller bättre än, många tidigare preparationer, vilket bekräftade att den centrala signaleringskemin var på plats.
Installera verkliga receptorer i artificiella membran
Därefter infogade författarna de tre proteinerna i membranen hos jättelika unilamellära vesikler—cellstora lipidbubblor som fungerar som chassit för artificiella celler. De fluorescensmärkte ADRB2 och ADCY5 för att verifiera att proteinerna satt i membranet, rörde sig fritt och fanns i stora mängder, med ungefär 1,8 miljoner receptorer per vesikel. Enzymatisk behandling visade att mer än 94 % av dessa receptorer vände åt rätt håll, med sina bindningsställen exponerade mot utsidan. En fluorescerande GTP‑probe bekräftade att ISO‑bindning vid membranet verkligen aktiverade G‑proteiner inuti vesiklerna. Detta innebar att de artificiella cellerna i princip kunde överföra en extern ISO‑signal över sitt membran precis som naturliga celler gör.
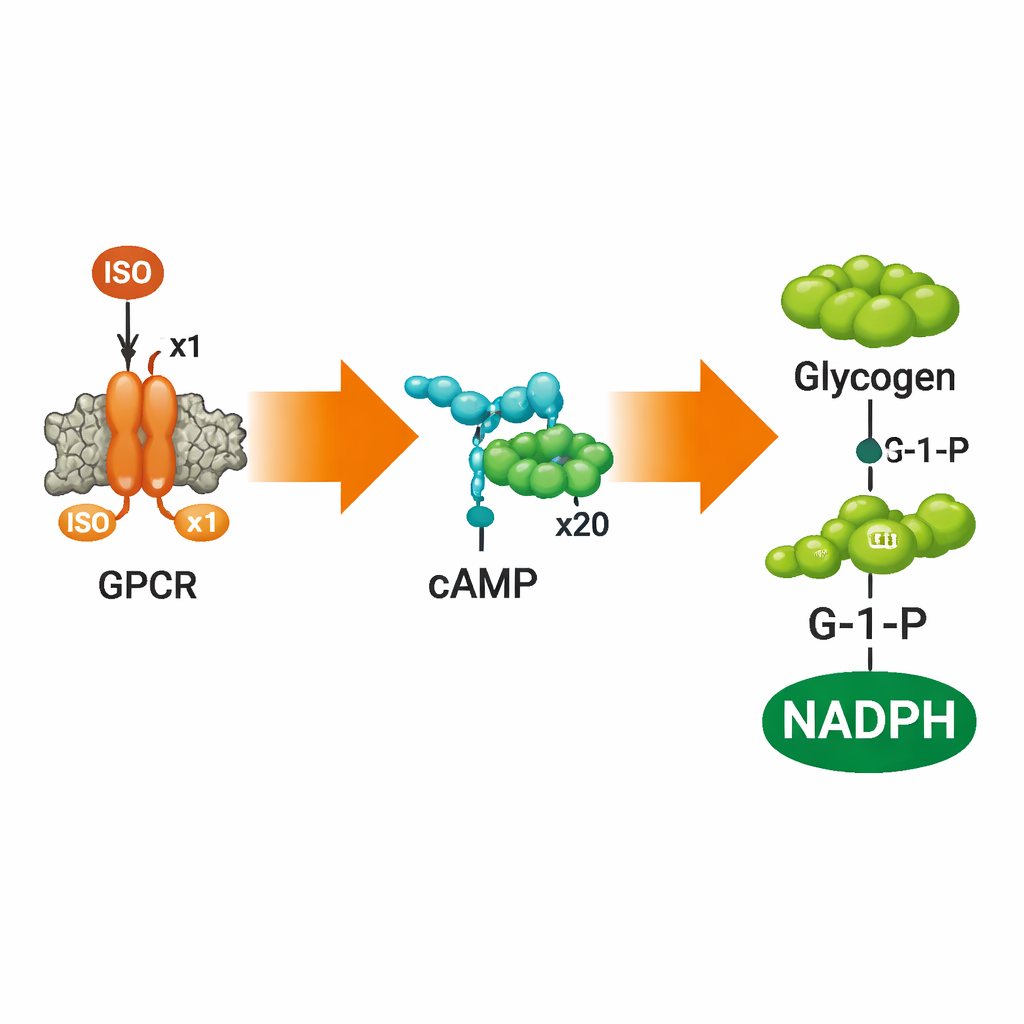
Omvandla signaler till bränsle‑nedbrytning
För att se om dessa syntetiska celler kunde göra något användbart med signalen tillsatte teamet en sensor för cAMP och sedan en hel glykogennedbrytningsväg inuti vesiklerna. Med en FRET‑baserad cAMP‑probe visade de att tillsats av ISO utanför vesiklerna orsakade att cAMP‑nivåerna steg inuti på ett dosberoende sätt för att sedan plana ut när receptorerna mättades, vilket återspeglade klassiskt beteende hos naturliga G‑protein‑kopplade receptorer. Läkemedel som blockerar eller tystar ADRB2—alprenolol och carazolol—stängde av denna respons exakt som förväntat. När författarna också inkapslade fem enzymer som normalt omvandlar glykogen till glukos‑1‑fosfat (G‑1‑P) och sedan till NADPH ledde ISO‑stimulering till mätbar produktion av både G‑1‑P och NADPH inuti de artificiella cellerna, spårat med masspektrometri, kromatografi och fluorescens.
Förstärka en viskning till ett rop
En nyckelobservation är hur starkt den interna responsen förstärktes. En måttlig mängd ISO utanför vesiklerna gav ungefär 22 gånger fler cAMP‑molekyler än det fanns ISO‑molekyler, och denna förstärkning växte vidare nedströms i vägen. När signalen hade drivit glykogennedbrytning och omvandling till 6‑fosfoglukonolakton med tillhörande NADPH översteg den sammanlagda förstärkningen hundrafaldigt. Denna stegvisa förstärkning är ett kännetecken för naturlig hormonsignalering och visar att det artificiella systemet gör mer än att bara detektera ISO—det bearbetar och förstärker budskapet till ett robust metabolt utflöde.
Varför detta spelar roll för framtida syntetiskt liv
För en icke‑specialist kokar de tekniska detaljerna ner till en enkel idé: forskarna har lärt en minimal, människotillverkad cell att lyssna och reagera som en levande cell. En utanförliggande läkemedelsmolekyl binder till en realistisk människoreceptor, en signal förmedlas över ett syntetiskt membran och ett internt enzymnätverk svarar genom att mobilisera lagrad kemisk energi. Att demonstrera denna fulla kedja—från receptoraktivering till kontrollerad metabolism—i ett avskalad artificiellt system är ett stort steg mot autonoma syntetiska celler som kan känna, fatta beslut och agera på användbara sätt, till exempel genom att justera sin egen energiförsörjning eller leverera terapier bara när de upptäcker rätt kemiska signaler.
Citering: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
Nyckelord: artificiella celler, signaltransduktion, GPCR, glykogenolys, syntetisk biologi