Clear Sky Science · sv
Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry
Aktivera potenta läkemedel endast där de behövs
Många moderna läkemedel är extremt potenta, vilket är bra för att bekämpa cancer eller lindra smärta — men riskfyllt för resten av kroppen. Den här studien beskriver en kemi-baserad "på/av‑knapp" som låter forskare parkera läkemedel i en inaktiv, ofarlig form och sedan slå på dem endast på en vald plats och tidpunkt, till exempel inne i en tumör eller i ett litet område som behöver lokalbedövning.
En ny typ av kemisk omkopplare
Forskarna bygger vidare på begreppet "click chemistry", en familj reaktioner som uppskattas för att vara snabba, precisa och säkra att använda i levande system. Klassiska click‑reaktioner fäster permanent ihop två molekyler. Här vänder teamet på logiken: deras click‑reaktion är direkt kopplad till att bryta en bindning och frigöra ett läkemedel eller en signalmolekyl. Huvudaktörerna är en ringformad molekyl kallad cyklooktyn och en liten partner kallad mono‑alkyl‑hydroxylamin. När dessa två möts binder de snabbt ihop och omarrangerar sig så att ett kopplat "last" (payload) klipps loss. Genom att fästa olika läkemedel eller fluorescerande färgämnen som payload kan samma grundreaktion återanvändas för många ändamål. 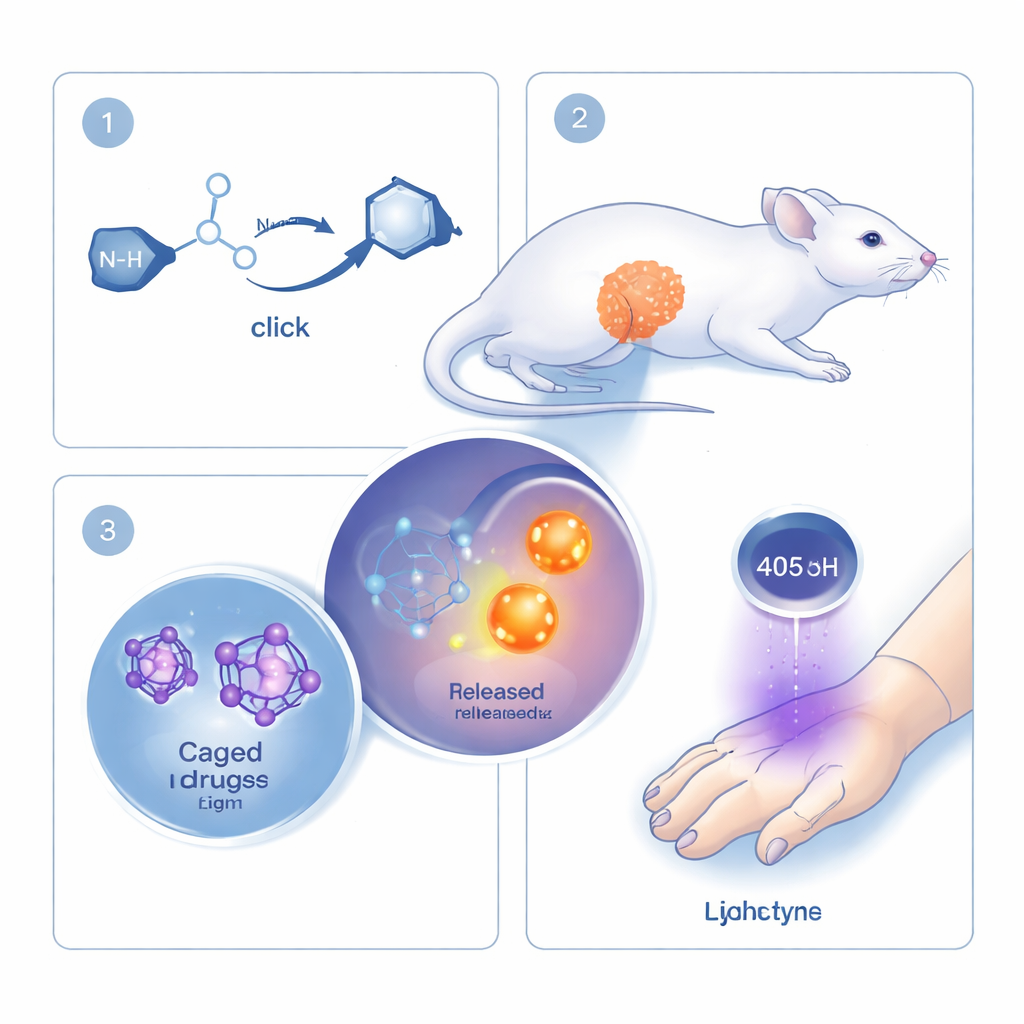
Snabb, ren frigöring inne i och utanför celler
För att säkerställa att denna omkopplare skulle vara praktisk mätte teamet hur snabbt reaktionen fortskrider och hur fullständigt den frigör den fästa lasten. De fann att noggrant utvalda mono‑alkyl‑hydroxylaminer reagerar betydligt snabbare än enkel hydroxylamin och når nära‑komplett konversion inom minuter till timmar, beroende på strukturen. Viktigt är att de kemiska stegen som faktiskt befriar lasten är så snabba och selektiva att nästan hela den fästa molekylen frigörs, med nästan inga restprodukter. Författarna testade en rad olika laster, inklusive fluorescerande färgämnen och till och med en fluoridjon, och visade att systemet kan bryta flera vanliga bindningstyper som används i läkemedelsdesign, såsom karbamater och etrar.
Tända celler och aktivera cancerläkemedel på begäran
Nästa steg för forskarna var att gå in i levande celler. De gömde först starkt fluorescerande färgämnen bakom den kemiska omkopplaren och tillsatte dessa "inkapslade" prober till cancerceller. På egen hand förblev proberna mörka, vilket visade att cellerna inte aktiverade dem av misstag. När mono‑alkyl‑hydroxylamin‑partnern tillsattes frigjordes färgämnena och cellerna lystes upp i blått, grönt eller nära‑infrarött, vilket bekräftade att reaktionen fungerar pålitligt i en biologisk miljö. De tillämpade sedan samma idé på doksorubicin, ett brett använt cytostatikum. I sin inkapslade form var doksorubicin‑prodrigen mycket mindre giftig för cellerna. Men när click‑partnern var närvarande frigjordes det aktiva läkemedlet effektivt och återställde dess förmåga att döda cancerceller nästan lika starkt som fri doksorubicin.
Bygga intelligenta avtryckare för plats och tid
En begränsning med många befintliga click‑baserade system är att de reaktiva komponenterna alltid är "på", vilket gör det svårt att kontrollera exakt var och när de aktiveras. För att lösa detta blockerade teamet tillfälligt reaktiviteten hos mono‑alkyl‑hydroxylamin med små skyddshättor som endast tas bort av specifika triggers. De skapade varianter som svarar på höga nivåer av glutation (en liten molekyl som är riklig i många tumörer), på enzymer och på blixtar av violett ljus. I celler och i tumör‑bärande möss förblev den glutation‑känsliga versionen tyst under normala förhållanden men slog på i tumörens kemiskt reducerande miljö, frigjorde fluorescerande färgämnen eller aktiverade doksorubicin‑prodrigen precis där cancern växte. Möss behandlade med kombinationen prodrug plus trigger visade starkare tumörminskning än de som fick standarddoksorubicin, samtidigt som exponeringen av känsliga organ som hjärtat minskade.
Fjärrstyrd lokalbedövning med ljus
För att Visa tidkontrollen designade författarna en andra tillämpning: ljustyrd lokalbedövning. De fäste smärtstillande läkemedlet tetrakain till sin cyklooktyn‑stomme, vilket gjorde det inaktivt, och blandade denna prodrug med en ljuskänslig version av hydroxylamin i ett temperaturkänsligt gel. Injicerat i en råttas tass gjorde blandningen ingenting tills huden belystes med 405‑nanometerljus. Belysning utlöste click‑release‑reaktionen, frigjorde tetrakain och gav domning jämförbar med direkt injektion av tetrakain. Genom att ändra hur länge och hur starkt ljuset sken kunde forskarna ställa in hur länge nervblocket varade, och de kunde till och med utlösa upprepade vågor av anestesi från en enda injektion. 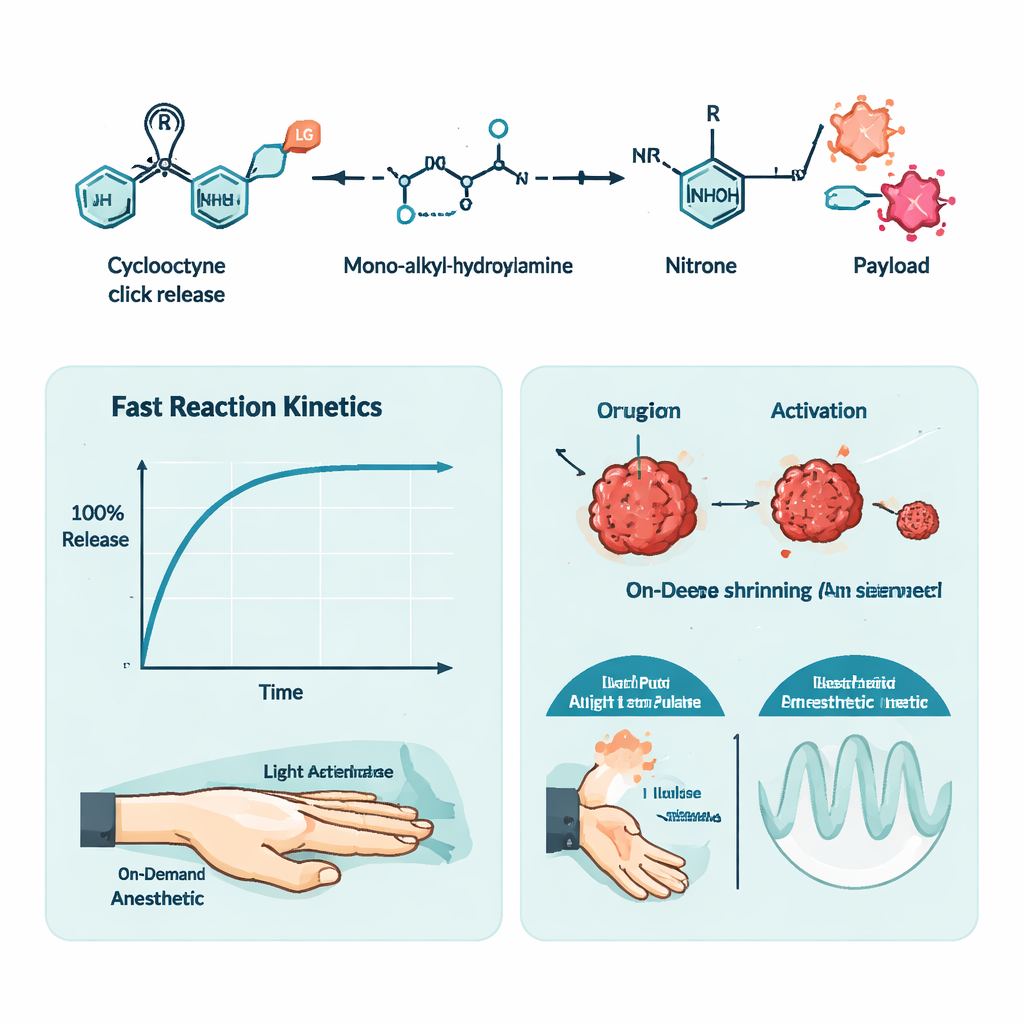
Vad detta kan betyda för framtida behandlingar
För icke‑specialister är huvudbudskapet att detta arbete erbjuder en flexibel kemisk fjärrkontroll för läkemedel: läkemedel kan levereras i en säker, tyst form och sedan aktiveras endast på rätt plats och i rätt ögonblick, med signaler som kommer från kroppen själv eller från en extern ljuskälla. Även om fler tester krävs innan klinisk användning kan denna strategi så småningom göra cancerbehandlingar mer riktade och mindre toxiska, möjliggöra anpassningsbar smärtkontroll efter operation och stödja ett spektrum av andra terapier som gynnas av precis spatiotemporal kontroll.
Citering: Xu, X., Tong, X., Shi, Y. et al. Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry. Nat Commun 17, 1794 (2026). https://doi.org/10.1038/s41467-026-68502-4
Nyckelord: click chemistry, targeted drug delivery, prodrugs, tumor microenvironment, photo-controlled anesthesia