Clear Sky Science · sv
Att rikta in sig på UFL1–AKT-kaskaden dämpar trippelnegativ bröstcancerprogression
Varför denna forskning är viktig
Trippelnegativ bröstcancer (TNBC) är en av de mest dödliga formerna av bröstcancer eftersom den saknar de hormon- och tillväxtfaktorsignaler som många moderna läkemedel riktar sig mot. Patienter får ofta enbart traditionell cytostatikabehandling, vilken kan sluta fungera när tumörer utvecklar resistens. Denna studie avslöjar en tidigare dold molekylär "motor" som hjälper TNBC-celler att växa och motstå cytostatika, och föreslår en ny typ av läkemedel som direkt stör denna motor.
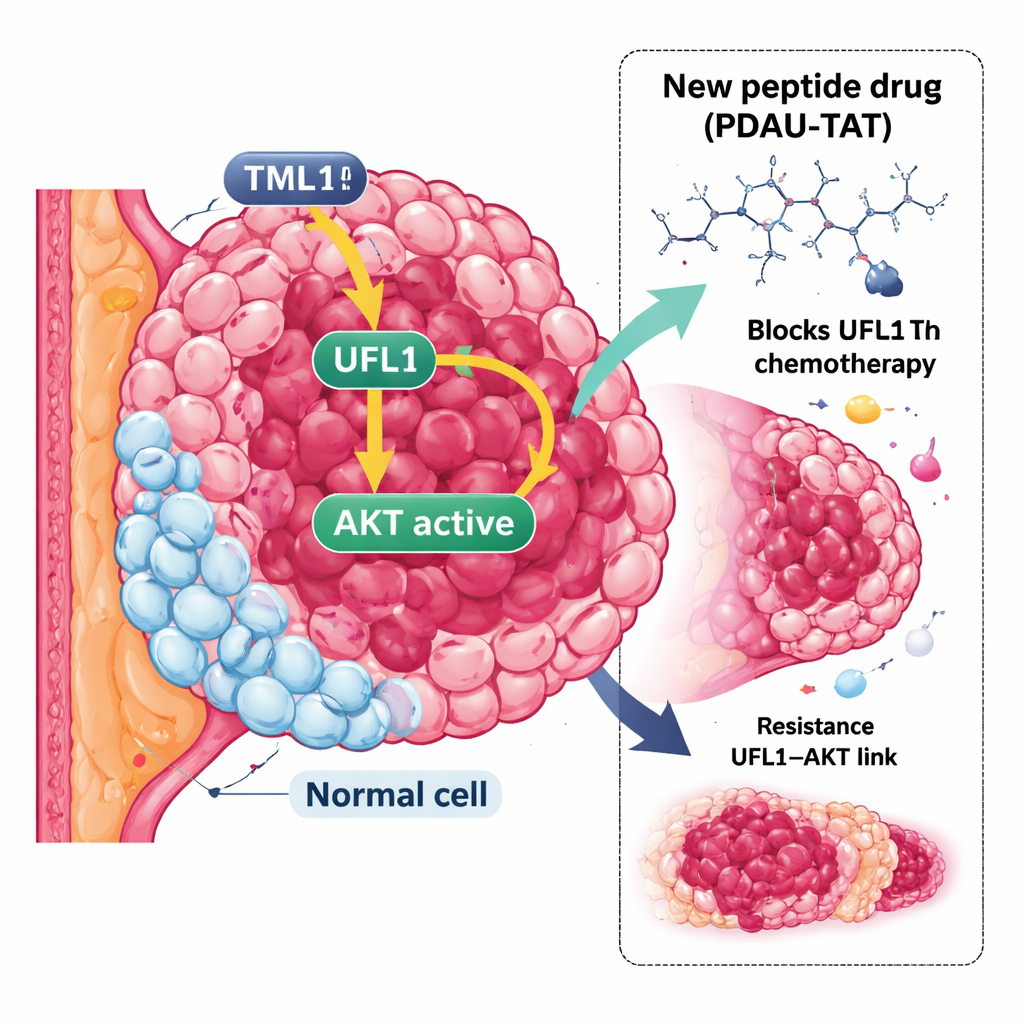
En seglivad form av bröstcancer
TNBC definieras av frånvaron av tre vanliga markörer: östrogenreceptorn, progesteronreceptorn och tillväxtreceptorn HER2. Utan dessa markörer gäller många effektiva riktade behandlingar inte. Standardläkemedel som cisplatin och doksorubicin används istället, men TNBC-tumörer blir ofta resistenta eller anpassar sig snabbt till dessa behandlingar och har högre sannolikhet att sprida sig. Detta skapar ett akut behov av nya strategier som går bortom de vanliga målen och söker andra svagheter i tumörens kontrollsystem.
En lite känd protein med stor påverkan
Forskarna fokuserade på UFL1, ett protein som fäster en liten märkning, kallad UFM1, på andra proteiner i en process som kallas UFMylering. Detta märkessystem har bara nyligen upptäckts och dess roll i cancer har varit oklar och ibland motsägelsefull. Genom att analysera patientdata och tumörprover visade teamet att UFL1 är markant förhöjt i TNBC jämfört med normalt bröstvävnad. När de minskade UFL1-nivåerna i TNBC-cellinjer och i musmodeller med tumörer delade cancercellerna sig långsammare och blev betydligt mer känsliga för cytostatika, vilket tyder på att UFL1 spelar en tumörfrämjande roll i detta sammanhang.
Kopplingen mellan UFL1 och en huvudvakt för tillväxt
Vid djupare undersökning upptäckte forskarna att UFL1 binder direkt till AKT, ett centralt signalprotein som driver celltillväxt, överlevnad och ämnesomsättning och som ofta är överaktivt i cancer. I TNBC är AKT ofta överaktivt även när de vanliga upstream-mutationerna saknas. Teamet fann att UFL1 kemiskt märker AKT på tre specifika positioner, vilket gör det lättare för AKT att aktiveras av sina aktiverande partners samtidigt som det skyddar AKT från enzymer som normalt skulle stänga av det. Celler utan UFL1 eller som uttryckte en konstruerad form av AKT som inte kan ta emot dessa märkningar visade mycket lägre AKT-aktivitet, långsammare tillväxt och större sårbarhet för cytostatika både i cellkulturer och i djurmodeller.
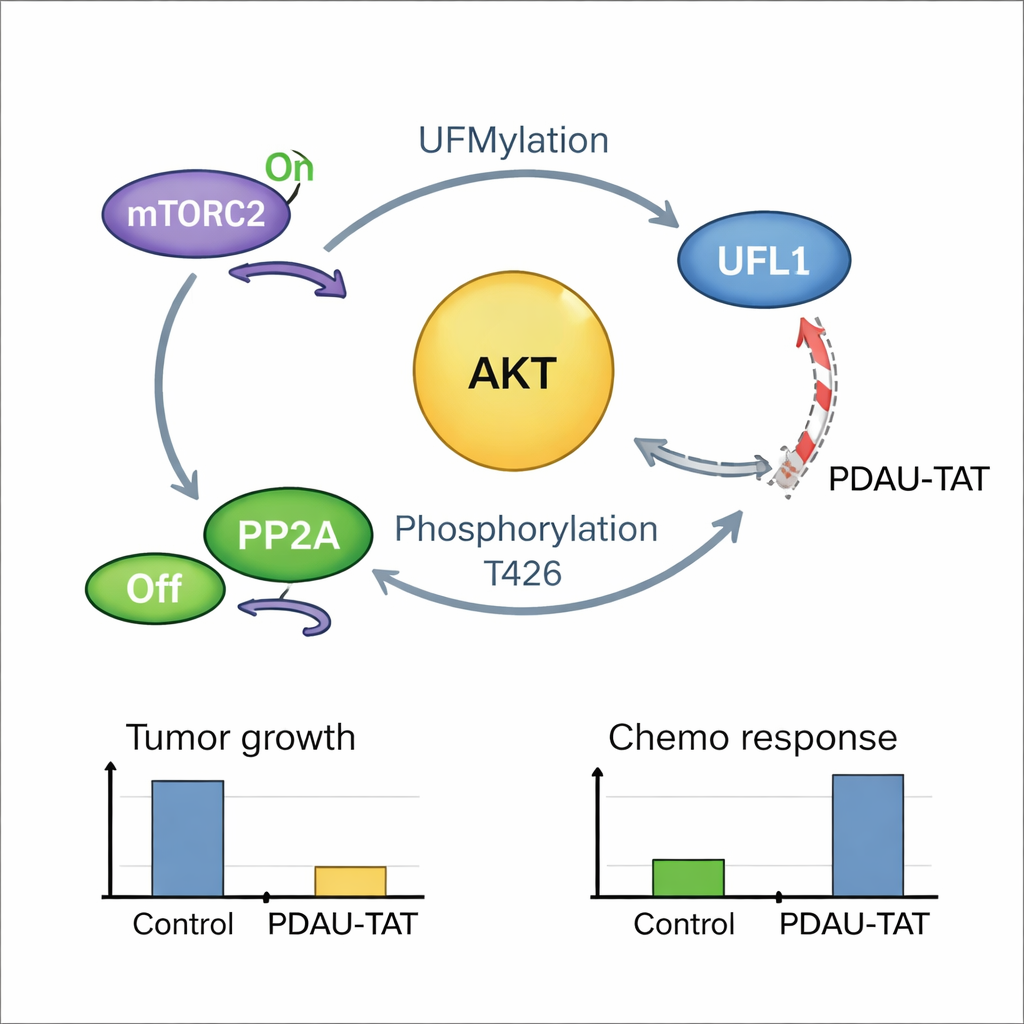
En självförstärkande cancerloop och ett sätt att bryta den
Berättelsen visade sig vara ännu tätare kopplad: när AKT väl är aktiverat ger det återkoppling och modifierar UFL1 på en enda avgörande plats, vilket ökar UFL1:s märkaktivitet på AKT och andra mål. Detta skapar en positiv återkopplingsloop där UFL1 aktiverar AKT, och aktivt AKT i sin tur förstärker UFL1. Patientprover visade att höga nivåer av modifierat UFL1 starkt korrelerar med höga nivåer av aktivt AKT, vilket stödjer förekomsten av denna loop i mänsklig sjukdom. För att utnyttja denna sårbarhet designade teamet ett kort, cellpenetrerande peptid, kallat PDAU-TAT, som efterliknar en liten region av UFL1 och kilas in mellan UFL1 och AKT. Detta peptid stör deras interaktion, minskar AKT-aktiveringen, bromsar tumörtillväxt och gör TNBC-celler och patienthärledda tumörer mer responsiva på cytostatika, utan tydliga skador på viktiga organ i möss.
Vad detta kan innebära för patienter
Enkelt uttryckt har forskarna avslöjat en dold kopplingsschema inne i TNBC-celler: UFL1 och AKT är fastlåsta i en självförstärkande loop som håller tillväxtsignaler i "på"-läge och hjälper tumörer att motstå behandling. Genom att skapa ett litet peptid som glider in i denna loop och kopplar bort UFL1 från AKT visar de en tänkbar ny metod för att försvaga TNBC-tumörer samtidigt som normala celler, som tenderar att ha lägre UFL1-nivåer, skonas. Även om detta arbete fortfarande är i preklinisk fas pekar det mot en ny klass av riktade terapier som inte angriper de vanliga receptorerna utan i stället de protein–protein-interaktioner som driver några av de mest aggressiva bröstcancerformerna.
Citering: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Nyckelord: trippelnegativ bröstcancer, AKT-signalering, UFMylering, UFL1, peptidbehandling mot cancer