Clear Sky Science · sv
Den positiva återkopplingsloopen UFL1–AKT främjar bröstcancerprogression genom att öka lipidsyntesen
Varför cancerceller bryr sig så mycket om fett
Bröstcancerceller, liksom alla snabbväxande celler, behöver en stadig tillförsel av byggstenar för att skapa nya membran och signalmolekyler. Fett, eller lipider, är en central del av den tillgången. Denna studie avslöjar hur ett litet känt proteinsystem skjuter cancercellerna in i ett "fettsyntes‑övervarv" som hjälper tumörer att växa och undvika behandling. Att förstå denna dolda bränslerelation kan öppna nya vägar för att bromsa eller svälta ut bröstcancer.
En dold proteintagg med stora konsekvenser
Våra celler justerar ständigt sina proteiners beteende med små kemiska taggar. En sådan tagg, kallad UFM1, läggs på av ett enzym som heter UFL1. UFM1‑märkning (UFMylering) har kopplats till DNA‑reparation och stressreaktioner, men dess roll i cancer var otydlig. Författarna visar att UFL1 är mycket mer aktivt i mänskliga brösttumörer än i normalt bröstvävnad, över alla stora subtyper. Patienter vars tumörer har högre UFL1‑nivåer tenderar att få sämre överlevnad. När forskarna minskade UFL1 i bröstcancerceller eller i tumörer hos möss, saktade cancertillväxten ner, celldelningen minskade och celldöd ökade, vilket tyder på att UFL1 beter sig som en cancerfrämjande faktor.
Hur en signalcentral vrids över till fettproduktion
För att förstå hur UFL1 hjälper tumörer sökte teamet efter dess molekylära partner och fann ett nyckelprotein för signalreglering kallat AKT1. AKT1 är en central omkopplare som instruerar celler att växa och att producera nya lipider. Studien visar att UFL1 fysiskt binder till AKT1 och pryder det med UFM1‑taggar på flera specifika platser. Denna märkning ändrar AKT1:s form och lossar på en intern "broms" som normalt håller det tyst. Det hjälper också AKT1 att förflytta sig till ett membrankompartiment inne i cellen, det endoplasmatiska retikulumet, där andra enzymer kan aktivera det fullt ut genom fosforylering. Utan UFM1‑taggar på dessa platser är AKT1 mycket svårare att aktivera.
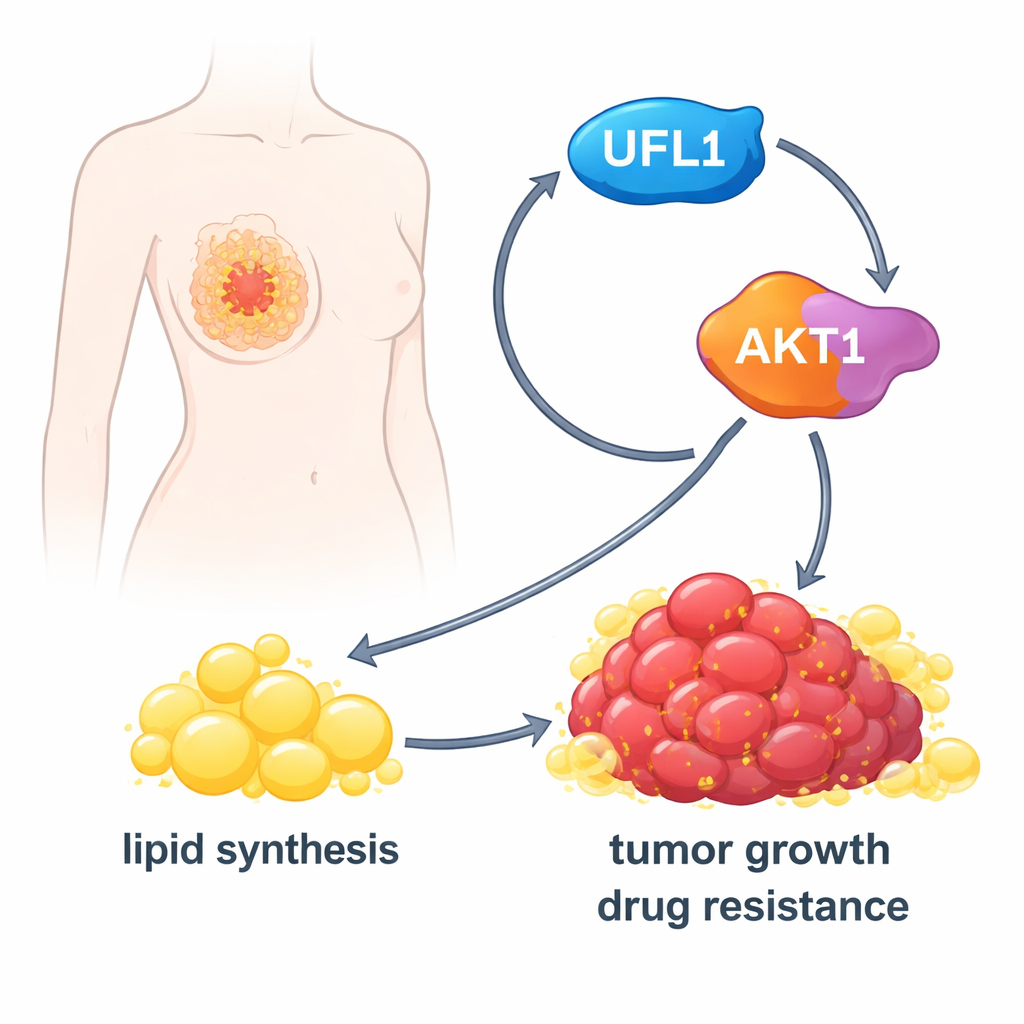
Att slå på cancerns fettfabrik
När AKT1 väl är aktiverat driver det cellerna att öka sin fettproduktion. Det höjer aktiviteten hos ett nyckelmetaboliskt enzym, ACLY, och ökar nivåerna av huvudregulatorer som SREBP1 som slår på många fettbildande gener. I bröstcancerceller odlade i labbet fick UFL1 cellerna att samla på sig fler fettdroppar, fria fettsyror och kolesterol. Att ta bort UFL1 minskade kraftigt dessa lipidförråd, både i petriskålar och i tumörer odlade i möss. Tillskott av extra fettsyror utifrån kunde till stor del återställa tillväxten hos UFL1‑defekta cancerceller, vilket indikerar att UFL1:s huvudsakliga effekt är att säkra tillräckligt med lipider för att upprätthålla tumörexpansion.
En självförstärkande slinga som driver tumörtillväxt
Överraskande nog går relationen mellan UFL1 och AKT1 åt båda håll. Forskarna upptäckte att när AKT1 är aktiv så sätter det i sin tur en fosfatgrupp på UFL1 vid en särskild plats. Denna modifiering förstärker ytterligare UFL1:s förmåga att märka AKT1 med UFM1, vilket skapar en positiv återkopplingsslinga: UFL1 aktiverar AKT1, och AKT1 aktiverar UFL1. Mutation av antingen UFM1‑märkningsställena på AKT1 eller fosforyleringsstället på UFL1 bryter denna slinga. I möss växte tumörer med dessa mutanta varianter dåligt, innehöll färre lipider och uppvisade fler döende celler. I prover från patienter med trippelnegativ bröstcancer tenderade högre nivåer av aktiverat UFL1 och aktiverat AKT1 att förekomma tillsammans, vilket understryker att denna slinga är verksam i verkliga tumörer.
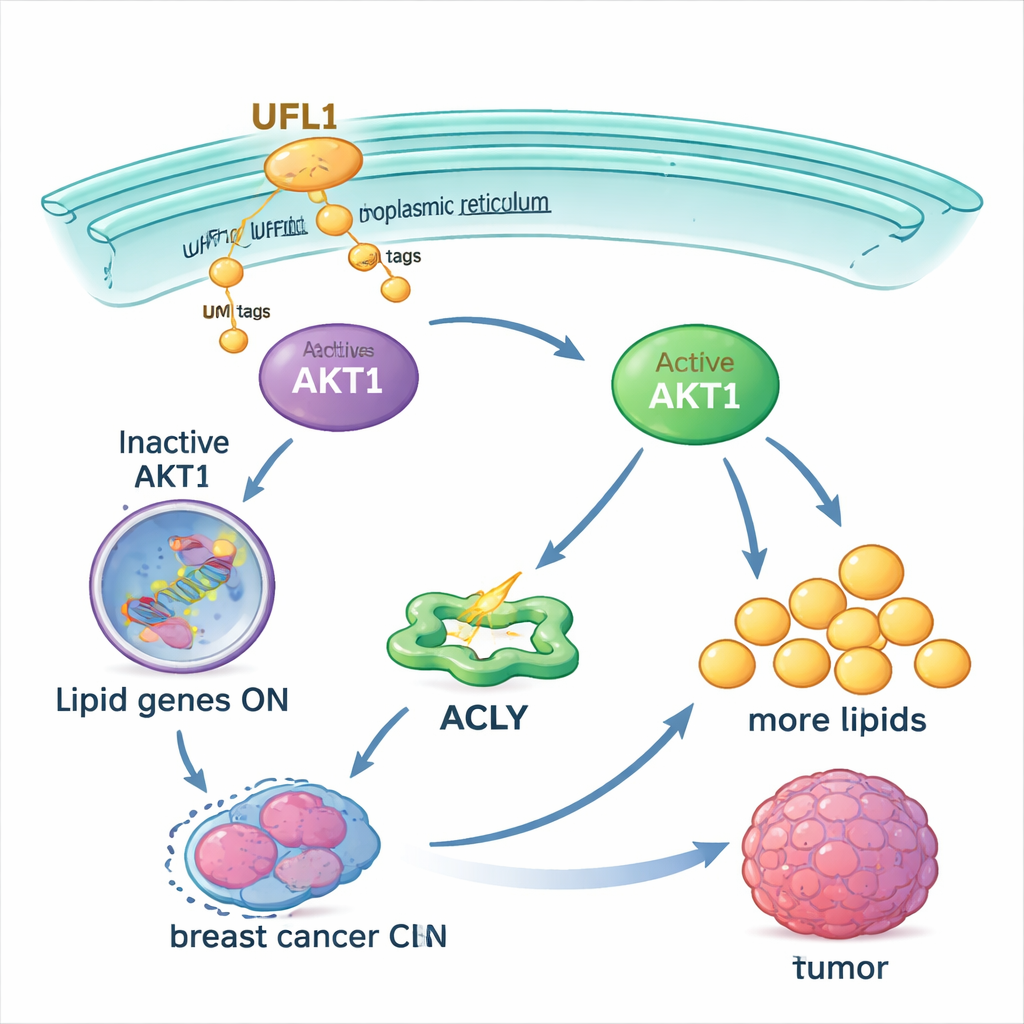
Svagare slinga hjälper behandlingar att fungera
Eftersom många läkemedelsprövningar redan riktar in sig mot AKT, testade författarna om blockering av UFMylering kunde göra dessa behandlingar mer effektiva. I bröstcancerceller sänkte både en småmolekylär hämmare av UFMylering och en AKT‑hämmare var och en för sig AKT1‑aktiviteten och lipidsamling, men att använda dem tillsammans fungerade mycket bättre än någon av dem ensam. Kombinationen bromsade också tumörtillväxt och minskade fettinnehållet i mösstumörer utan märkbar viktminskning hos djuren. Blockering av UFMylering gjorde vidare cancerceller mer känsliga för standardkemoterapier som cisplatin och etoposid, vilka ofta misslyckas när AKT är högt aktivt.
Vad detta betyder för patienter
För en lekmansläsare visar studien att vissa bröstcancerformer kopplar ihop sig med en självförstärkande slinga som matar både deras tillväxt och deras fetttillgång. UFL1 och AKT1 fungerar tillsammans som två ihållande pedaler: den ena märker, den andra signalerar, och tillsammans driver de lipidsyntes och tumörexpansion. Genom att hitta läkemedel som stör denna slinga — antingen genom att blockera UFMylering, AKT1 eller deras interaktion — kan framtida terapier kanske sakta ner tumörtillväxt och göra befintliga behandlingar mer effektiva, särskilt vid aggressiva bröstcancerformer.
Citering: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Nyckelord: bröstcancer, lipidmetabolism, AKT‑signalering, UFMylering, målinriktad terapi