Clear Sky Science · sv
In situ självmonterande cellreservoarhydrogel för styrning av flerstegs radioimmunterapi
Att förvandla strålning till ett smartare cancervapen
Strålbehandling är en av de mest använda behandlingarna mot cancer, men tumörer överlever ofta genom att gömma sig för immunsystemet och genom att växa i syrefattiga (hypoxiska) förhållanden som minskar strålningens effekt. Denna studie beskriver en injicerbar ”smart” hydrogel som bildas direkt inne i en tumör och fungerar som ett litet läkemedelsfabrikat och en syrgengenerator. Genom att förse tumören både med strålning och noggrant tidpunktsstyrda immunstimulerande signaler syftar systemet till att göra en svårbehandlad cancer igenkännbar och förintbar för kroppens egna försvar.
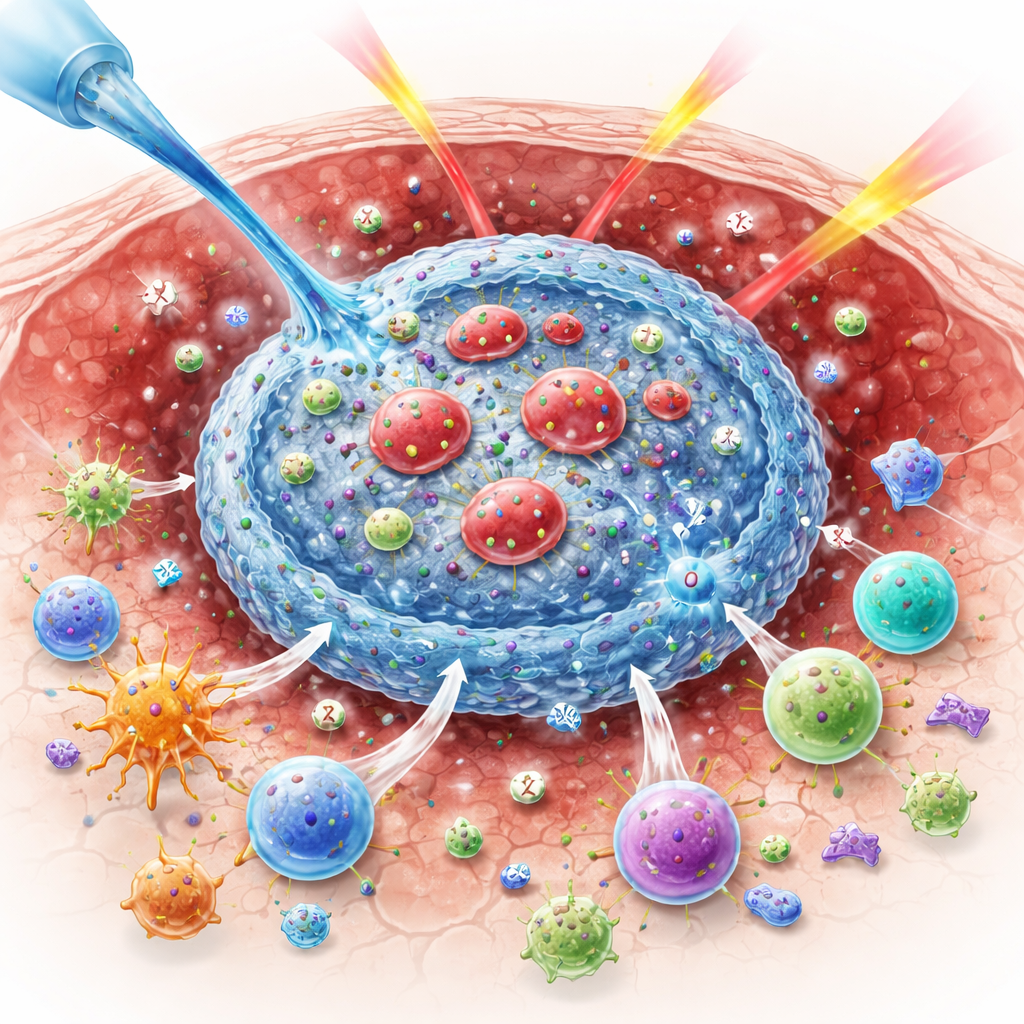
Varför syre spelar roll för att slå tumörer
Strålning dödar cancerceller delvis genom att skapa mycket reaktiva syremolekyler som bryter ner DNA. När tumörer lider brist på syre är denna kemi mindre effektiv, så fler cancerceller överlever. Samtidigt sänder strålning blandade signaler till immunsystemet. Den kan exponera tumörproteiner som markerar cancern som farlig, men den kan också förstärka ”bromsar” på immunceller, till exempel kontrollproteinet CTLA-4, och gynna regulatoriska T‑celler som dämpar angrepp. Dessa motstridiga effekter hjälper förklara varför kombinationen av strålning och immunläkemedel inte alltid fungerat lika bra hos patienter som i musmodeller.
En levande gel byggd inne i tumören
Forskarna designade ett material som självmonterar sig endast i den sura miljön i en tumör. Det består av tre huvudkomponenter: ett naturligt sockerbaserat polymer kallat alginat, ett oorganiskt pulver kallat bariumperoxid, och röda blodkroppar som varsamt modifierats för att bära två immundroger. När blandningen injiceras i en tumör triggar de sura förhållandena att bariumperoxiden sönderfaller och frigör bariumjoner och väteperoxid. Bariumjonerna korsbinder omedelbart alginatet till en mjuk hydrogel, fångar de modifierade röda blodkropparna på plats och förhindrar att läkemedlen sköljs bort. Samtidigt omvandlar enzymer som naturligt finns i de röda blodkropparna väteperoxiden till syre, vilket hjälper till att lindra tumörhypoxi och förbereda tumören för mer effektiv strålning.
Tidsinställd frisättning av dubbla immunsignaler
Systemets verkliga kraft ligger i hur det sprider ut frisättningen av två immungivare: en antikropp som blockerar CTLA-4 och en cytokin kallad interleukin‑12 (IL‑12). Antikroppen är innesluten i de röda blodkropparna, medan IL‑12 är förankrad på deras yta. När syre genereras öppnas porer i de röda blodkropparnas membran, vilket gör att CTLA‑4‑blockerande antikroppen kan släppas snabbt. Denna tidiga frisättning lättar immunsuppression, uppmuntrar dendritiska celler att föra tumörantigener till närliggande lymfknutor och hjälper till att aktivera tumörspecifika T‑celler. IL‑12, däremot, sipprar ut långsamt i takt med att hydrogels struktur gradvis luckras upp. Denna senare signal driver T‑celler och natural killer‑celler att producera interferon‑gamma, främjar fortsatt rekrytering av mördarceller till tumören och förstärker en positiv återkopplingsslinga mellan immunsentineller och effektorceller.
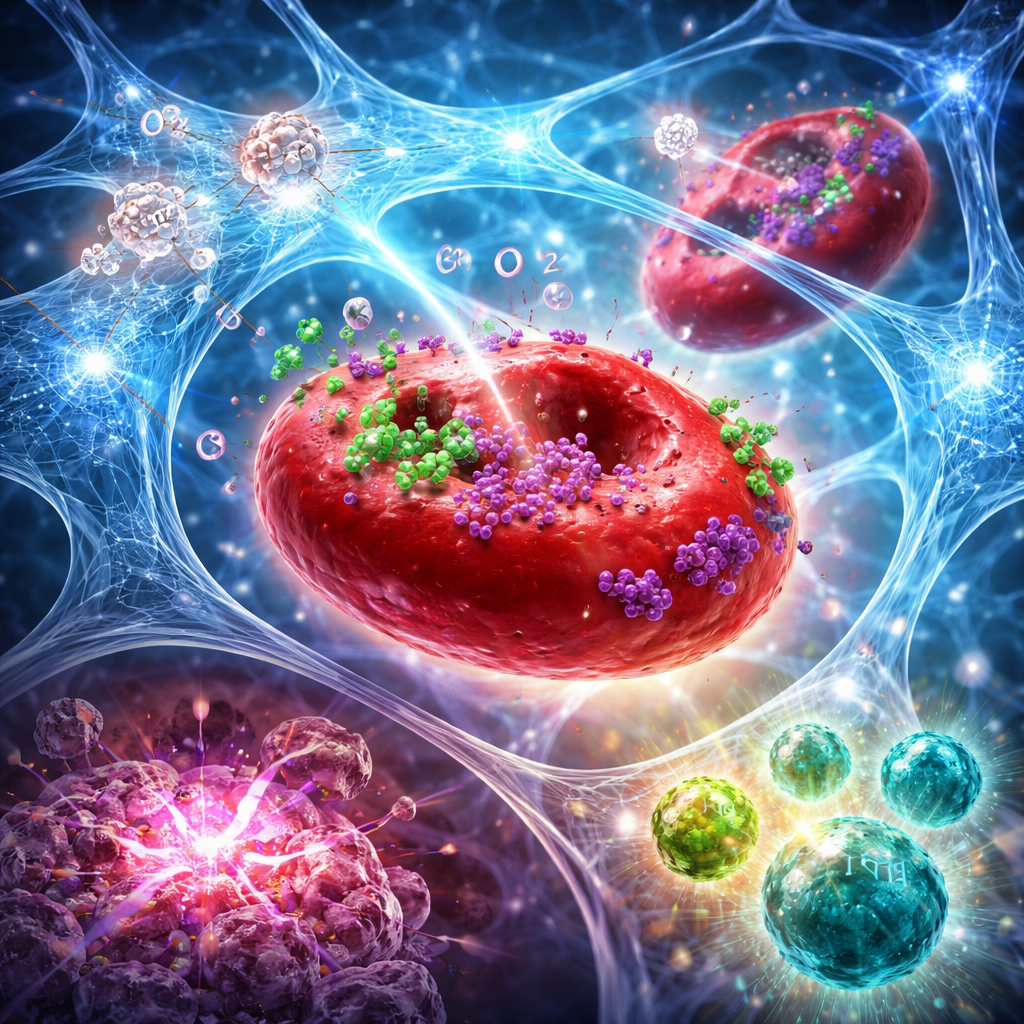
Från lokal injektion till systemiskt immunangrepp
I musmodeller av aggressiv bröst‑ och bukspottkörtelcancer gjorde kombinationen av denna hydrogel och fokuserad strålning mer än att bara krympa den behandlade tumören. Den sammansatta metoden ökade syrenivåerna i tumörerna i flera dagar, förstärkte strålningsinducerad DNA‑skada och utlöste en starkare form av celldöd som naturligt signalerar tumörer för immunigenkänning. Flödescytometri och vävnadsfärgning visade en tydlig förskjutning i tumörmikromiljön: fler cytotoxiska CD8‑T‑celler och natural killer‑celler, färre regulatoriska T‑celler och en högre andel effektor‑ kontra suppressorceller. Specialiserade dendritiska celler i lymfknutor ökade också, vilket indikerar bättre antigenpresentation. Många möss upplevde fullständig tumörregression, och några var skyddade mot tumöråterkomst när cancerceller återintroducerades veckor senare, vilket tyder på bildandet av varaktigt immunminne.
Säkerhet, praktik och framtida riktningar
Eftersom gelen bildas lokalt och håller kvar sin last läcker endast små mängder IL‑12 och anti‑CTLA‑4 ut i blodomloppet, vilket minskar risken för allvarliga biverkningar som cytokinstormar eller organskador som tidigare begränsat användningen av dessa ämnen. Byggstenarna—alginat, röda blodkroppar och bariumperoxid—är relativt billiga och skalbara, vilket väcker förhoppningar om att strategin kan anpassas till olika cancerformer. Även om utmaningar återstår inom tillverkning, kvalitetskontroll och leverans av gelen till djupa eller spridda tumörer, visar arbetet ett lovande sätt att synkronisera strålning med noggrant tidpunktstyrd immunaktivering och förvandla en fysisk cancerbehandling till en kraftfull trigger för hela kroppens antitumörimmunitet.
Vad detta kan betyda för patienter
I vardagliga termer antyder denna forskning att istället för att ge strålning och immunläkemedel separat och hoppas att de samarbetar, kan vi paketera dem i ett smart material som sitter inne i tumören, tillverkar sitt eget syre och frigör immunsignaler i en noga koreograferad ordning. I djur gjorde detta tillvägagångssätt inte bara strålningen mer dödlig för cancerceller utan också tränade immunsystemet att känna igen och minnas tumören, vilket hjälpte till att förhindra att den kom tillbaka. Om liknande resultat kan uppnås hos människor kan sådana hydrogel en dag förvandla svårbehandlade tumörer till mål som kroppens egna försvar tillförlitligt kan hitta och förstöra.
Citering: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
Nyckelord: radioimmunterapi, hydrogel, cancerimmunterapi, tumörmikromiljö, strålbehandling