Clear Sky Science · sv
Kontinuerligt ställbar multistabilitet i DNA-replikationsnätverk
Från enkla strömbrytare till många möjliga tillstånd
Biologiska system, från delande celler till utvecklande embryon, fungerar sällan som enkla ljusbrytare som bara är på eller av. Istället behåller de ofta många långvariga tillstånd, ungefär som en dimmer som kan stanna i otaliga positioner. Denna artikel beskriver ett DNA‑baserat kemiskt nätverk som beter sig mer som en sådan dimmer: det kan stabilt bibehålla inte bara några få distinkta tillstånd utan i princip vilken sammansättning som helst längs ett kontinuerligt spektrum. Den förmågan kan bli en kraftfull grund för framtida smarta material, molekylära minnen och biokemiska datorer som bearbetar analog, inte bara digital, information.
Varför flera stabila tillstånd spelar roll
Många cellulära beslut—om en stamcell mognar, en cell självdödar eller ett gen-nätverk minns en tidigare signal—beroende av “multistabilitet”, förmågan att vila i mer än ett stabilt aktivitetsmönster under samma förhållanden. Traditionella syntetiska versioner av sådana system har byggts av genkretsar, enzymer eller DNA-strängar som aktiverar eller inhiberar varandra. Dessa konstruktioner ger vanligtvis ett fåtal diskreta utfall, som klassiska bistabila brytare med två långlivade tillstånd. Att skala upp den idén är svårt: ett N‑tillstånds system kan kräva i storleksordningen N×(N−1) noggrant avstämda hämmande länkar, och systemet hoppar fortfarande bara mellan ett litet antal fasta punkter snarare än en jämn kontinuitet av möjligheter.
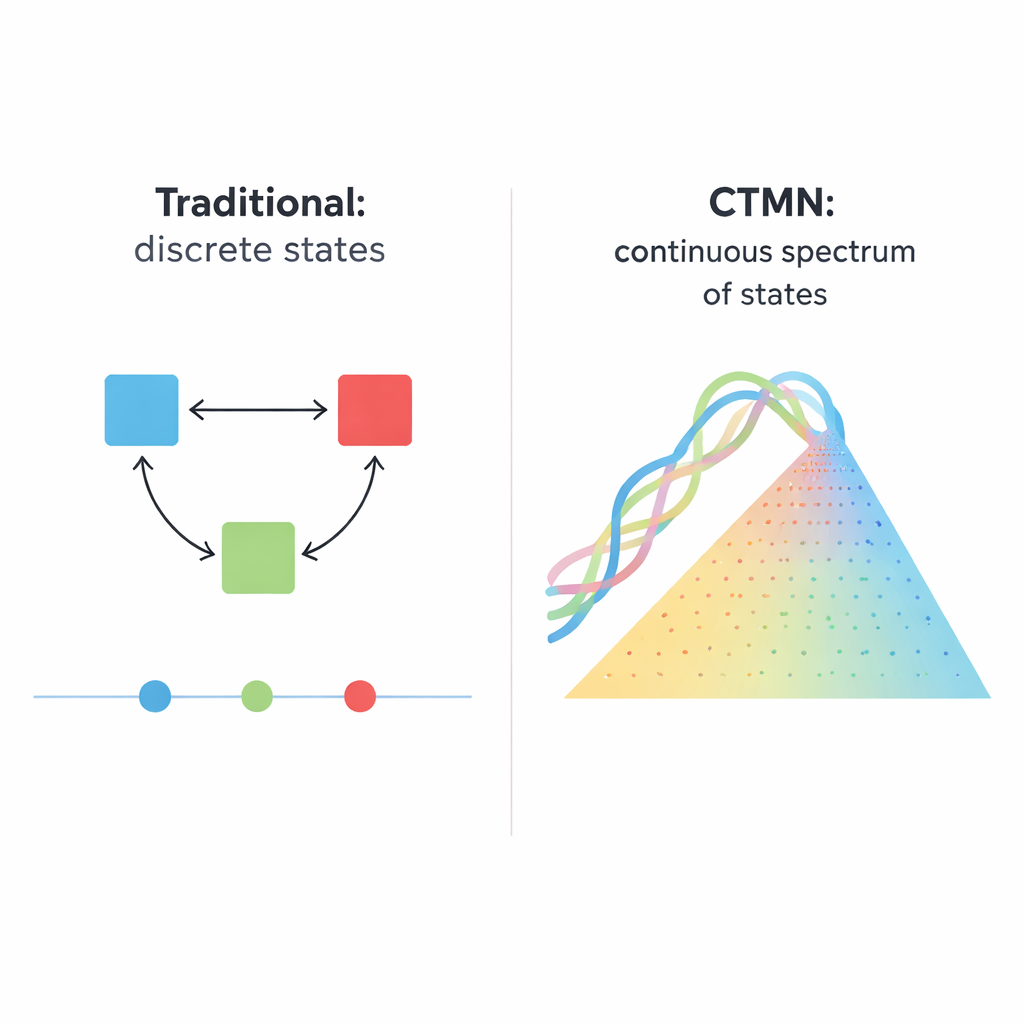
En ny sorts DNA-nätverk: kontinuerligt ställbar
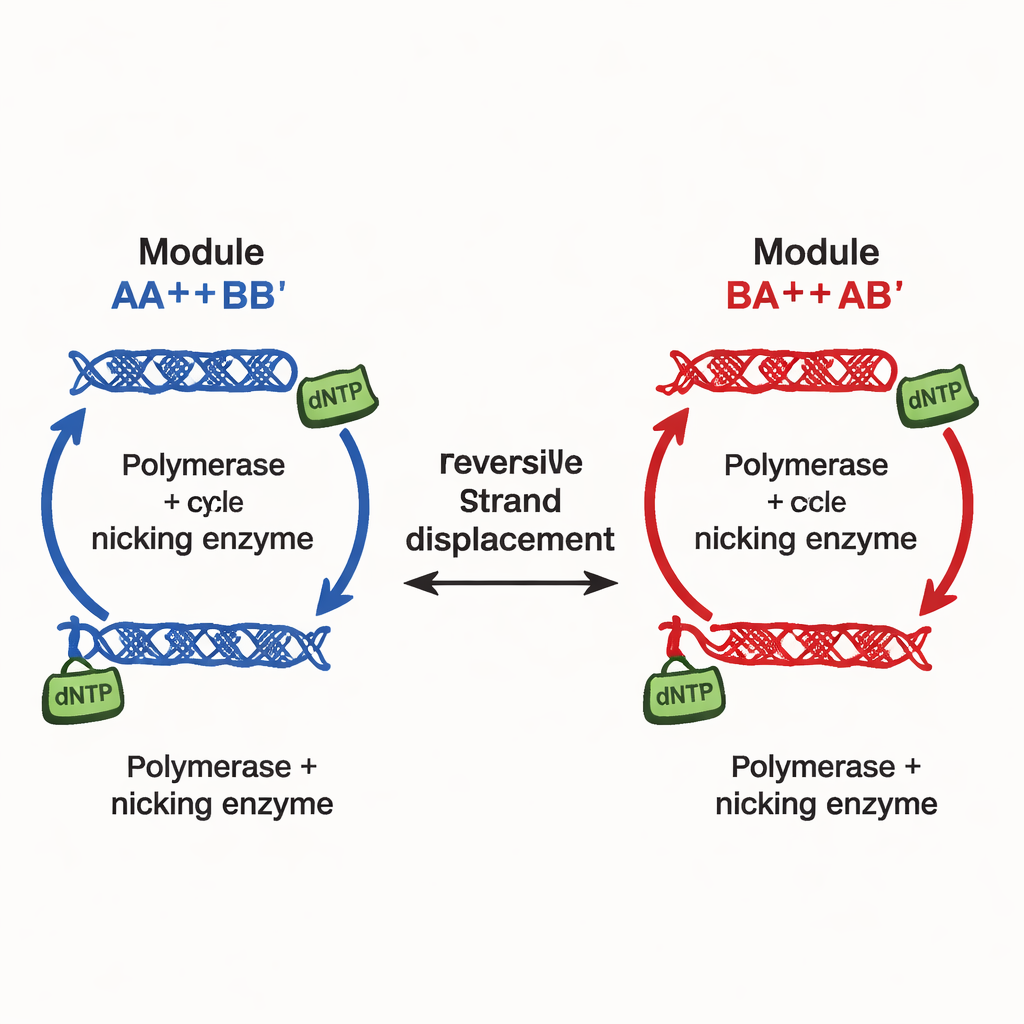
Författarna introducerar en annan designprincip, genomförd i det de kallar kontinuerligt ställbara multistabilitetsnätverk (CTMN). Istället för att förlita sig på många separata hämmande signaler använder de direkt konkurrens mellan DNA‑replikationsmoduler kopplade via reversibla strängutbytesreaktioner. Varje modul består av designade DNA‑duplex som både kan delta i strängdisplacement och fungera som mall för DNA‑polymeras, understödda av ett nickande enzym som klipper och regenererar nyckelsegment. Den kemiska bränslen—nukleotidbyggstenar kallade dNTP—driver pågående polymerisering och nickning och håller systemet långt från jämvikt. Under dessa villkor ”fryser” de konkurrerande modulerna effektivt i de relativa proportioner de startade i, vilket ger inte bara två eller tre utfall utan en hel kontinuerlig linje (eller, för fler moduler, ett plan) av långlivade tillstånd.
Hur den molekylära apparaten låser fast minne
I deras enklaste två‑modulsnätverk, CTMN‑1, visar teamet experimentellt och via detaljerad kinetisk modellering att systemet kan slå sig ner i en familj av stabila blandningar som sträcker sig nästan hela vägen från ”mest modul A” till ”mest modul B.” Polymerisering omvandlar aktiva duplex till förlängda former som temporärt tas ur strängutbyteskonkurrensen; nickning återställer dem och sluter en autoreglerande cykel. När båda modulerna delar denna cykel undertrycker de ömsesidig omvandling så starkt att systemet förblir låst nära sin startkomposition i många timmar, så länge bränsle finns tillgängligt. Linjär stabilitetsanalys av de underliggande ekvationerna avslöjar en hel mångfald—effektivt en kontinuitet—av stationära tillstånd, i kontrast till den enskilda fasta punkten som ses när enzymer eller bränsle tas bort.
Programmerbara svar och molekylärt minne
Eftersom nätverkets tillstånd lagras i DNA‑sammansättningar kan det styras och avläsas på programmerbara sätt. Författarna designar korta RNA‑”triggers” som tillfälligt binder specifika DNA‑strängar, biaserar konkurrensen och förskjuter nätverket till en ny sammansättning. Även efter att RNA:t degraderas av ett enzym kvarstår det nya tillståndet och fungerar som en form av molekylärt minne. Upprepade eller starkare stimuli driver systemet smidigt längs kontinuiteten av tillstånd snarare än att slå om det mellan enkla på/av‑positioner. Dessutom kan DNA‑replikationsprodukterna anpassas för att fungera som signaler för efterföljande processer: i demonstrationer aktiverar olika tillstånd av CTMN‑1 selektivt en av två DNA‑baserade katalysatorer eller biaserar RNA‑transkription mot en av två budbärarsträngar, utan att störa den underliggande multistabiliteten.
Uppskalning till komplexa molekylära “dimmers”
För att visa att strategin är skalbar bygger forskarna ett tre‑modulsnätverk, CTMN‑2, genom att lägga till fler designade DNA‑duplex som delar en gemensam utbytesdomän men kodar för olika replikationsmallar. Nu fyller de möjliga stationära tillstånden en tvådimensionell region, som punkter över ett triangulärt fasdiagram, istället för längs en enkel linje. Återigen bekräftar experiment att många distinkta sammansättningar är stabila så länge bränsle och enzymer finns närvarande, och att alla kollapsar till en enda jämviktspunkt när energiförsörjningen tas bort. Eftersom tillägg av nya moduler kräver endast nya DNA‑konstrukter som kopplas in i samma displacement‑ramverk, ökar inte den övergripande kopplingskomplexiteten som i traditionella designer.
Vad detta betyder för framtida molekylära teknologier
För en icke‑specialist är huvudbudskapet att författarna har förvandlat ett DNA‑replikationsnätverk till en mycket flexibel, analog minnesenhet. Istället för att välja mellan ett fåtal förinställda alternativ kan deras system pålitligt hålla ett av många experimentellt åtskiljbara tillstånd, vardera definierat av hur mycket av varje DNA‑modul som är närvarande, och kan omvandla kortvariga kemiska pulser till långvariga skift längs denna kontinuitet. Eftersom utgångs‑DNA‑strängarna är programmerbara och lösgjorda från stabiliseringsmekanismen, skulle samma ramverk i princip kunna reglera ett brett spektrum av efterföljande biokemiska reaktioner eller materialegenskaper med fin, graderad kontroll. Detta arbete pekar därmed mot molekylära enheter som beräknar, minns och anpassar sig mer som neurala eller mekaniska analoga system än som enkla digitala strömbrytare.
Citering: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Nyckelord: DNA-multistabilitet, molekylärt minne, syntetiska biokemiska nätverk, DNA-strängförskjutning, analog molekylär beräkning