Clear Sky Science · sv
Robust och tolkningsbar prediktion av genmarkörer och celltyper från spatiala transkriptomikdata
Att förvandla rutinmässiga vävnadssnitt till molekylära kartor
När en biopsi tas ser läkare vanligen bara vad mikroskopet visar: cellernas former och mönster i rosa-och-lila färgade preparat. Men under dessa färger finns en dold värld av gener som slås på och av och som påverkar hur en cancer växer och svarar på behandling. I denna studie presenteras STimage, ett nytt artificiellt intelligenssystem (AI) som syftar till att läsa det molekylära manuset direkt från standardpatologibilder, vilket potentiellt kan ge snabbare och billigare insikter utan extra laboratorietester.
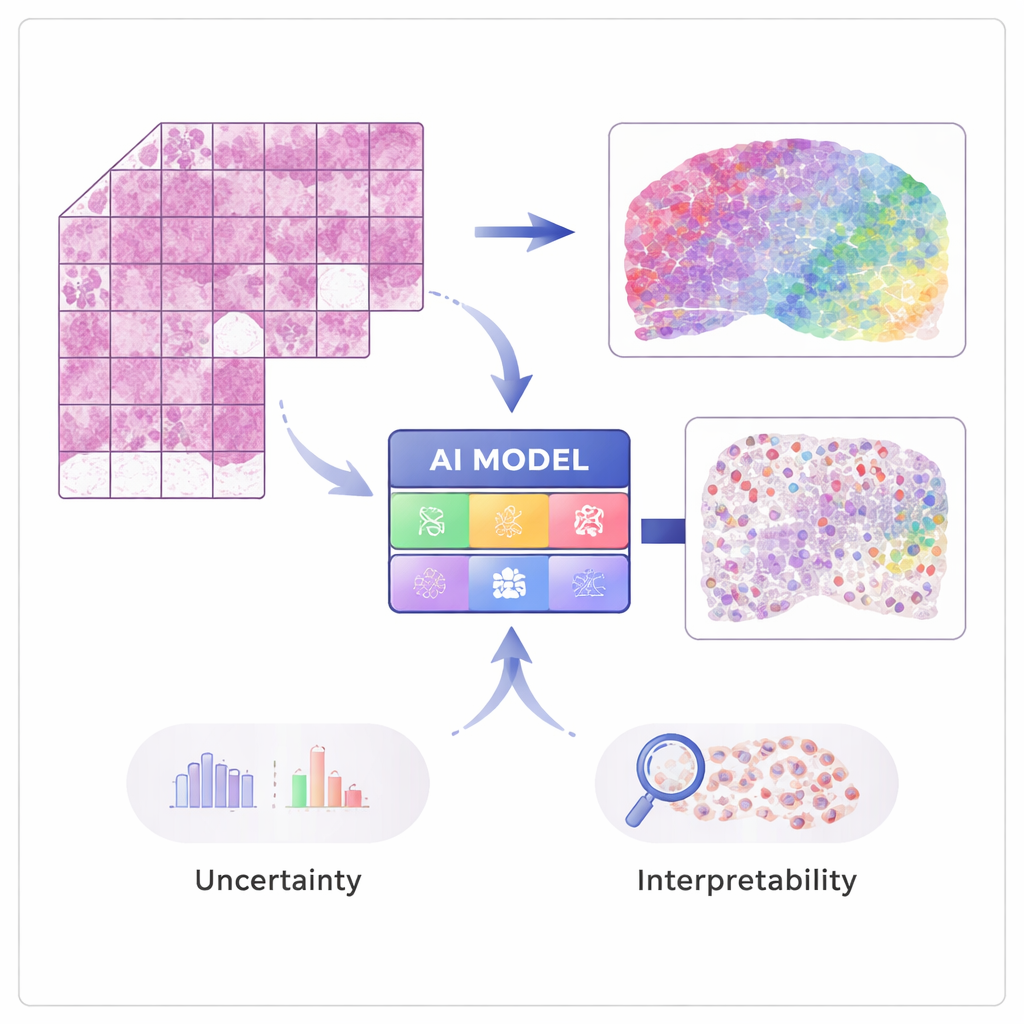
Från bilder till genaktivitet
Moderna tekniker inom ”spatial transkriptomik” kan mäta aktiviteten hos tiotusentals gener samtidigt som de bevarar var varje signal kom ifrån i vävnaden. Dessa metoder är kraftfulla men dyra och ännu inte rutin på sjukhusen. STimage tränas på ett måttligt antal sådana spatiala dataset, där varje vävnadsbild matchas med detaljerade genmätningar vid många små punkter. AI:n lär sig att associera lokala visuella mönster i hematoxylin- och eosinfärgat (H&E) preparat—såsom hur täta eller oregelbundna cellkärnorna är—med underliggande genaktivitet, så att den senare kan förutsäga genuttryck och celltyper från vanliga bilder ensam.
Att bygga en mer pålitlig AI-patolog
Ett centralt mål i arbetet är inte bara noggrannhet, utan också tillförlitlighet och förklarbarhet. Istället för att ge ut ett enda tal för varje gen förutspår STimage en full sannolikhetsfördelning som beskriver ett sannolikt intervall av genaktivitet på varje plats. Den särskiljer också två typer av osäkerhet: en som drivs av brusiga eller varierande data och en annan som speglar modellens egen brist på kunskap. Genom att träna många något olika versioner av modellen och genomsnittliggöra dem—en ”ensemble”-strategi—förbättrar forskarna både prestanda och får en tydligare bild av var systemet är självsäkert och var det inte är det, vilket är avgörande för kliniska beslut.
Testning över cancerformer, teknologier och sjukhus
Teamet utvärderade STimage på mångsidiga dataset från bröst-, hud- och njurcancer samt en immunrelaterad leversjukdom. Den lärde sig att förutsäga viktiga cancer- och immunmarkörer och matchade ofta de verkliga rumsliga mönstren som sågs i oberoende experiment. Modellen höll för när den utmanades med data från olika laboratorier, olika provberedningsmetoder och till och med olika underliggande teknologier, inklusive plattformar med enkelcellsupplösning och äldre, lågupplösta system. I huvud-till-huvud-jämförelser med flera befintliga AI-verktyg kom STimage och dess ensemblevarianter oftast ut i topp, särskilt när man bedömde hur väl de förutsagda mönstren matchade den verkliga fördelningen av genaktivitet över vävnaden.
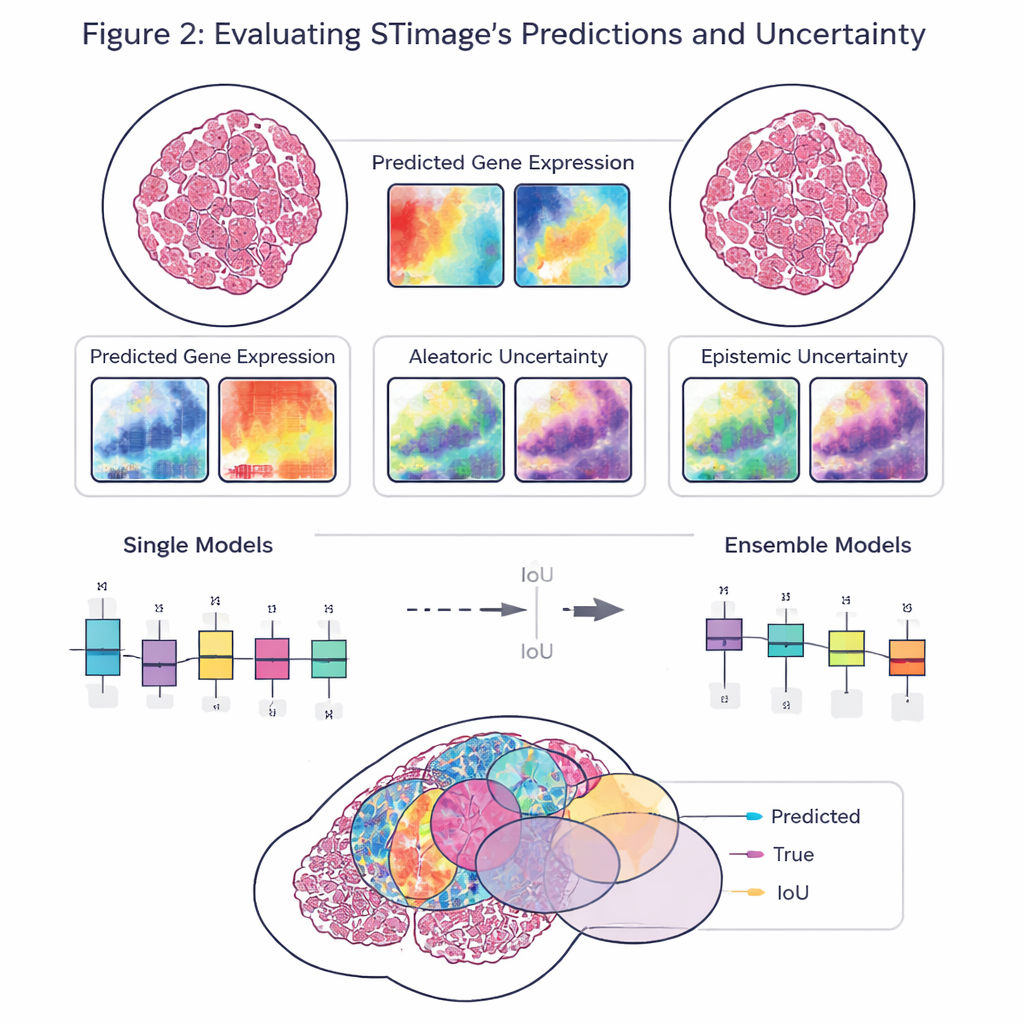
Att se inuti tumörer: celler, överlevnad och läkemedelssvar
STimage går bortom genprediktion för att härleda vilka celltyper som upptar varje region, med hjälp av högupplösta dataset där varje cells identitet är känd. Modellen kunde skilja cancerceller från immunceller och stödjeceller och kartlägga deras arrangemang över ett preparat. Författarna tillämpade sedan STimage på stora samlingar av rutinmässiga cancerbilder från The Cancer Genome Atlas. Även utan rumsliga mätningar låg AI:ns förutsagda genprofiler nära verkliga bulkgen-data. Dessa prediktioner var tillräckligt starka för att dela in patienter i högre- och lägre-riskkategorier och för att hjälpa till att särskilja dem som troligen skulle få ett fullständigt svar på vissa bröstcancerbehandlingar.
Varför detta betyder något för framtida patienter
För patienter och kliniker innebär STimage:s löfte en slags ”molekylär överlagring” på det välbekanta patologipreparatet. Istället för att beställa flera dyra tester skulle en enda skannad bild en dag kunna visa var aggressiva genprogram är aktiva, hur immunceller är fördelade och vilka markörer som pekar mot bättre eller sämre utfall eller olika läkemedelssvar. Även om metoden fortfarande förfinas och korrelationen med verkliga mätningar inte är perfekt, gör dess förmåga att fånga rumsliga mönster, uppskatta sin egen osäkerhet och framhäva vilka celler som driver dess prediktioner det till ett praktiskt steg mot mer informativ och transparent digital patologi.
Citering: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Nyckelord: digital patologi, spatial transkriptomik, cancerbiomarkörer, djupinlärning, tumörmikromiljö