Clear Sky Science · sv
PTRAMP, CSS och Ripr bildar ett konservat komplext som krävs för merozoit-invasion av Plasmodium‑arter i erytrocyter
Varför detta är viktigt i kampen mot malaria
Malariaparasiter måste ta sig in i våra röda blodkroppar för att orsaka sjukdom. Denna studie avslöjar en liten uppsättning proteiner som bildar en gemensam ”ombordningsbro” som används av flera stora malariarter, inklusive de som infekterar människor. Genom att visa hur denna bro byggs upp och hur antikroppar ibland kan blockera den, pekar arbetet mot nya sätt att utforma vacciner som skulle kunna skydda mot mer än en typ av malaria samtidigt. 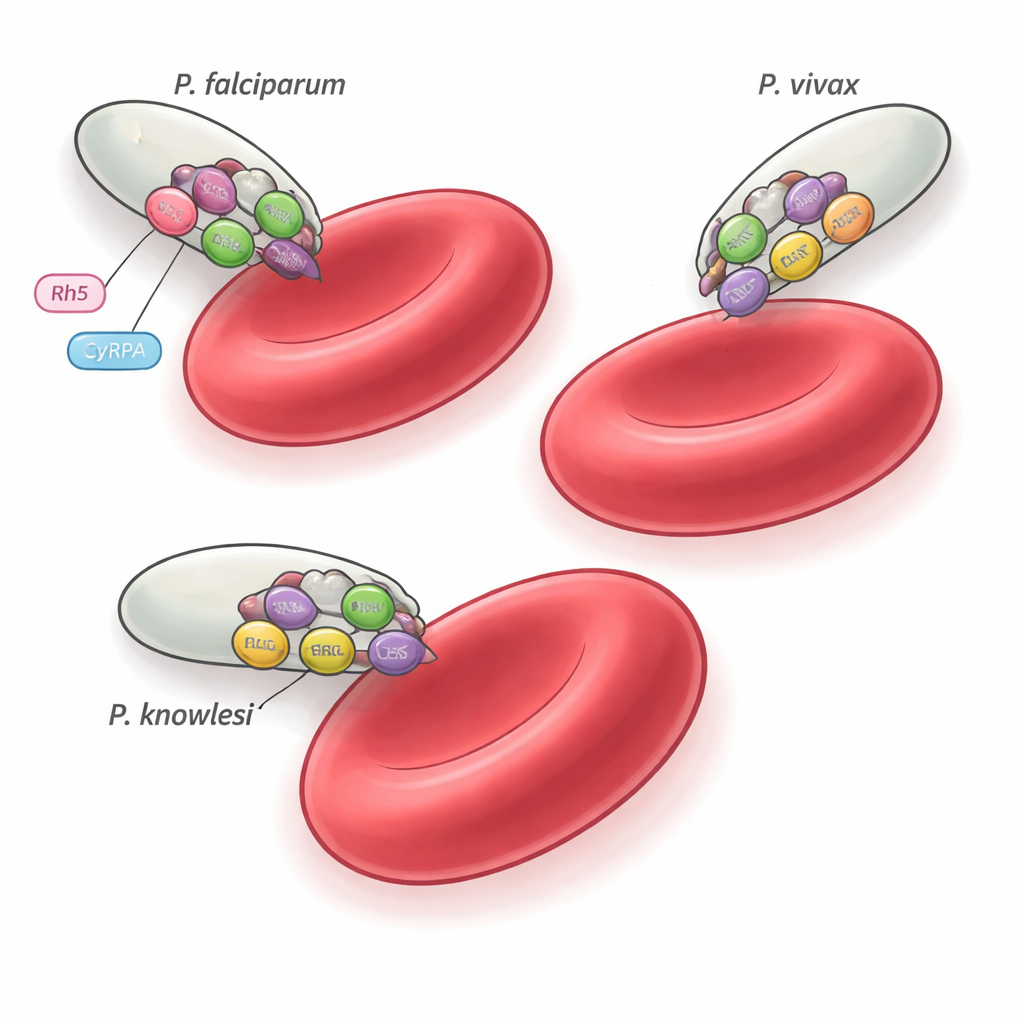
En gemensam verktygslåda hos många malariaparasiter
Det finns mer än 200 Plasmodium‑arter, men endast några få, såsom P. falciparum, P. vivax och P. knowlesi, infekterar människor. Dessa arter ligger på olika grenar i parasitens släktträd och föredrar olika typer av röda blodkroppar, men alla måste invadera erytrocyter med enastående precision. Tidigare arbete i P. falciparum identifierade en femdelad sammansättning, PCRCR‑komplexet, som är nödvändig för invasion och binder till en mänsklig erytrocytreceptor kallad basigin. Ett av komplexets komponenter, ett protein som heter Rh5, är unikt för P. falciparum och dess närmaste släktingar, vilket väcker frågan: vad använder andra malariarter istället? Den aktuella studien fokuserar på tre följeslagarproteiner—PTRAMP, CSS och Ripr—som är konservade över släktet och undersöker om de bildar en universell invasionsmaskin.
Bygga en tredelad invasionsbro
Genom sekvensökningar i många parasitgenom visar författarna att PTRAMP, CSS och Ripr finns i alla stora Plasmodium‑linjer, till skillnad från Rh5 som är begränsat till en undergrupp. Strukturprediktion med AlphaFold, kombinerat med detaljerade biokemiska mätningar, avslöjar att PTRAMP och CSS förenas till ett stabilt par, hållna samman av en specifik disulfidbindning mellan två bevarade cysteiner. Denna tvåproteinplattform klämmer sedan fast vid bakänden av Ripr och skapar ett tredelat PTRAMP–CSS–Ripr (PCR)‑komplex. Experiment med proteiner från P. falciparum, P. vivax och P. knowlesi visar att detta komplex bildas i alla tre arter med hög affinitet, och att endast en liten region i Ripr:s C-terminala ände krävs för stark bindning. 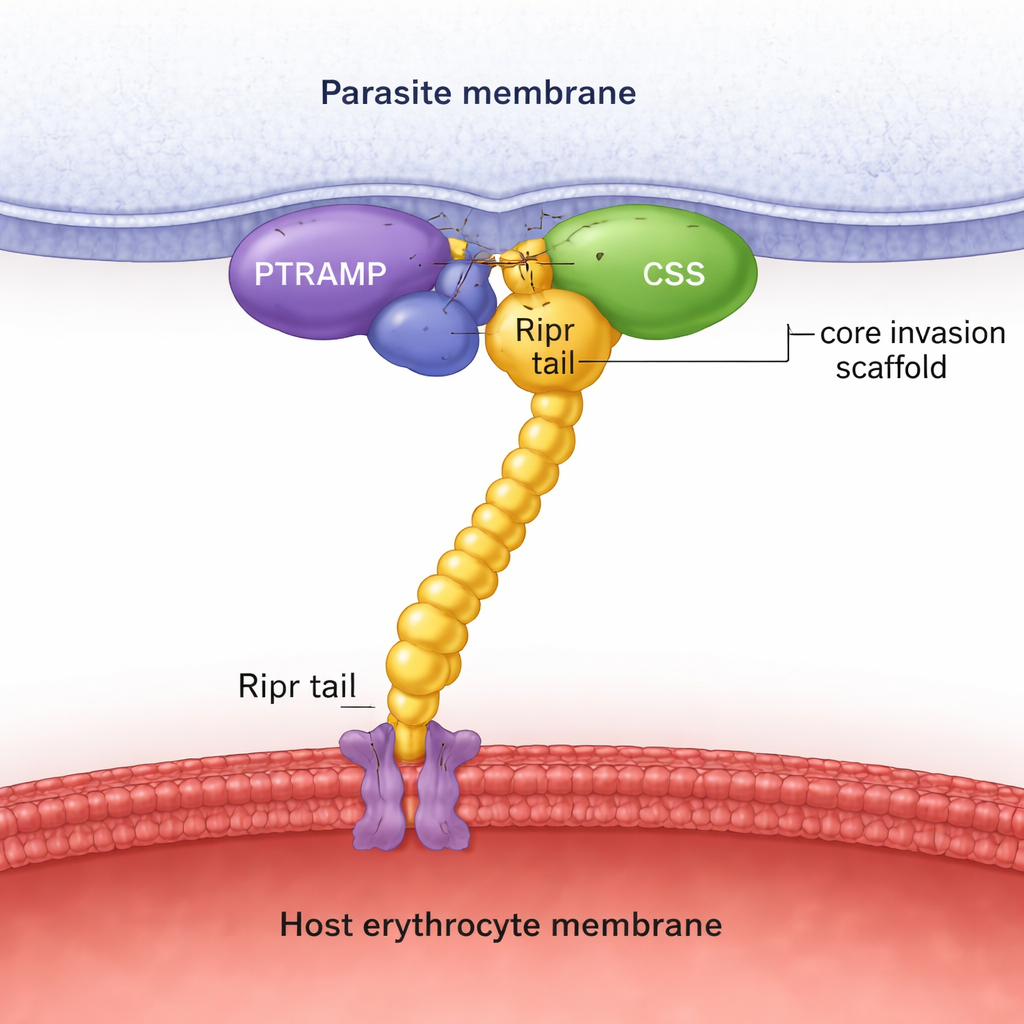
Se strukturen i atomisk detalj
För att gå vidare från förutsägelser löste teamet kristallstrukturer och samlade kryo‑elektronmikroskopibilder. Kristallstrukturen av P. vivax PTRAMP–CSS‑paret visar exakt hur en kort sträcka av PTRAMP trådar sig över CSS och bildar den viktiga disulfidkopplingen. En annan struktur fångar en potent antikropp bunden till två av Riprs tillväxtfaktorliknande domäner och kartlägger ett inhiberande epitop på Ripr‑svansen. Kryo‑EM‑analys av P. knowlesi PCR‑komplexet bekräftar den övergripande form som AlphaFold förutspådde: PTRAMP och CSS sitter nära parasitens membran och greppar Ripr, vars förlängda kropp pekar mot värdcellen. Tillsammans stöder dessa strukturella ögonblicksbilder idén att PCR‑trion bildar ett styvt skelett som fysiskt spänner över gapet mellan parasit och röda blodkropp vid invasion.
Antikroppar som känner igen mer än en art
Eftersom dessa proteiner är konservade undersökte författarna om mänskliga infektioner naturligt genererar antikroppar som korsreagerar mellan arter. Plasma från patienter infekterade med P. falciparum, P. vivax eller P. knowlesi visade starka antikroppsreaktioner mot CSS och Ripr från flera arter, vilket tyder på att människor utvecklar antikroppar mot delade regioner av PCR‑komplexet. Teamet framställde sedan monoklonala antikroppar och nanobodies riktade mot P. vivax PTRAMP, CSS och Ripr och testade om dessa kunde blockera parasittillväxt i kultur. Vissa antikroppar, särskilt en benämnd 5B3 som binder Riprs svans, kunde hämma invasion av P. knowlesi och, vid högre koncentrationer, av P. falciparum. Överraskande nog stoppade samma antikroppar inte P. vivax eller den närbesläktade ap‑parasiten P. cynomolgi, trots att de kunde binda proteiner från dessa arter.
Ett delat skelett med artspecifika påhäng
Funktionstesterna visar att PCR‑komplexet i sig inte fäster vid röda blodkroppar; istället tjänar det sannolikt som ett bevarat strukturellt skelett som varje art fäster sina egna receptor‑bindande partner vid. I P. falciparum samarbetar till exempel PCR‑trion med CyRPA och Rh5 för att engagera basigin på mänskliga erytrocyter. I P. vivax och P. knowlesi återstår de motsvarande receptorbindande proteinerna och värd‑målen att identifiera, men samma PTRAMP–CSS–Ripr‑kärna tycks organisera invasionsmaskineriet. Att vissa antikroppar kan korsreagera men endast hämma vissa arter understryker hur subtila skillnader i komplexets sammansättning och timing kan förändra sårbarheten för immunsvar.
Vad detta betyder för framtida malariavacciner
För en icke‑specialist är huvudpoängen att malariaparasiter av mycket olika arter delar en gemensam ”plugg” de använder för att komma in i röda blodkroppar—gjord av PTRAMP, CSS och Ripr—även om de kopplar den pluggen till olika receptorer på cellytan. Denna bevarade plugg är nu strukturellt kartlagd och kan i vissa fall träffas av antikroppar som fungerar över arter. Även om mer arbete behövs för att identifiera hela uppsättningen partnerproteiner och förbättra inhiberande antikroppar, öppnar upptäckten av ett universellt invasionsskelett dörren för vaccindesigner som kan skydda mot flera typer av malaria snarare än bara en.
Citering: Seager, B.A., Lim, P.S., Xiao, X. et al. PTRAMP, CSS and Ripr form a conserved complex required for merozoite invasion of Plasmodium species into erythrocytes. Nat Commun 17, 1780 (2026). https://doi.org/10.1038/s41467-026-68486-1
Nyckelord: malariainvasion, Plasmodium‑proteiner, merozoitintrång, tvärartsvaccin, erytrocytinfektion