Clear Sky Science · sv
Kryoelektrontomografi avslöjar sammankopplad flavivirusreplikation, knoppning och mognad
Hur hjärninfekterande virus kapar cellmembran
Flavivirus, en stor grupp virus som bland annat innefattar orsakerna till denguefeber och fästingöverförd encefalit, kan tränga in i hjärnan och ge upphov till svår sjukdom. Hur dessa små patogener kopierar sitt genom och sätter ihop nya viruspartiklar inne i våra celler har dock till stora delar förblivit dolt. Denna studie använder banbrytande 3D-elektronmikroskopi vid kryogena temperaturer för att iaktta fästingöverförda flavivirus i arbete inne i humana celler och mus-hjärnvävnad, och avslöjar en oväntat nära koppling mellan genombildning, virusmontering och virusmognad.
Virala fabriker dolda i cellmembran
Flavivirus flyter inte fritt i cellen när de replikerar. I stället remodelerar de ett cellulärt membransystem kallat endoplasmatiskt retikulum (ER) för att bilda specialiserade fickor kända som replikationsorganeller. Dessa liknar små inåtgående knölar på ER:s yta och fungerar som skyddade kammare där viralt RNA kopieras. Med kryoelektrontomografi, en teknik som ger 3D-ögonblicksbilder av celler blixtfrusna i ett nära naturnära tillstånd, visualiserade forskarna dessa knölar i humana lungceller infekterade med ett fästingöverfört flavivirus släkt med viruset som ger fästingburen encefalit. De fann att ER kring infekterade områden sväller och blir packat med kluster av dessa replikationsorganeller, där vissa är tomma medan andra är fyllda med tätt, trådlikt RNA.
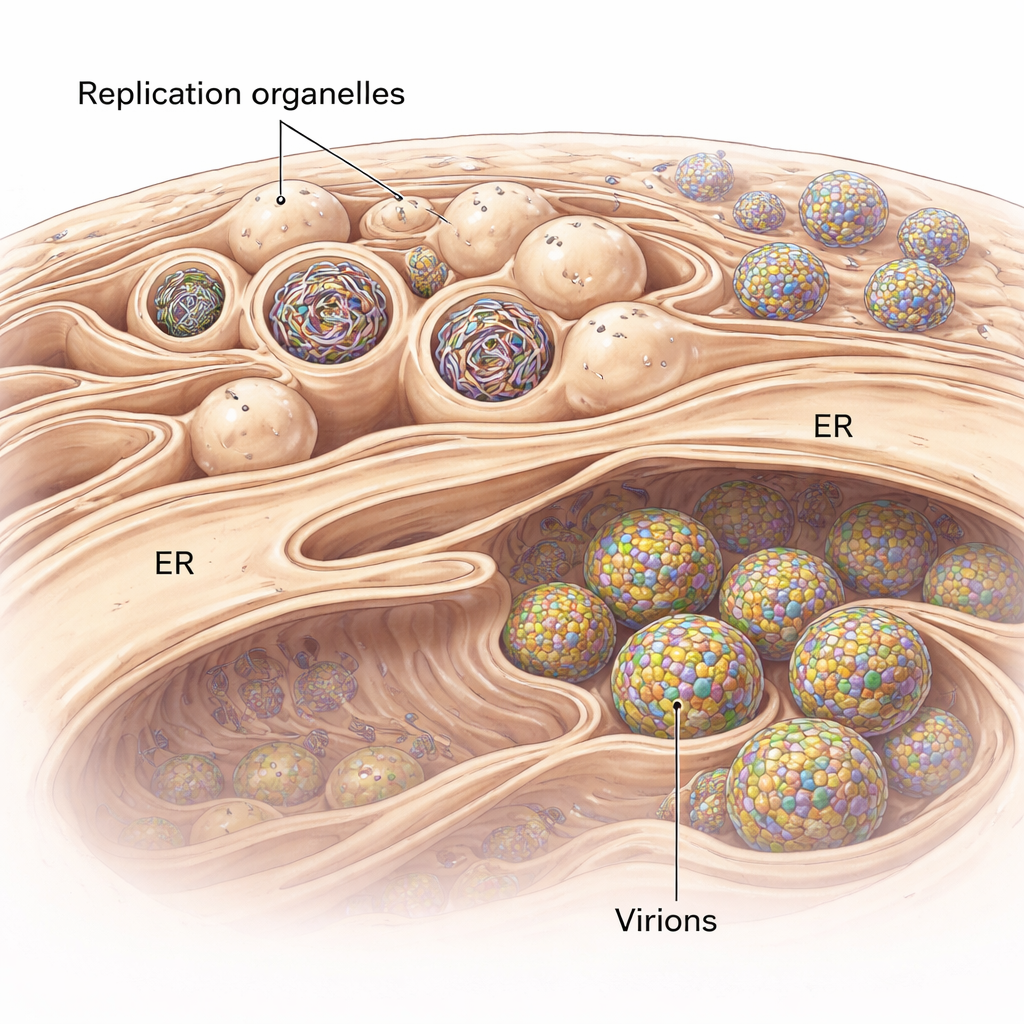
Bygga den perfekta virusbubblan
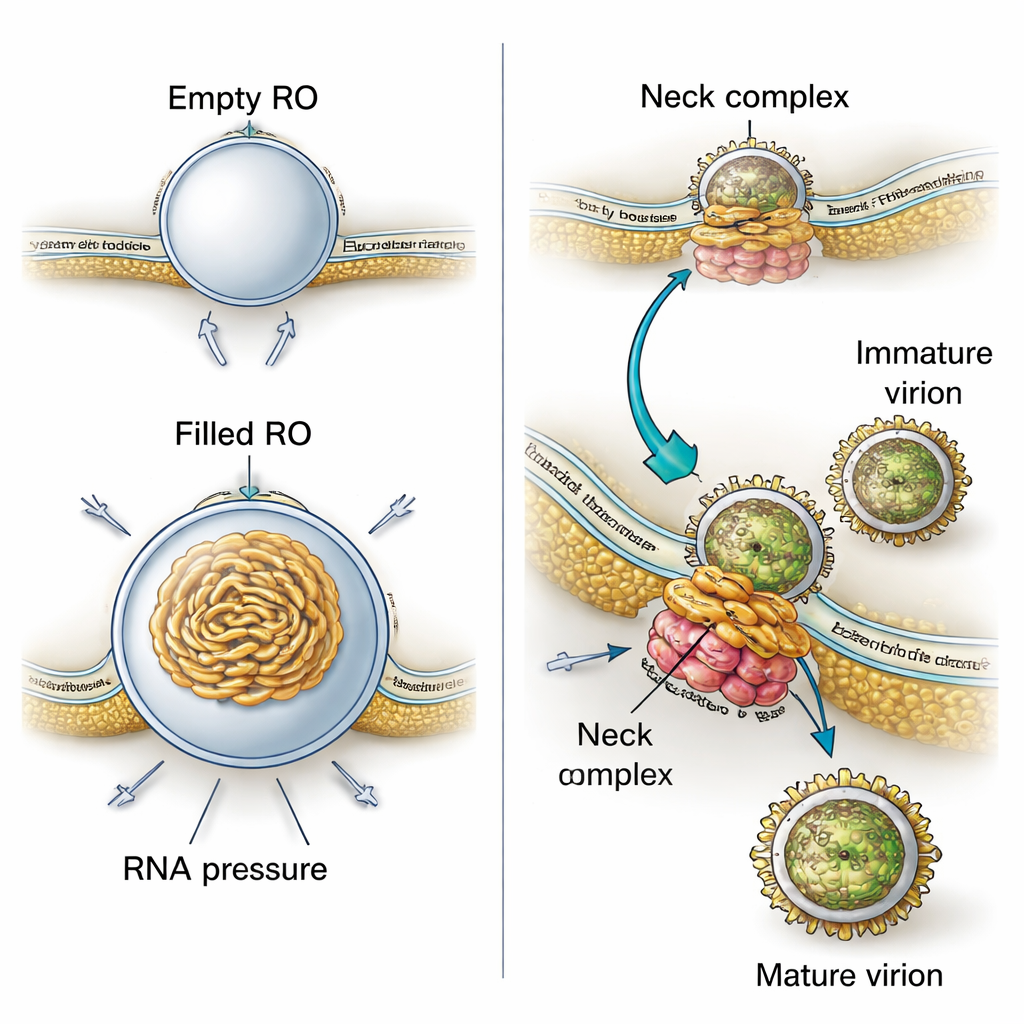
Varför har dessa membranfickor en så exakt, knopp-liknande form? Genom att kombinera sina 3D-bilder med fysikaliska modeller visar författarna att två krafter samarbetar. För det första är membranet i replikationsorganellerna konsekvent tjockare än normalt ER, vilket tyder på att virala proteiner eller förändrade lipider styvar upp och böjer membranet till en stabil knopp redan innan något RNA kommer in. För det andra, när viralt RNA är närvarande, spiralar det ihop sig inne i fickan och trycker utåt, vilket ökar knoppens storlek. Beräkningar baserade på de uppmätta storlekarna indikerar att varje fylld organell sannolikt innehåller ett tryck som motsvarar ungefär en kopia av det virala genomet i dubbelsträngad form. Det innebär att viruset använder både ett förformat membran och den fysiska kraften från sitt eget genetiska material för att bygga och stabilisera sina miniatyrfabriker.
Monteringslinje: från genomkopiering till nya virus
Studien avslöjar också hur tätt virusproduktion är kopplad till dessa replikationsplatser. I sina 3D-vyer observerade forskarna ofta nya viruspartiklar som bildades precis intill replikationsorganellerna och knoppade in i närliggande ER-liknande utrymmen. Omogna partiklar hade en taggig yta, medan mer mogna såg släta ut. Mätningar i tomogrammen visade att omogna partiklar sitter närmare replikationsorganellerna än mogna, vilket antyder att partiklar genomgår de strukturella förändringar som krävs för att bli infektiva under en kort förflyttning genom sammanflätade membrankompartiment. Ett stort proteinkomplex vid den smala ”nacken” där varje replikationsknopp förbinder till cytoplasman verkar fästa replikationsorganellen vid ett intilliggande membran där knoppning sker. Detta komplex fungerar sannolikt som ett molekylärt blixtlås som koordinerar RNA-produktion med paketeringen av det RNA som ska bli nya viruspartiklar.
Fininställning av mognad med en enda aminosyra
För att undersöka hur virusmognad regleras jämförde teamet två versioner av ett chimeriskt virus som skiljer sig med bara en aminosyra i en plats som känns igen av ett värdenzym kallat furin. Detta enzym klyver ett viralt ytprotein och hjälper till att omvandla omogna taggiga partiklar till släta mogna. I provrörstester och i infekterade celler klövs varianten med en arginin i denna position snabbare än varianten med en glutamin. När de visualiserades i celler med kryoelektrontomografi producerade det snabbare klyvande viruset en högre andel mogna partiklar nära replikationsorganellerna. Trots dessa mikroskopiska skillnader visade båda varianterna liknande tillväxt- och sjukdomsmönster i en musmodell, vilket tyder på att viruset kan tolerera en variation i mognadseffektivitet och ändå förbli infektivt.
Att se infektion direkt i hjärnan
De flesta strukturella virusstudier bygger på cellinjer, men detta arbete tar steget in i levande vävnad. Forskarna isolerade en hjärnstruktur kallad plexus choroideus från infekterade möss och förberedde den för kryoelektrontomografi med högtrycksfrysteknik och fokuserad jonbionslipning. Även i denna komplexa miljö observerade de samma kännetecken: kluster av replikationsorganeller, förtjockade membran och närliggande vesiklar fyllda med mogna viruspartiklar. Detta visar att membranomformningen och den tätt kopplade replikation–montering–mognadssekvensen som ses i odlade celler också är aktiv i hjärnan, där dessa virus orsakar sjukdom.
Varför dessa dolda arbetsflöden är viktiga
För icke-specialister är huvudbudskapet att dessa hjärninfekterande virus driver en högst organiserad monteringslinje inne i våra celler. De formar cellmembran till små pressade bubblor där genomen kopieras, kopplar dessa bubblor direkt till platser där nya partiklar knoppas av, och påbörjar till och med de sista mognadsstegen inom räckhåll från den ursprungliga replikationsplatsen. Identifieringen av de förtjockade replikationsmembranen, proteinkomplexet som spänner över nacken och de tätt sammanflätade mognadskompartimenten förklarar inte bara hur flavivirus replikerar så effektivt, utan pekar också på nya mål för antivirala läkemedel utformade för att störa virusets dolda fabriker och monteringsvägar.
Citering: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
Nyckelord: flavivirus, kryoelektrontomografi, replikationsorganeller, virusmognad, fästingöverförd encefalit