Clear Sky Science · sv
Spektroelektrokemisk insikt i koppar-kobolt-katalysatorer för samtidig elektroreduktIon av CO2 och nitrit till urea
Att förvandla avfallsgaser till gödsel
Urea-gödsel är grundläggande för modern jordbruk, men dess konventionella framställning kräver mycket energi och ger stora koldioxidutsläpp. Denna studie undersöker en helt annan väg: att med elektricitet omvandla koldioxid (CO2) och kvävehaltigt avfall (som nitrit från avgaser eller avloppsvatten) direkt till urea. För en allmän läsare är lockelsen tydlig: en väg till ett väsentligt gödselmedel som kan minska utsläpp, använda avfallsströmmar som råvara och en dag även drivas med förnybar el.
Varför tänka om hur vi tillverkar urea?
Idag framställs urea mest genom att först producera ammoniak från kväve och fossilt väte (Haber–Bosch-processen) och därefter reagera ammoniak med CO2 vid höga temperaturer och tryck. Denna reaktionskedja är centraliserad, kapitalintensiv och ger nära ett ton CO2 per ton producerad urea. När den globala efterfrågan på gödsel ökar, stiger också de miljömässiga kostnaderna. Ett alternativ är att helt kringgå fossila bränslen genom att driva de centrala kemiska stegen med elektricitet, helst från förnybara källor, och genom att använda CO2 och kväveoxider (NOx) som i dag hanteras som avfall.
En ny roll för koppar och kobolt
Författarna utformar tunnfilmskatalysatorer genom samtidig sputtring av koppar (Cu) och kobolt (Co) på kolpapper och finjusterar noggrant Cu:Co-förhållandet. De fokuserar på samtidig elektroreduktions av CO2 och nitrit (NO2⁻) i vatten vid neutral pH, en miljö som kan gynna den känsliga bildningen av kol–kväve (C–N)-bindningar som krävs för urea. Den framstående sammansättningen är en 1:1-blandning av Cu och Co, som uppnår en ureakvot på ungefär 61 millimol per timme per gram katalysator vid en måttlig applicerad spänning. Mikroskopi och röntgenmätningar visar att metallerna är intimt blandade på atomskala och förblir till största delen metalliska under drift, vilket ger en robust plattform där både CO2 och nitrit kan reagera effektivt. 
Hur katalysatorn delar upp och samverkar
Att tillverka urea på detta sätt är utmanande eftersom enklare reaktioner—som att bilda vätgas eller reducera enbart CO2 eller nitrit—konkurrerar starkt. Nyckeln, visar forskarna, är en arbetsdelning mellan koppar- och koboltställen som samarbetar. ElektroKemiska tester visar att koppar ensam huvudsakligen omvandlar CO2 till kolbaserade bränslen och kemikalier, medan kobolt ensam huvudsakligen omvandlar nitrit till ammoniak, utan urea i något av fallen. Endast när Cu- och Co-atomer är tätt blandade ser man betydande urea. Spektroskopiska ”ögonblicksbilder” tagna under reaktionen upptäcker karakteristiska ytbundna fragment: kolarter härledda från CO2 (*CO och *COOH) som föredrar koppar, och kvävearter härledda från nitrit (*NH2 och näraliggande grupper) som föredrar kobolt. Vid gränsytorna mellan Cu och Co kan dessa fragment mötas och kopplas för att bilda ureas C–N-ryggrad.
Att hitta rätt villkor för att bygga bindningar
Studien visar att sammansättning ensam inte räcker; omgivande lösning och membran måste också justeras. Urea bildas endast i en neutral bikarbonatelektrolyt, som håller tillräckligt med löst CO2 tillgängligt och förser precis rätt mängd protoner (vätejoner) för att driva proton-kopplade elektronöverföringssteg utan att överbelasta ytan med vätgasutveckling. Under starkt sura eller starkt basiska förhållanden bildas antingen ingen urea eller så sönderfaller den snabbt till enklare produkter. Experiment med olika kvävekällor visar att nitrit är särskilt effektivt för ureakonstruktion och överträffar nitrat och hydroxylamin. Testkörningar över många timmar indikerar att Cu–Co-filmerna är relativt stabila, med endast måttliga metallförluster och bibehållen ureakvot.
En titt under huven med teori
För att förstå varför denna tandemkatalysator fungerar så bra använder teamet datorsimuleringar baserade på densitetsfunktionalteori. Dessa beräkningar stöder idén att koppar gynnar bindning av CO2-deriverade arter, medan kobolt bättre aktiverar nitrit och stabiliserar kväveinnehållande fragment. Simuleringarna pekar på ett särskilt steg som den energimässiga flaskhalsen: kopplingen av ett *NH2-fragment (från nitrit) med ett *COOH-fragment (från CO2) för att bilda ett intermediär som ibland skrivs som *NH2CO. När denna del är på plats är de återstående stegen till urea relativt enkla. Cu–Co-gränsytan sänker energikostnaden för denna avgörande koppling jämfört med rent koppar eller rent kobolt, vilket förklarar den experimentellt observerade ökningen i ureaavkastning för det bimetalliska systemet. 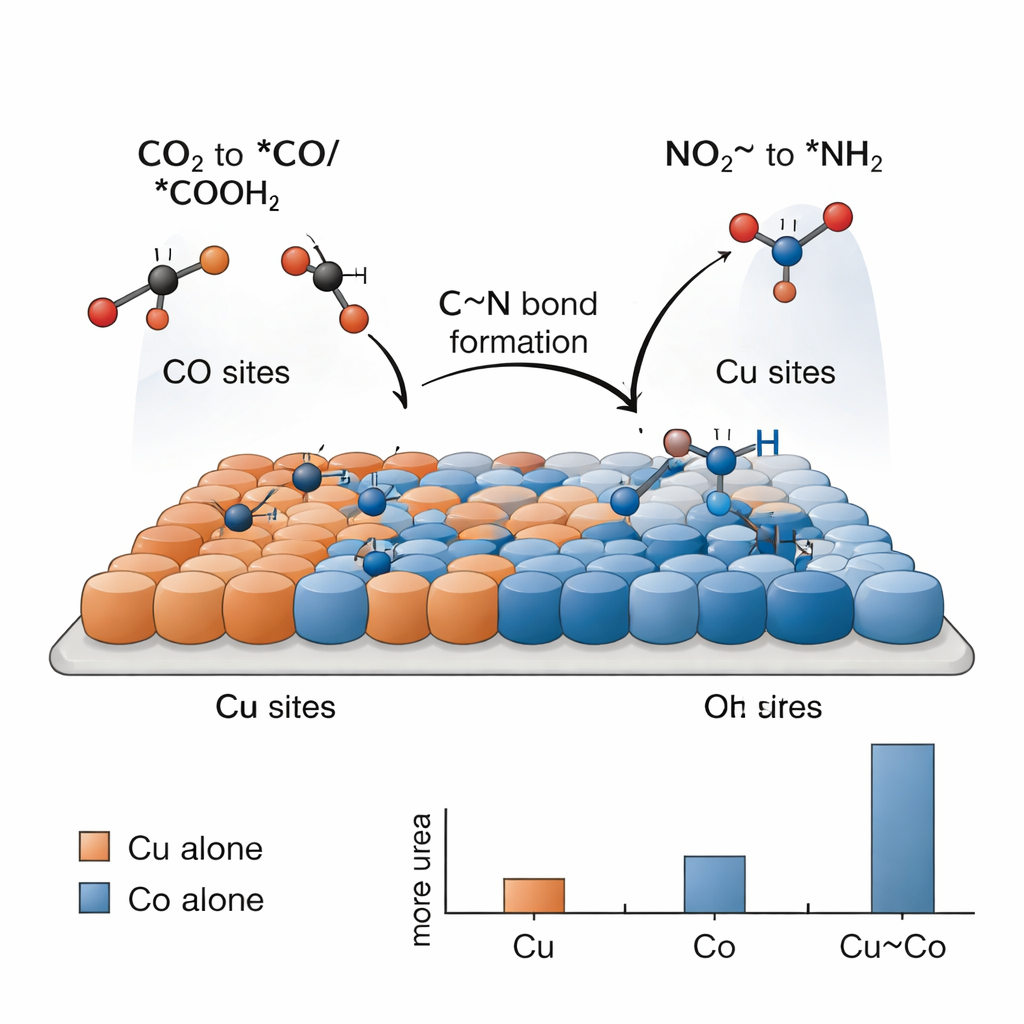
Från laboratorieinsikt till grönare gödsel
I praktiska termer ersätter detta arbete ännu inte dagens enorma ureatillverkningsanläggningar, men det klargör hur en framtida elektrokemisk väg kan utformas. Genom att visa att koppar och kobolt kan fungera i tandem—den ena levererar aktiverade kolarter, den andra aktiverade kvävearter, båda under noggrant kontrollerade protonvillkor—kartlägger studien en realistisk väg mot renare, potentiellt decentraliserad ureatillverkning som använder CO2 och kvävavfall som resurser snarare än föroreningar.
Citering: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
Nyckelord: elektrokemisk ureasyntes, koppar-kobolt-katalysator, CO2-användning, nitritreduktion, C–N-koppling