Clear Sky Science · sv
Strukturell grund för selektiv hämning av mänskliga GABA‑transportören GAT3
Varför dämpande hjärnsignaler är viktiga
Våra hjärnor förlitar sig på en känslig balans mellan signaler som exciterar och sådana som dämpar. En viktig dämpande budbärare är GABA, ett ämne som hjälper till att förhindra okontrollerad aktivitet kopplad till tillstånd som epilepsi, skador efter stroke och Alzheimers sjukdom. Den här studien fokuserar på ett protein kallat GAT3, som avlägsnar GABA från omkring nervcellerna. Genom att visa, i atomär detalj, hur en ny molekyl fäster vid GAT3 och slår av det, ger forskarna en strukturell färdplan för att utforma nästa generations läkemedel som skulle kunna förstärka hjärnans naturliga bromssystem på ett försiktigt sätt.
Hjärnans egen bromspedal
GABA är den främsta inhibitoriska, eller dämpande, neurotransmittorn i centrala nervsystemet. Efter att GABA släpps från nervändar måste det snabbt tas bort så att hjärnkretsar kan återställas. Denna städning utförs av transportörproteiner som pumpar tillbaka GABA in i celler. Två av dessa transportörer dominerar i hjärnan: GAT1, som främst finns på neuroner, och GAT3, som finns på stödjeceller kallade astrocyter. Medan ett GAT1‑blockerande läkemedel (tiagabin) har använts i årtionden för att behandla epilepsi, har jämförbara läkemedel som riktar sig mot GAT3 halkat efter. GAT3 är ändå särskilt intressant eftersom det kontrollerar GABA‑nivåer utanför synapser och formar långvarig, bakgrundsdämpning som kan finjustera hjärnaktiviteten. 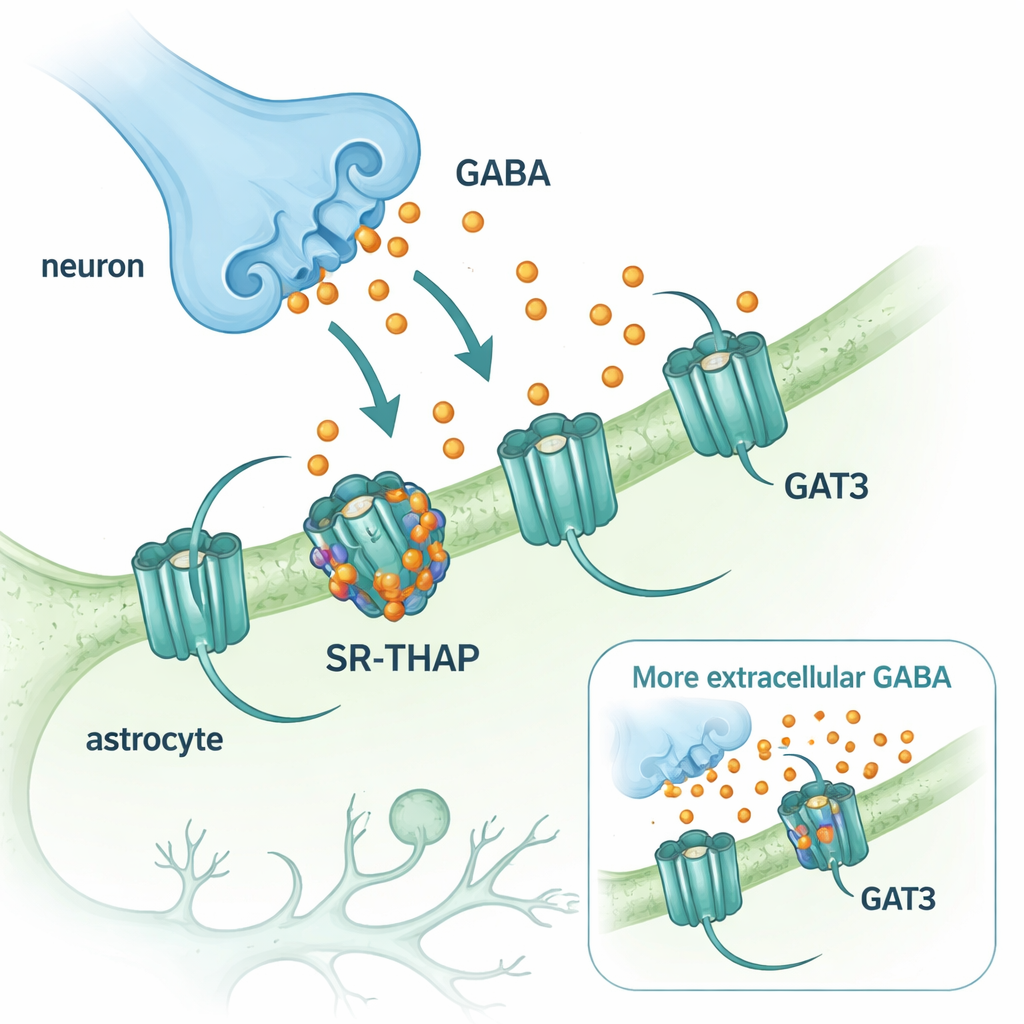
Att designa ett mer precist molekylärt lås
Försök att hämma GAT3 har hindrats av brist på detaljerad strukturell information. Många tidigare föreningar skapades genom trial‑and‑error, ofta genom att göra skrymmande variationer av kända GABA‑lika molekyler. En av de bäst kända, (S)‑SNAP‑5114, visade sig vara kemiskt instabil och svår att använda i levande djur. Byggande på en mer robust släkting till denna förening utvecklade författarna SR‑THAP, en ny liten molekyl utformad för att passa GAT3 mer tätt och motstå nedbrytning. Experiment i humana cellkulturer visade att SR‑THAP kraftigt blockerar GAT3 och gör det på ett icke‑konkurrerande sätt: istället för att helt enkelt konkurrera med GABA vid den vanliga platsen förändrar den hur transportören fungerar och minskar dess maximala transportkapacitet.
Att se GAT3 i nästan atomär upplösning
För att förstå exakt hur SR‑THAP fungerar vände sig teamet till kryo‑elektronmikroskopi, en teknik som avbildar blixtfrusna proteiner med elektroner och rekonstruerar deras tredimensionella form. De löste tre versioner av mänskligt GAT3: bundet till SR‑THAP, bundet till GABA och i ett substratfritt tillstånd. Alla tre visar den typiska arkitekturen som ses i närliggande neurotransmittortransportörer: 12 tätt packade helixar som spänner över membranet och bildar en central väg för GABA och dess följeslagande joner, natrium och klorid. I den GABA‑bundna strukturen sitter transportören i ett ”inåt‑occluderat” tillstånd—GABA och en natriumjon är klämda i mitten, förseglade från både utsida och insida. En nyckelaromatisk aminosyra bildar en specialiserad interaktion med GABA:s aminogrupp, vilket hjälper till att förklara hur GAT3 känner igen sitt substrat.
Hur SR‑THAP kilas fast och öppnar transportören
I slående kontrast fångar SR‑THAP‑bundna strukturen GAT3 i ett ”inåt‑öppet” tillstånd, där den interna sidan av proteinet gapar mot cellens inre. SR‑THAP ligger djupt i denna inre kavitet, kilad mellan flera helixar som normalt rör sig under transportcykeln. Den upptar tre små fickor med olika kemiska karaktär, och engagerar ett nätverk av vätebindningar och hydrofoba kontakter. Denna positionering sätter effektivt fast transportören så att GABA och joner inte längre kan fullfölja sin resa. Författarna visar att ett fåtal specifika aminosyror som kantar denna kavitet skiljer sig mellan GAT3 och dess nära släktingar; att byta ut en av dessa rester ändrar både transportaktivitet och SR‑THAP:s potens, vilket hjälper till att förklara varför inhibitorn är mycket mer selektiv för GAT3 än för GAT1 eller besläktade transportörer. 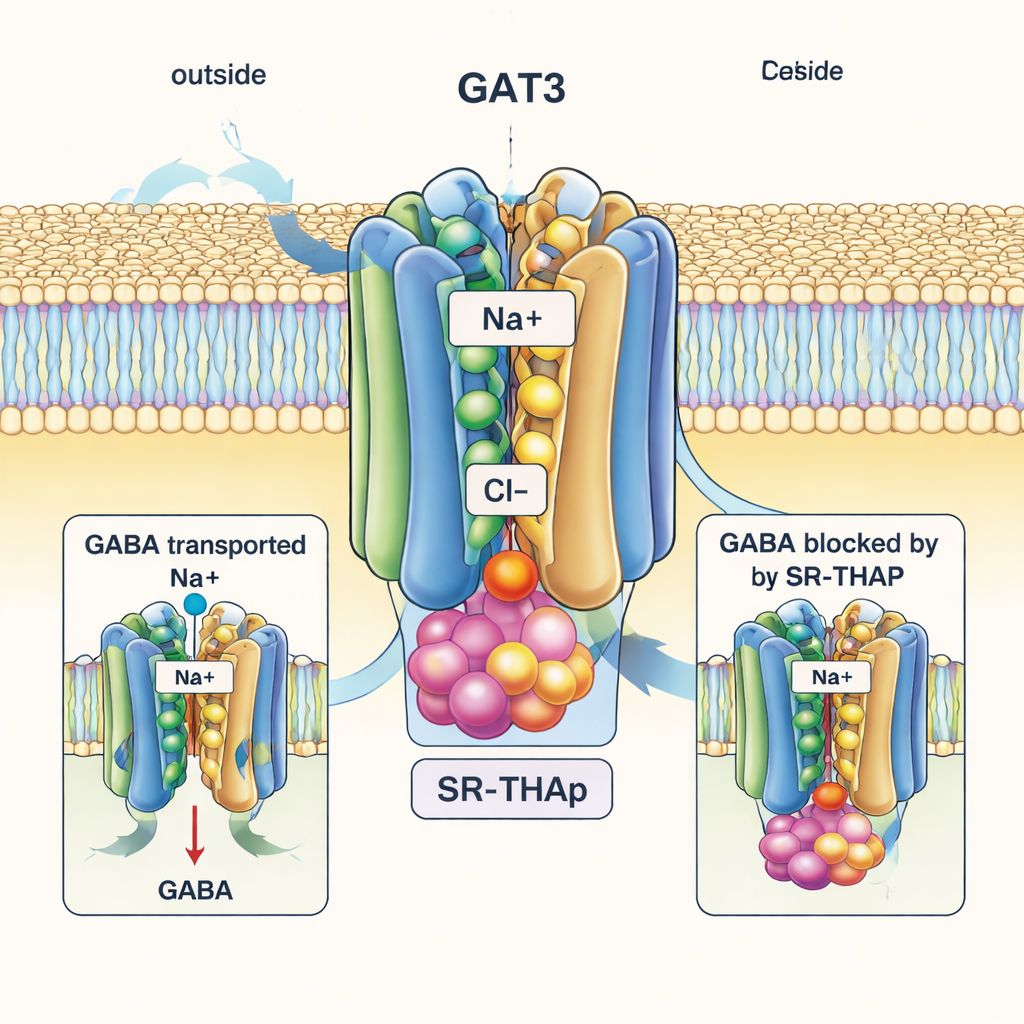
Öppnar dörrar för nya läkemedel mot epilepsi och hjärnhälsa
Tillsammans visar dessa strukturer hur GAT3 växlar mellan olika former för att flytta GABA, och hur SR‑THAP utnyttjar en mindre bevarad inre ficka för att frysa den cykeln. För icke‑specialister är huvudpoängen att studien levererar en detaljerad molekylär ritning för att stänga av GAT3 på ett mycket selektivt sätt. Sådana föreningar skulle kunna höja dämpande GABA‑nivåer på ett mer finställt sätt än befintliga läkemedel, vilket potentiellt kan leda till nya behandlingar eller forskningsverktyg för epilepsi, återhämtning efter stroke, Alzheimers sjukdom och andra tillstånd där inhibitorisk signalering är störd.
Citering: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Nyckelord: GABA‑transportör, GAT3, epilepsi, kryo‑EM, neurotransmittor‑inhibition