Clear Sky Science · sv
En stokastisk mekanism driver snabb substrattranslokation i AAA+-maskinen ClpB
Hur cellulära maskiner håller proteiner i rörelse
Inuti varje cell drar, sliter och formar små molekylära maskiner ständigt proteiner för att förhindra att de klumpar ihop sig och för att reparera skador. En sådan maskin, kallad ClpB, hjälper till att rädda proteiner som trasslat ihop sig—en avgörande uppgift för cellens överlevnad under stress. Denna studie ställer en enkel men djup fråga: hur omvandlar ClpB den kemiska bränslen ATP till det mekaniska arbete som krävs för att dra en proteinkedja genom sin centrala por, och sker det i prydliga, klockliknande steg eller på ett mer slumpmässigt, diffust sätt?
En räddningsring för proteiner i arbete
ClpB tillhör en stor familj enzymer som kallas AAA+-maskiner som sätter ihop sig till ringformade strukturer med en central tunnel. Många har avbildats i utsökt detalj med cryo-elektronmikroskopi, vilket gett upphov till en populär "hand-över-hand"-modell: varje ATP-molekyl som förbrukas skulle driva ett litet, precist steg, som ett team som drar i ett rep i tur och ordning. Andra experiment antydde dock att ClpB kan föra proteiner mycket snabbare än dess långsamma ATP-förbrukning verkar tillåta. För att lösa detta pussel följde författarna enskilda ClpB-molekyler i realtid medan de förde ett flexibelt testprotein, κ-casein, genom sin por.
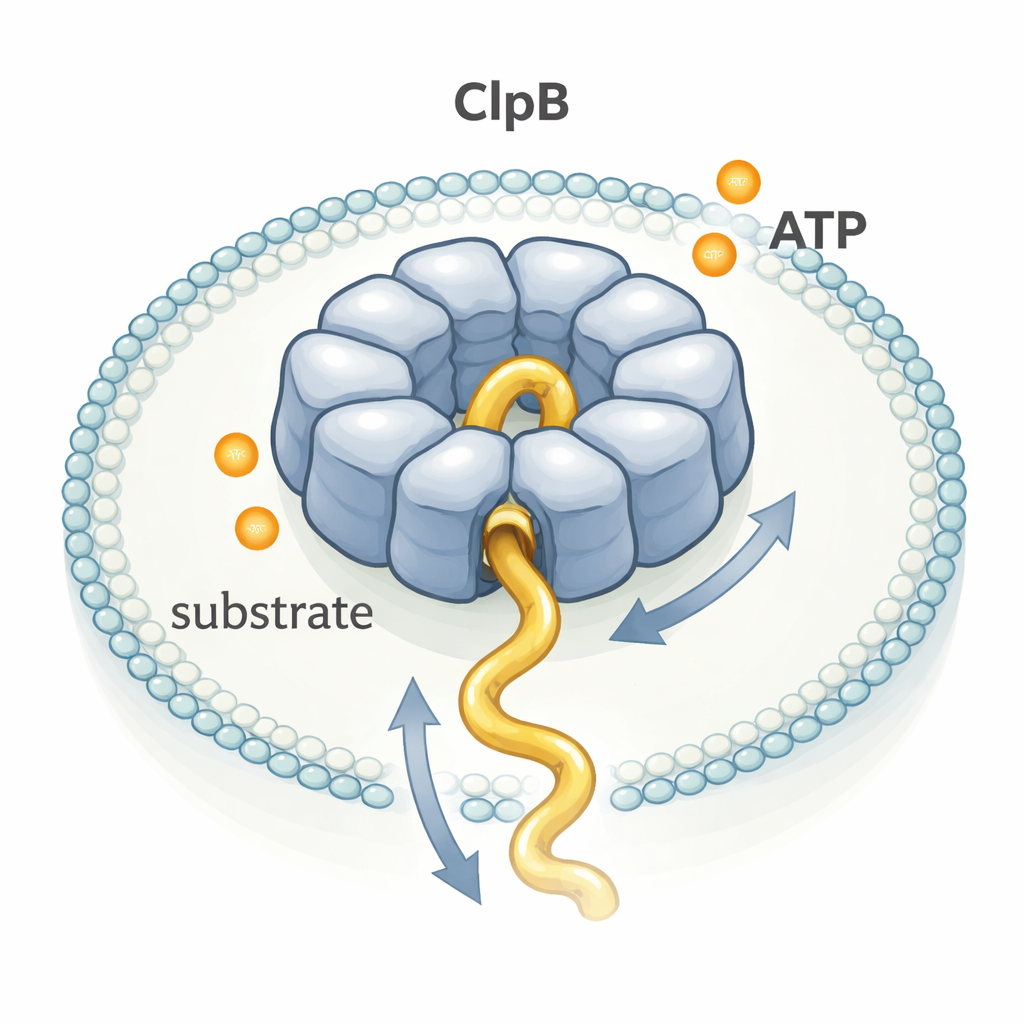
Att observera en molekyl i taget
Forskarna fångade individuella ClpB-ringar och enskilda κ-casein-molekyler tillsammans inne i små lipidsäckar som var fästa på en glasyta. De fäste fluorescerande färgämnen på specifika punkter på ClpB och på proteinkedjan, och använde sedan enkelmolekyl-FRET, en teknik som rapporterar förändringar i avstånd mellan färgämnen på nanometerskala. När κ-casein gled in i ClpB-poren kom färgämnena nära varandra och FRET sköt i höjden som en kort spik; när kedjan lämnade sjönk signalen igen. Genom att mäta varaktigheten och höjden på tusentals sådana spikar kunde de härleda hur snabbt och hur långt segment av proteinet trädde genom poren.
Snabbt, svagt driftat och nästan temperaturoberoende
Överraskande nog var translokationsepisoderna extremt snabba: det märkta segmentet av κ-casein färdades typiskt flera nanometer genom poren på cirka 1–2 millisekunder—ungefär tusen gånger snabbare än den genomsnittliga tiden mellan ATP-hydrolyshändelser i ClpB. De flesta händelser var så korta och följde en bred, potenslagringsfördelning snarare än en enda karakteristisk tidsskala. Att ändra temperaturen från 10 till 32 °C bromsade knappt dessa rörelser, vilket antyder att energibarriären för rörelse är liten jämfört med den för klassiska "power-stroke"-motorer som kinesin. Likaså minskade en lägre ATP-koncentration kraftigt hur ofta händelser inträffade, men hade nästan ingen effekt på hur lång varje händelse var. ATP styrde med andra ord när ClpB engagerade sig och hur frekvent det agerade, mer än hastigheten hos individuella trådningsutbrott.
Fram- och återrörelse med framåtriktad förskjutning
För att se om kedjor alltid rör sig i en riktning utförde teamet mer komplexa trefärgade FRET-experiment och färgade båda ändarna av poren och substratet. Detta gjorde det möjligt för dem att skilja på om κ-casein trädde in från ringens topp eller botten och om det passerade hela vägen igenom eller drog sig tillbaka. De upptäckte sex olika mönster: komplett fram- och bakåtsträdning, längre "partiella" besök där kedjan provade båda ändarna av poren innan den lämnade, och flyktiga möten nära endast ena änden. Ungefär tre fjärdedelar av de kompletta händelserna gick i framåtriktningen, men en betydande andel gick bakåt, vilket visar att ClpB tillåter bidirektionell diffusion av sitt substrat med endast en måttlig framåtriktad förskjutning. När ATP ersattes av en långsamt hydrolyserad analog blev händelserna sällsynta och mycket långsammare, och den framåtriktade preferensen försvann i praktiken.
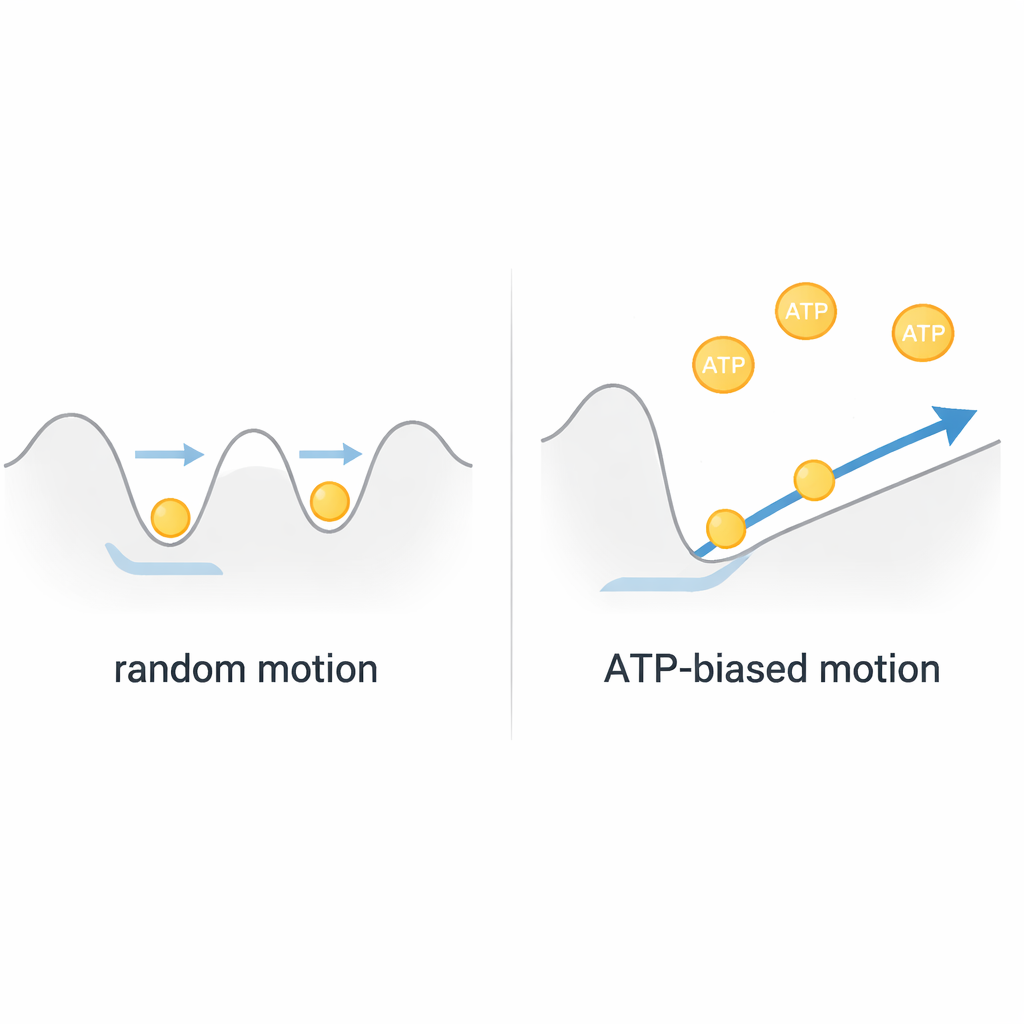
En Brownsk motor, inte en enkel vinsch
Sammantaget drar författarna slutsatsen att ClpB fungerar mer som en Brownsk motor än som en stel, bränsledriven vinsch. Proteinkedjan jiggar termiskt inom ett grunt energilandskap inne i poren och rör sig fram och tillbaka i hög hastighet. ATP driver inte direkt stora, diskreta dragstötar; istället formar det detta landskap via snabba rörelser hos interna "por-loopar" och favoriserar subtilt rörelse i en riktning. Eftersom varje komplett trädningshändelse korrelerar med endast omkring en eller två konsumerade ATP-molekyler uppnår ClpB anmärkningsvärt effektiv, snabb transport genom att rektifiera slumpmässig rörelse snarare än att kämpa emot den. Denna syn omformar vår uppfattning om många AAA+-maskiner och antyder att biologiska nanomotorer ofta kan utnyttja slumpmässighet snarare än att eliminera den.
Citering: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Nyckelord: proteintranslokation, AAA+-maskin, Brownsk motor, molekylär chaperon, enkelmolekyl-FRET