Clear Sky Science · sv
Struktur hos en Brochothrix thermosphacta-bakteriofag avslöjar mekanism för adsorption till cellväggen hos siphophager som infekterar Gram-positiva bakterier
Virus som håller vår mat färsk
Bakteriedödande virus, så kallade bakteriofager, påverkar i tysthet vår hälsa och livsmedelsförsörjning. Vissa orsakar dödliga infektioner, men andra kan utnyttjas för att bekämpa matburna smittämnen och födoämnesspoilering. Den här studien visar, i slående atomär detalj, hur ett sådant virus, kallat NF5, fäster sig vid och borrar igenom det tuffa yttre skalet hos en bakterie som orsakar köttfördärv. Att förstå denna mikroskopiska kamp kan hjälpa oss att utveckla säkrare sätt att bevara mat och bekämpa antibiotikaresistenta bakterier.
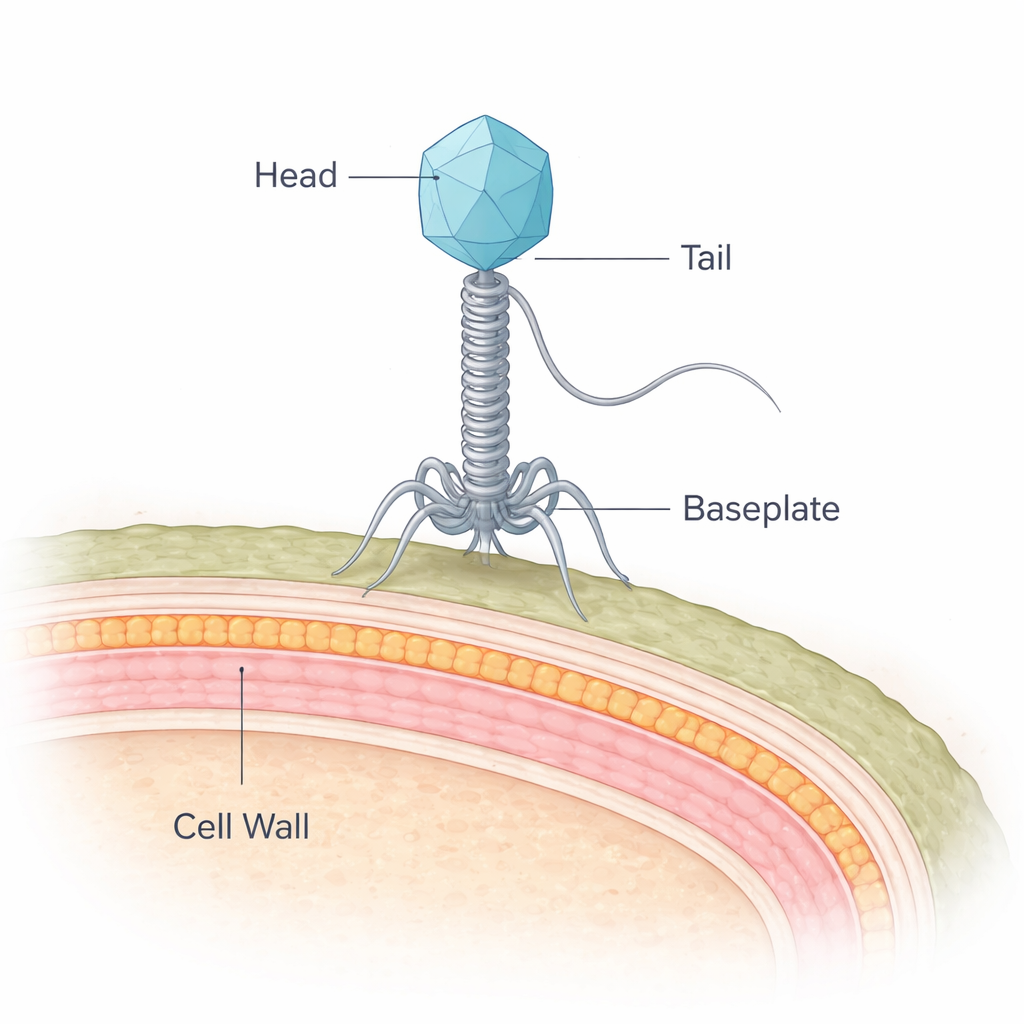
En köttfördärvare möter sin naturliga fiende
Bakterien i centrum för detta arbete, Brochothrix thermosphacta, är en vanlig bov bakom de dåliga lukter och slembildning som utvecklas på kylt kött. NF5 är ett virus som infekterar denna bakterie och tillhör en grupp som kallas siphophager, vilka bär sitt DNA i ett proteinskal och levererar det genom en lång, flexibel svans. Medan forskare har kartlagt strukturerna hos många virus som infekterar så kallade Gram-negativa bakterier, har de som riktar sig mot Gram-positiva bakterier som B. thermosphacta varit betydligt mindre väl förstådda. Gram-positiva bakterier utgör ett särskilt pussel eftersom de är skyddade av en tjock, flerskiktad cellvägg snarare än en tunn vägg och ett yttre membran.
Bygger en molekylär spruta, atom för atom
Med hjälp av toppmodern kryo-elektronmikroskopi frös forskarna miljoner NF5-partiklar och rekonstruerade deras tredimensionella struktur med närapå atomär upplösning. De identifierade 11 olika virusproteiner som tillsammans bygger det virala huvudet, nacken, tailröret och en invecklad basplatta vid svansspetsen, totalt 643 proteinkedjor. Huvudet bildar ett robust ikosaedralt skal runt det virala DNA:t, medan en 135 nanometer lång svans sträcker sig nedåt som en flexibel spruta. Ringar av upprepade proteiner formar ett ihåligt tailrör vars inre yta är starkt negativt laddad—en ordning som sannolikt hjälper viruset att snabbt skjuta in sitt DNA i värden.
Den smarta borren vid svansspetsen
Den mest intrikata delen av NF5 är basplattan, en flerskiktad struktur som fungerar som sensor, borr och förankring på samma gång. Nära centrum sitter ett ”måttband”-protein som fyller tailröret och en svansassocierad lysin som stoppar röret tills infektionen börjar. Runt denna kärna finns proteiner som känner igen och greppar tag i bakterieytan. Några fungerar som fjädrande armar som kan böjas dramatiskt, vilket hjälper basplattan att luta sig och sedan slå sig fast i en vinkel vinkelrät mot cellväggen. Andra liknar fibrer funna i besläktade virus och tros binda specifika molekyler i den tjocka Gram-positiva väggen och till och med nöta bort delar av cellväggens socker‑rika nätverk. Intressant nog verkar ett NF5-sidofiberproteiner kombinera funktioner som i andra Gram-positiva virus är fördelade på flera proteiner, vilket antyder en effektiv, evolutionärt strömlinjeformad design.
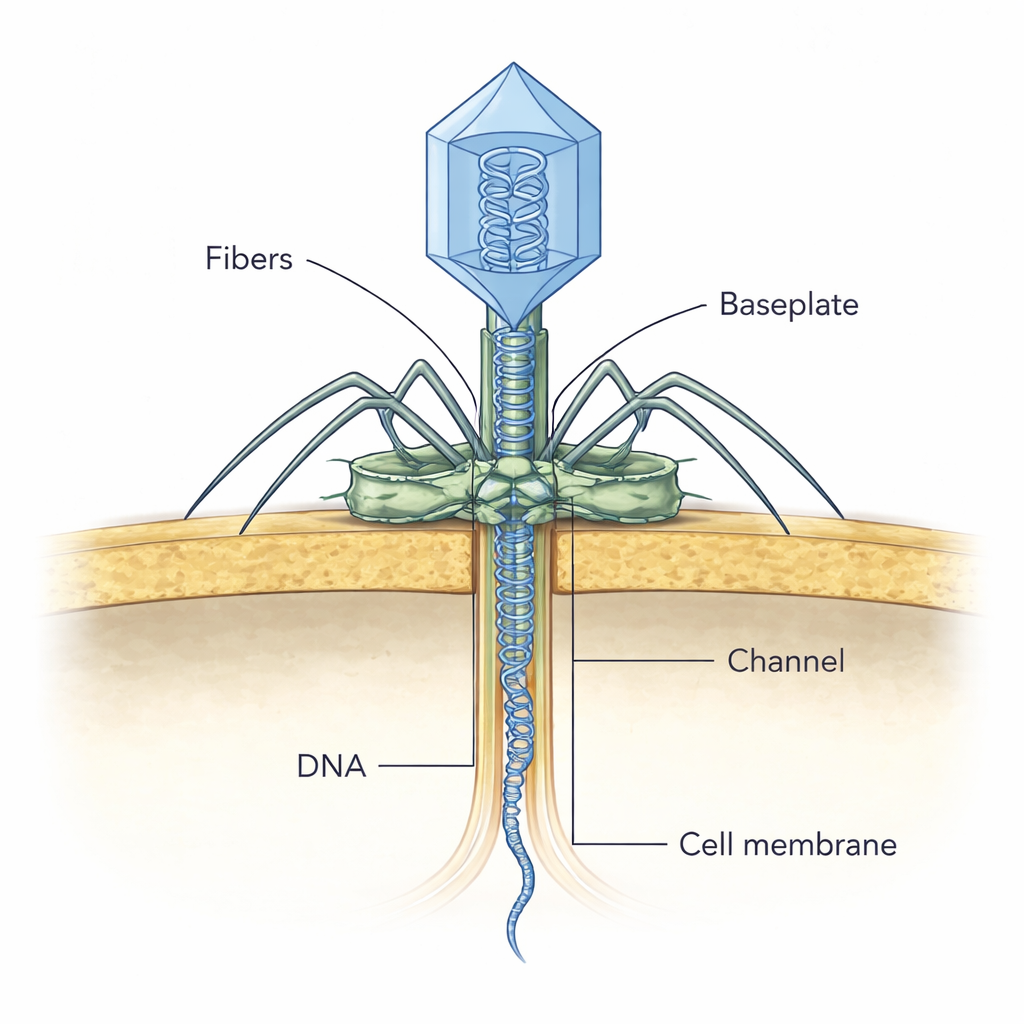
Fånga ett virus i akten
För att se hur dessa delar samverkar under infektionen använde teamet kryo-elektrontomografi på tunna skivor av infekterade bakterier. De fångade NF5-partiklar i olika till synes skeden av angrepp. I tidiga ögonblick fäster sig viruset mot cellväggen i en vinkel, sannolikt med sina yttre fibrer för att hitta lämpliga receptorer. Senare ställer basplattan in sig vinkelrätt mot cellens yta, samtidigt som det fästa virala huvudet fortfarande tycks vara fyllt med DNA. I efterföljande stadier mattas huvudets inre ut när DNA släpps ut, och en tunn, kanal-liknande densitet framträder som korsar bakterieväggen mot cellmembranet. Författarna föreslår att när enzymet i svansspetsen kommer i kontakt med och bryter ner cellväggen, omarrangeras det, pluggen öppnas och måttbandsproteinet kan skjuta ut och bilda denna tillfälliga tunnel genom vilken det virala DNA:t färdas säkert in i cellen.
Varför detta är viktigt bortom ett virus
Genom att jämföra NF5 med virus som infekterar andra bakterier visar forskarna att nyckelproteiner i svansen och basplattan har utvecklats olika hos Gram-positiva respektive Gram-negativa fager för att hantera sina värdars mycket olika ytar-arkitekturer. Dessa strukturella anpassningar—extra domäner, längre armar eller sammanlagda funktioner i enskilda proteiner—tycks vara finjusterade lösningar för tjockare, mer komplexa cellväggar. Arbetet levererar en detaljerad ritning av hur ett virus kan känna igen, fästa vid och bryta igenom en tålig bakteriebarriär, och ger en grund för att designa fager eller faginspirerade verktyg för bättre kontroll av födoämnessp spoilage och potentiellt bekämpa skadliga Gram‑positiva patogener.
Citering: Peng, Y., Pang, H., Zheng, J. et al. Structure of a Brochothrix thermosphacta bacteriophage reveals cell wall adsorption mechanism in Gram-positive infecting siphophages. Nat Commun 17, 1772 (2026). https://doi.org/10.1038/s41467-026-68477-2
Nyckelord: bakteriofagstruktur, Gram-positiva bakterier, kryo-elektronmikroskopi, kontroll av födoämnessp spoilage, faginfektionsmekanism