Clear Sky Science · sv
Identifiering av termotoleranta icke-kanoniska PAM:ar för robust ensteg CRISPR‑Cas12a‑detektion
Höjer temperaturen för DNA‑tester
Snabba, precisa tester för infektioner och genetiska förändringar är avgörande inom medicin, men dagens DNA‑tester kräver ofta komplicerad laboratorieutrustning och kan missa sällsynta eller subtila mål. Denna studie visar hur det enkla knepet att köra ett CRISPR‑baserat test något varmare öppnar upp många fler användbara DNA‑”handtag”, vilket gör en‑rörs‑diagnostik snabbare, mer känslig och kapabel att skilja även enkelbokstavsförändringar i genetiska koder. 
Varför CRISPR behöver en adress
CRISPR‑verktyg som Cas12a fungerar genom att rikta in sig mot specifika DNA‑sträckor, styrda av en kort RNA‑sekvens som fungerar som en söksträng. Men de kan bara fästa och börja verka om en intilliggande fyrbokstavs‑tagg, kallad PAM, har rätt sekvens—traditionellt en snäv uppsättning som börjar med “TTT”. Det är som att behöva ett husnummer för att kunna lämna ett brev: saknas rätt nummer kommer meddelandet aldrig fram. Detta PAM‑krav begränsar var CRISPR kan söka, vilket är en allvarlig nackdel när kliniker behöver detektera specifika mutationer, markörer för läkemedelsresistens eller virusvarianter som inte sitter intill dessa klassiska taggar.
Upptäcka nya ”dörrar” vid högre temperaturer
Forskarna testade systematiskt alla 256 möjliga fyrbokstavs‑PAM‑kombinationer för att se hur väl de drev Cas12a:s ”kollaterala” klyvningsaktivitet—dess förmåga att klippa många närliggande DNA‑stycken när det hittat sitt mål, vilket utgör grunden för CRISPR‑diagnostiksignaler. Vid normal kroppstemperatur (37 °C) presterade bara ett fåtal icke‑standard PAM:ar lika bra som de klassiska. Men när de höjde reaktionstemperaturen till cirka 45 °C hände något anmärkningsvärt: 82 olika icke‑kanoniska PAM:ar gav plötsligt stark signal‑klyvningsaktivitet, i nivå med de standardtaggarna. Teamet menar att extra värme luckrar upp den lokala DNA‑strukturen och gör Cas12a‑komplexet mer flexibelt, vilket sänker tröskeln för att känna igen dessa tidigare ”svaga” PAM:ar.
Stark signal, skonsam mot templatet
Cas12a har två klyvningslägen. I ”cis”‑läge klipper det det specifika DNA som det instruerats att hitta; i ”trans”‑läge, när det väl aktiverats, hugger det snabbt av alla närliggande signalbärande strängar, vilket lyser upp testet. Forskarna fann att vid högre temperaturer gav icke‑kanoniska PAM:ar mycket stark trans‑klyvning—bra för en klar, snabb avläsning—men höll cis‑klyvningen av huvud‑DNA:t relativt svag. Den kombinationen är idealisk för en‑rörs‑tester, där DNA först måste amplifieras utan att förstöras. De visade också att vid dessa varmare inställningar blir Cas12a mycket mer krävande vad gäller mismatch mellan guide‑RNA och mål: redan en enda fel bokstav kan stänga av signalen, särskilt vid användning av icke‑kanoniska PAM:ar. 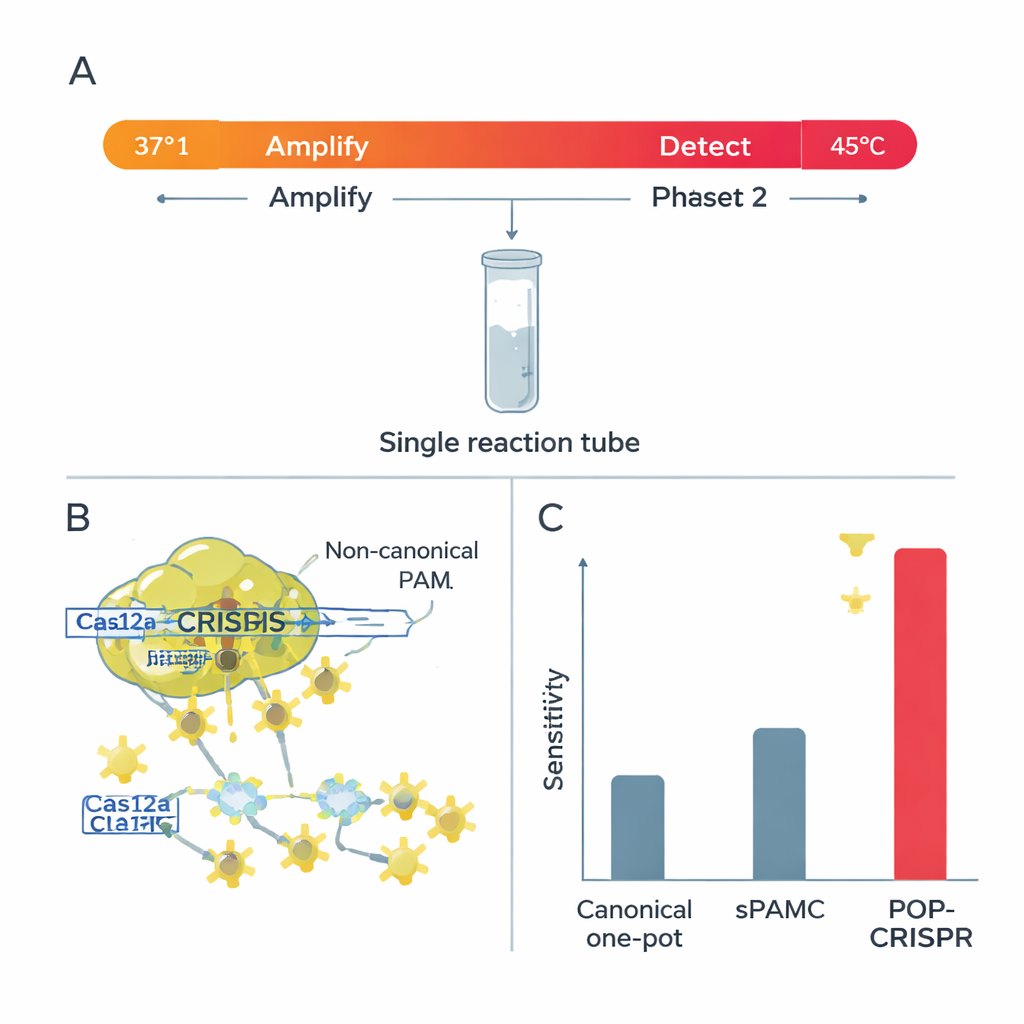
En smartare en‑rörs‑test: POP‑CRISPR
Med dessa insikter byggde teamet POP‑CRISPR, ett ”poikilotermiskt” (variabel temperatur) en‑rörsprov. Reaktionen startar runt 37 °C, där en isoterm amplifieringsmetod tyst mångfaldigar eventuellt mål‑DNA eller RNA medan Cas12a är relativt inaktiv. Efter cirka 10 minuter värms blandningen till omkring 45 °C, en optimal punkt där Cas12a—nu riktad mot icke‑kanoniska PAM‑ställen—slår på kraftfull trans‑klyvning och genererar stark fluorescenssignal. Detta enkla tvåstegs temperaturprogram ökade detektionskänsligheten ungefär tiofalt jämfört med tidigare en‑rörs CRISPR‑metoder som också använde svagare PAM:ar, och överträffade tydligt konventionella en‑rörsformat med kanoniska PAM:ar.
Från bänk till sängkant på minuter
POP‑CRISPR‑systemet testades på verkliga kliniska prover. Det detekterade känsligt humant papillomvirus (HPV‑16) i vaginala provpinnar och Mycoplasma pneumoniae i respiratoriska provpinnar, inklusive mycket låga ”gråzon”‑nivåer som utmanar standardmetoder. Avgörande var att POP‑CRISPR kunde skilja läkemedelsresistenta Mycoplasma‑stammar med en enda bokstavsändring i ett ribosomalt gen, trots att ingen klassisk PAM satt nära den mutationen—en uppgift som ställer till problem för många befintliga Cas12a‑tester. För att göra metoden fältvänlig kombinerade författarna en snabb tvåminuters värme‑ och Chelex‑lyseringssteg (som undviker fullständig DNA‑extraktion) med en handflatsstor fluorescensläsare styrd av en smartphone. Tillsammans kan detta arbetsflöde förvandla en rå provsticka till ett digitalt ja/nej‑resultat på omkring 20 minuter.
Vad detta betyder för vardagstestning
Genom att höja reaktionstemperaturen och utnyttja en mycket bredare uppsättning PAM‑”dörrar” förvandlar detta arbete Cas12a till en mer flexibel och precis sensor. POP‑CRISPR levererar snabbare, mer känslig och mer specifik nukleinsyra‑detektion i ett enda slutet rör, samtidigt som det utökar intervallet av genetiska platser som kan riktas—inklusive enkelbas‑mutationer kopplade till läkemedelsresistens eller cancer. För patienter kan det innebära snabbare punktdiagnoser och bättre anpassade behandlingar; för forskare och testutvecklare erbjuder det ett kraftfullt nytt sätt att designa CRISPR‑diagnostik som både är mer robust och mer selektiv.
Citering: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Nyckelord: CRISPR‑diagnostik, Cas12a, PAM‑ställen, point‑of‑care‑testning, nukleinsyra‑detektion