Clear Sky Science · sv
Strukturella mekanismer för hämning och aktivering av den humana småledande Ca2+-aktiverade kaliumkanalen SK2
Varför små kaliumkanaler är viktiga
Varje tanke du har och varje hjärtslag du känner bygger på elektriska signaler i dina celler. Dessa signaler formas av mikroskopiska porer, så kallade jonkanaler, som låter laddade atomer strömma in och ut. En sådan familj, de småledande kalciumaktiverade kaliumkanalerna (SK-kanaler), hjälper till att reglera hur nervceller avfyrar och hur hjärtat behåller sin rytm. Den här artikeln avslöjar, i atomär detalj, hur olika läkemedel och ett bistoxin antingen kan stänga av eller förstärka en viktig medlem i familjen, den humana SK2-kanalen — insikter som kan vägleda nya behandlingar för tillstånd som varierar från förmaksflimmer till tremor och minnessvårigheter.
Hur SK2-kanaler fungerar som cellernas broms
SK2-kanaler sitter i cellmembranet och fungerar som små bromsar för elektrisk aktivitet. När insidan av en cell tillfälligt fylls med kalciumjoner under en elektrisk signal känner ett hjälpprotein som kallas kalmodulin denna ökning. Kalmodulin är fäst vid kanalens insida och när det binder kalcium drar det i en del av kanalen som en draglina och öppnar en port som släpper ut kaliumjoner. Denna utåtriktade flöde hjälper till att dämpa cellen efter avfyrning, vilket formar hur ofta neuroner kan skicka signaler och hur tillförlitligt hjärtceller slår. Eftersom SK1–3-kanaler är vitt spridda i hjärnan och hjärtat, och SK2 är en särskilt viktig subtyp, är det avgörande för läkemedelsutveckling att förstå exakt hur de öppnas, stängs och svarar på läkemedel.
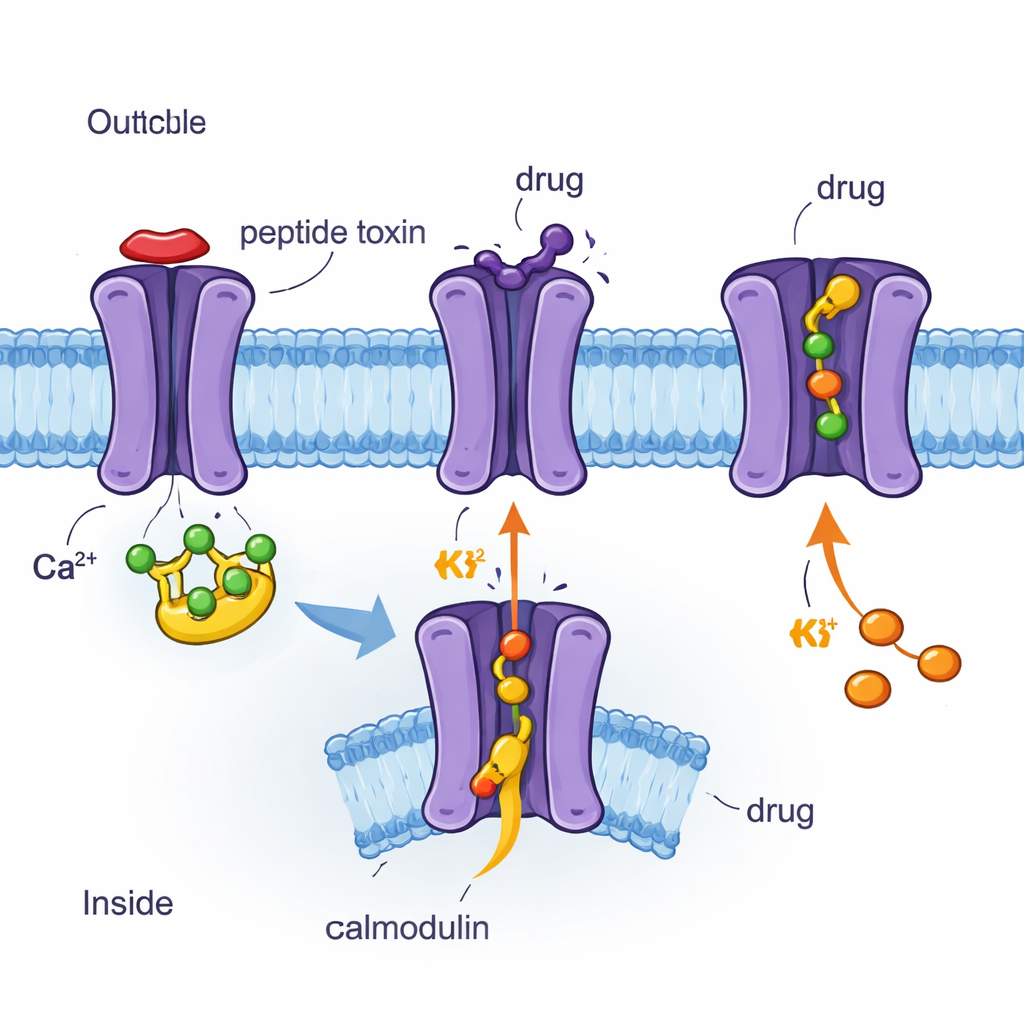
Att använda kryo‑EM för att se kanaler och läkemedel atom för atom
Forskarna använde kryoelektronmikroskopi (kryo‑EM), en teknik som avbildar snabbfrysta proteiner nära atomupplösning, för att bestämma fyra tredimensionella strukturer av den humana SK2-kanalen bunden till kalmodulin och olika molekyler. Dessa inkluderade bistoxinet apamin, den syntetiska blockaren UCL1684, den kliniska hämmaren AP30663 och den kliniska aktivatorn CAD‑1883. Alla fyra strukturer visar SK2 som en fyrdelad uppbyggnad som går igenom membranet, med kalmodulin fäst på insidan. Jämförelser mellan dessa ögonblicksbilder avslöjade vilka delar av kanalen som är stela, vilka som är flexibla och hur kalmodulin rör sig när kanalen är i ett stängt eller öppet tillstånd. Forskarna kombinerade också dessa bilder med elektriska mätningar i celler och testade hur specifika aminosyreförändringar påverkar kanalens respons på varje förening.
Ett bistoxin och ett laboratoriellt läkemedel som täpper till det yttre mynningen
Apamin, ett litet peptid från bisticksvätska, har länge varit känt som en extremt potent och selektiv SK2‑hämmare som används i forskning. De nya strukturerna visar att apamin binder som en kork på den yttre mynningen av SK2‑poren. Den lägger sig i en kupolformad vestibul som bildas av en kort slinga mellan två helixar (S3–S4‑länkaren) som är välordnad i SK2 men rörlig i en närbesläktad kanal, SK4, vilket förklarar varför SK4 är okänslig för apamin. Viktiga positivt laddade rester på apamin når mellan fyra aromatiska sidokedjor i kanalen och skapar starka elektrostatisk och staplingsinteraktioner som helt förseglar kaliumvägen. UCL1684, en syntetisk bis‑kinoliniumförening, upptar i huvudsak samma yttre ficka och blockerar också jonutgången, men dess mindre storlek låter den sitta djupare och efterlikna positionen för apamins kritiska positiva laddningar. Mutationer i kanalrester som formar denna vestibul minskar känsligheten kraftigt för apamin och, i mindre utsträckning, för UCL1684, vilket bekräftar att denna formade yttre slinga är en huvudfaktor för toxinets och läkemedlets verkan.
En central plugg och en intern kil som finjusterar aktiviteten
I kontrast binder den kliniska kandidaten AP30663 inne i SK2:s centrala kavitet, precis under selektivitetsfiltret som väljer kaliumjoner. Där fungerar den som en fysisk plugg, kilad mellan specifika sidokedjor som kantar poren. Förändringar i dessa kantande rester försvagar AP30663:s förmåga att hämma SK2, och sekvensjämförelser förklarar varför dess nära analoger kan skilja SK1–3 från SK4. CAD‑1883, en positiv modulator utvecklad för rörelsestörningar, använder en annan strategi. Den glider in i en ficka vid gränssnittet mellan kalmodulins N-lob och en kort länk (S4–S5) som kopplar kalmodulins rörelse till kanalens grind. Genom att förstärka kontakterna i denna ficka limmar CAD‑1883 effektivt ihop kalmodulin och SK2 i en konfiguration som drar upp den inre grinden och vidgar poren. Strukturella jämförelser visar att detta CAD‑1883‑bundna tillstånd liknar en fullt öppen kanal, även om selektivitetsfiltret kan anta en inaktiverad form efter långvarig öppning.
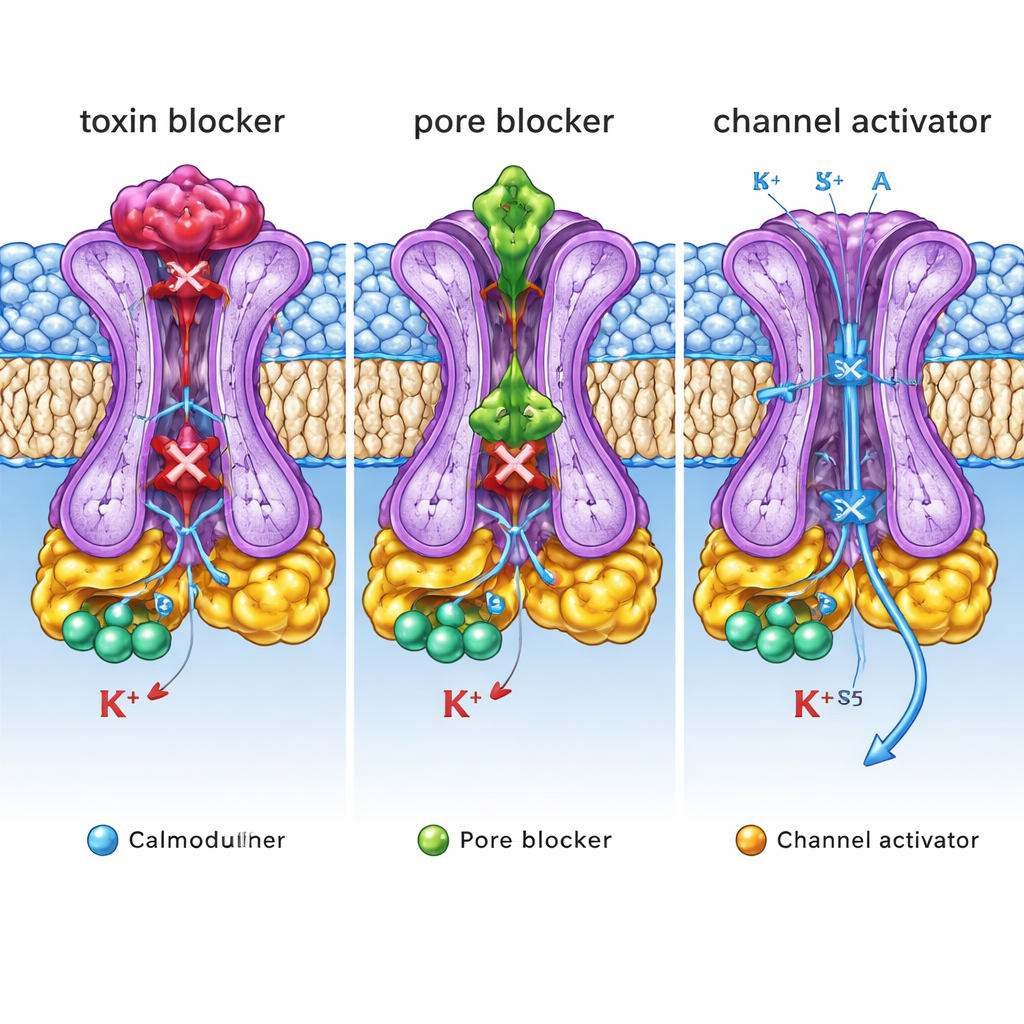
Vad dessa strukturella ritningar betyder för medicinen
Tillsammans avslöjar dessa strukturer tre distinkta “kontrollknappar” på en enda SK2‑kanal: ett yttre lock där toxiner och vissa blockare sitter, en inre porekavitet där andra hämmare stoppar flödet och en sidoficka där aktivatorer stabiliserar öppning. För en icke‑specialist är huvudbudskapet att samma jonkanal kan finjusteras uppåt eller nedåt av läkemedel som greppar mycket olika strukturella handtag. Genom att kartlägga dessa handtag med atomär precision och koppla dem till funktionella effekter ger detta arbete en detaljerad ritning för att designa nästa generations molekyler som selektivt dämpar eller förstärker SK2‑aktivitet. Sådana skräddarsydda läkemedel skulle en dag kunna hjälpa till att normalisera onormala hjärtrytmer, lindra tremor eller korrigera oregelbundna hjärtslag med färre biverkningar.
Citering: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Nyckelord: SK2-kaliumkanaler, kalciumaktiverade kanaler, kryo-EM-strukturer, jonkanalmodulatorer, förmaksflimmer och tremor