Clear Sky Science · sv
Nedsatt stamcellsrörelse och celldelning vid Duchennes muskeldystrofi avslöjad med levande avbildning
Varför den här muskelföreställningen är viktig
Duchennes muskeldystrofi (DMD) är en dödlig barndomssjukdom som gradvis förstör muskler. Under årtionden har det mesta forskningsfokus legat på de stora muskelfibrerna som bryts ner vid DMD. Denna studie visar att en annan, tystare aktör också är i bekymmer: muskelns egna stamceller, som normalt reparerar skador. Genom att följa dessa celler live inne i musmuskler och på enskilda fibrer visar författarna hur stamceller i DMD tappar orienteringen, vilket ger nya idéer för behandlingar som skulle kunna hjälpa muskler att regenerera mer effektivt.
Muskelns inbyggda reparationsstyrka
Varje skelettmuskelfiber flankeras av ett fåtal residenta stamceller, kända som muskel-satellitceller. I frisk muskel sover dessa celler större delen av tiden. När skada uppstår vaknar de, delar sig och antingen bildar nya stamceller för att fylla på reserven eller ger upphov till specialiserade celler som fusionerar med skadade fibrer. Denna noggranna balans mellan självförnyelse och differentiering håller muskelvävnad stark över en livstid. I DMD slits däremot muskelfibrerna upprepade gånger eftersom de saknar dystrofin, ett viktigt strukturellt protein, vilket väcker frågan om reparationsstyrkan själv blir uttömd eller felkalibrerad.
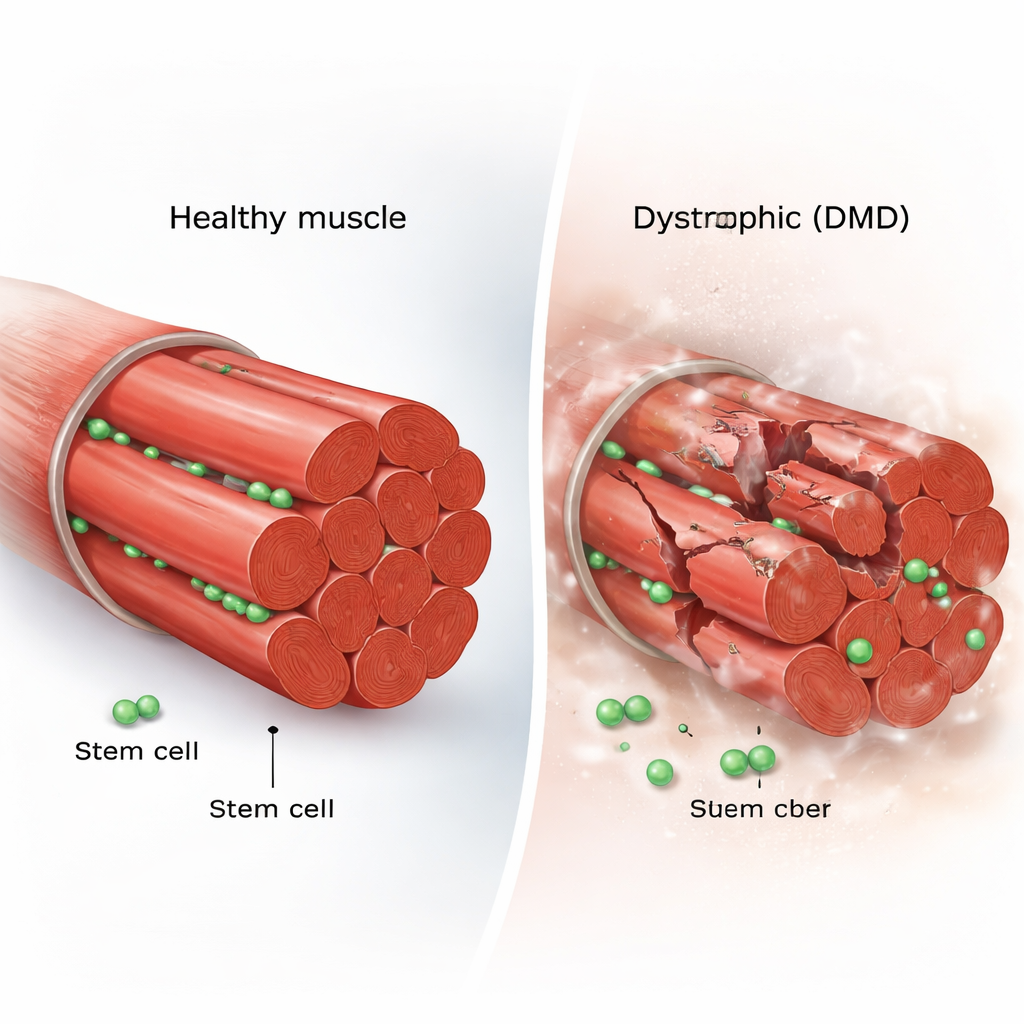
Filma stamceller i arbete
För att svara på detta använde forskarna mdx-musen, en standardmodell för DMD, och konstruerade dess muskelstamceller så att de lyste under mikroskopet. De utförde sedan intravital avbildning, en teknik som låter forskare filma levande celler inuti ett sövt djur under många timmar. De utvecklade också ett specialbyggt ”mikrobrunnssystem” för att hålla enskilda muskelfibrer i kultur samtidigt som varje stamcellsdelning och rörelse spårades. Denna dubbla metod gjorde det möjligt att följa enskilda celler från lugn vila genom upprepade delningar, migrationer och slutligen fusion in i ny muskel, och fånga beteenden som statiska ögonblicksbilder lätt kan missa.
När reparationsceller skyndar och snubblar
I skadade friska muskler förlängdes stamcells‑härledda myogena celler och kröp längs fibrerna med relativt raka, riktade banor, delade sig och spred sig effektivt. I kontrast blev dystrofiska (mdx) celler ofta runda och segare. De rörde sig långsammare och med mindre riktning, och en märkbar andel förblev nästan orörliga. Teamet fann också att mdx-celler fusionerade in i nya muskelfibrer tidigare än normalt, och många dotterceller migrerade tillsammans istället för att separera efter delning. Sammantaget visade mdx-muskler tecken på "för tidig differentiering": stamcellerna skyndade in i att bli muskelceller och bilda fibrer, i stället för att bibehålla en robust reserv för fortsatt reparation.
Obalanserade celldelningar och ett förvirrat grannskap
På isolerade fibrer kunde forskarna klassificera hur varje stamcell delade sig. I friska muskler var de flesta delningar symmetriska men balanserade—många gav upphov till två prolifererande döttrar som kunde fortsätta utöka reparationsreserven, och färre gav upphov till två terminalt differentierade celler. Asymmetriska delningar, där en dotter förblev en stamcell och den andra gick vidare för att reparera, var relativt sällsynta men förekom. I mdx-muskler försköts mönstret dramatiskt: de symmetriska delningarna lutade mot att producera två differentierande celler, med betydligt färre delningar som genererade två förnyande celler. Korstransplanteringsexperiment, där friska stamceller placerades på dystrofiska fibrer och vice versa, visade att migrationsdefekter till stor del bestämdes av den skadade fiber-miljön, medan den överdrivet differentierande beteendet hos mdx-stamceller följde cellerna själva, format delvis av deras inflammatoriska historia.
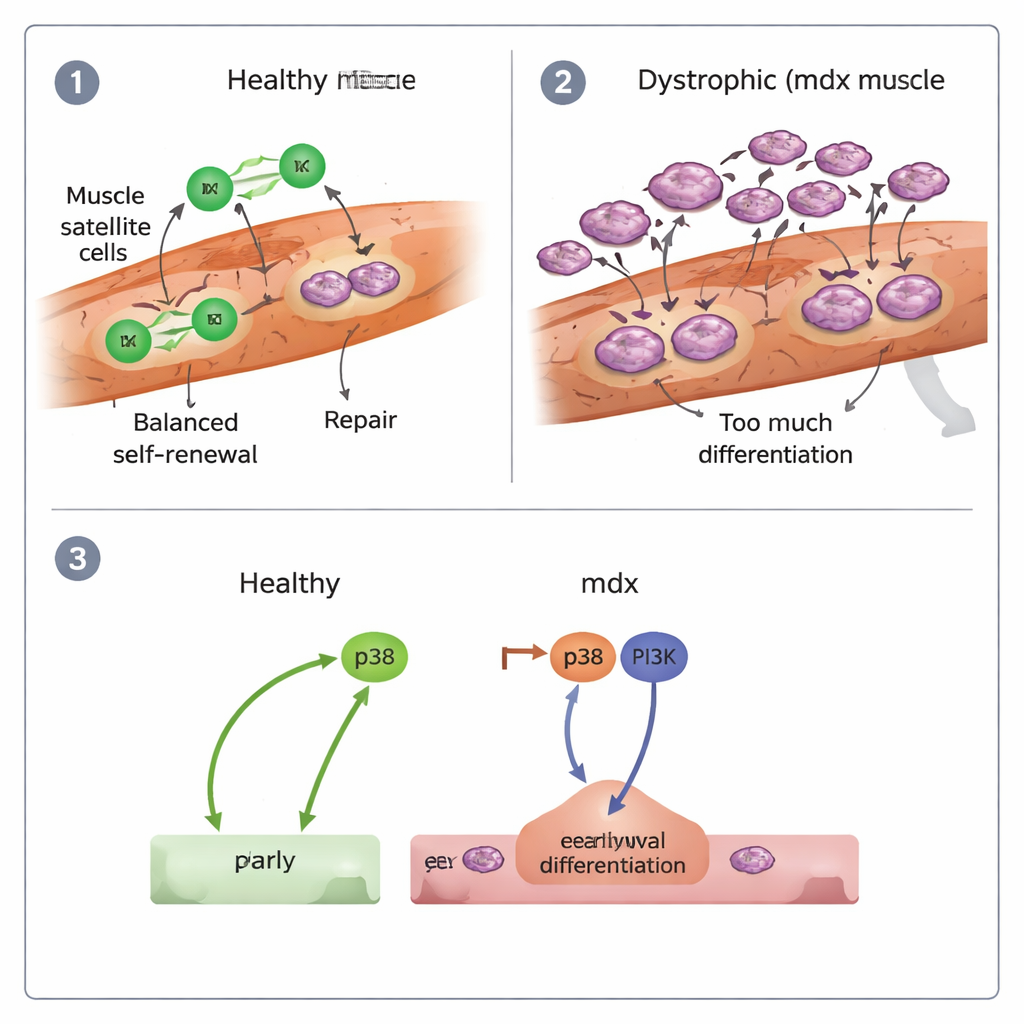
Felkopplade signaler och vad det innebär för terapi
Författarna undersökte också de molekylära omkopplare som driver stamceller att differentiera. De fokuserade på två signalvägar, kända som p38 och PI3K. I friska celler minskade blockad av p38 starkt differentieringen, medan hämning av PI3K hade liten effekt. I mdx-celler krävdes däremot att båda vägarna blockerades tillsammans för att dämpa den överdrivna rusningen mot specialisering, och även då förblev deras förmåga att fortsätta proliferera svag. Detta tyder på att DMD-stamceller drivs in i en "tidig utslitning" av kombinerad p38- och PI3K-aktivitet, vilket bidrar till en regeneration som startar snabbt men inte kan upprätthållas.
En ny syn på Duchenne: också en stamcellssjukdom
För en lekmannaläsare är huvudbudskapet att DMD inte bara är ett problem med sköra muskelfibrer; det är också ett problem med reparationssystemet som ska åtgärda dem. I dystrofisk muskel rör sig stamceller mindre effektivt, delar sig på ett sätt som tömmer reserven och svarar onormalt på viktiga tillväxtsignaler. Genom att peka ut vilka aspekter som orsakas av den skadade muskelmiljön och vilka som ligger inbyggda i stamcellernas förändrade tillstånd, antyder detta arbete nya strategier: behandlingar som dämpar p38- och PI3K‑signalering, återställer balanserade celldelningar eller förbättrar den lokala nischen skulle kunna hjälpa till att bygga upp muskler mer effektivt och förlänga nyttan av gen‑ eller cellbaserade terapier för personer som lever med Duchennes muskeldystrofi.
Citering: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
Nyckelord: Duchennes muskeldystrofi, muskelstamceller, cellmigration, stamcellsdelning, regenerativ medicin