Clear Sky Science · sv
Koiled-coil-heterodimer‑medierade delade basredigeringssystem möjliggör flexibla och robusta nukleotidsubstitutioner
Att laga DNA med färre biverkningar
Många sjukdomar orsakas av små stavfel i vårt DNA — enkelbokstavsfel som kan få livshotande konsekvenser. Forskare har kraftfulla verktyg, kallade basredigerare, som kan rätta dessa fel utan att klippa i DNA:t, men dessa verktyg är skrymmande och svåra att leverera säkert in i kroppen. Denna artikel introducerar ett nytt sätt att dela upp basredigerare i mindre, smartare delar som ändå fungerar lika bra — eller till och med bättre — än originalet, vilket öppnar nya vägar för behandling av genetiska sjukdomar i levern, musklerna och bortom.
Varför storleken är ett problem för genfixningsverktyg
Basredigerare kombinerar delar av CRISPR‑systemet med enzymer som kan byta ut en DNA‑bokstav mot en annan, till exempel genom att ändra ett A till G eller ett C till T. Dessa precisa byten är lovande för att behandla tillstånd som högt kolesterol eller muskulär dystrofi. En ledande leveransmetod för genterapi, adeno‑associated virus (AAV), kan dock bara bära omkring 4,7 tusen DNA‑bokstäver, medan standardbasredigerare är större än så. Tidigare försök att dela dessa redigerare använde särskilda protein"saxar" kallade inteiner, eller genom att förminska dem med kompaktare enzymer, men dessa tillvägagångssätt minskade ofta effektiviteten, lade till designkomplexitet eller begränsade var i genomet verktygen kunde verka.
Använda molekylärt kardborreband för att återskapa redigeraren
För att lösa detta designade forskarna en "delad" basredigerare som hålls samman av små proteinzippar kända som koiled‑coil‑heterodimerer — som ett stycke molekylärt kardborreband. De separerade basredigeraren i två delar: en som bär DNA‑målande Cas9‑nickas och en annan som bär redigeringsenzymet. Korta koiled‑coil‑peptider på varje halva söker efter varandra och snappar ihop när båda når samma DNA‑sekvens. Detta skapar koiled‑coil‑basredigerare (CC‑BEs), inklusive varianter som redigerar C (CC‑CBE), A (CC‑ABE) och mer komplexa varianter som kan göra olika slags bokstavsbyten. 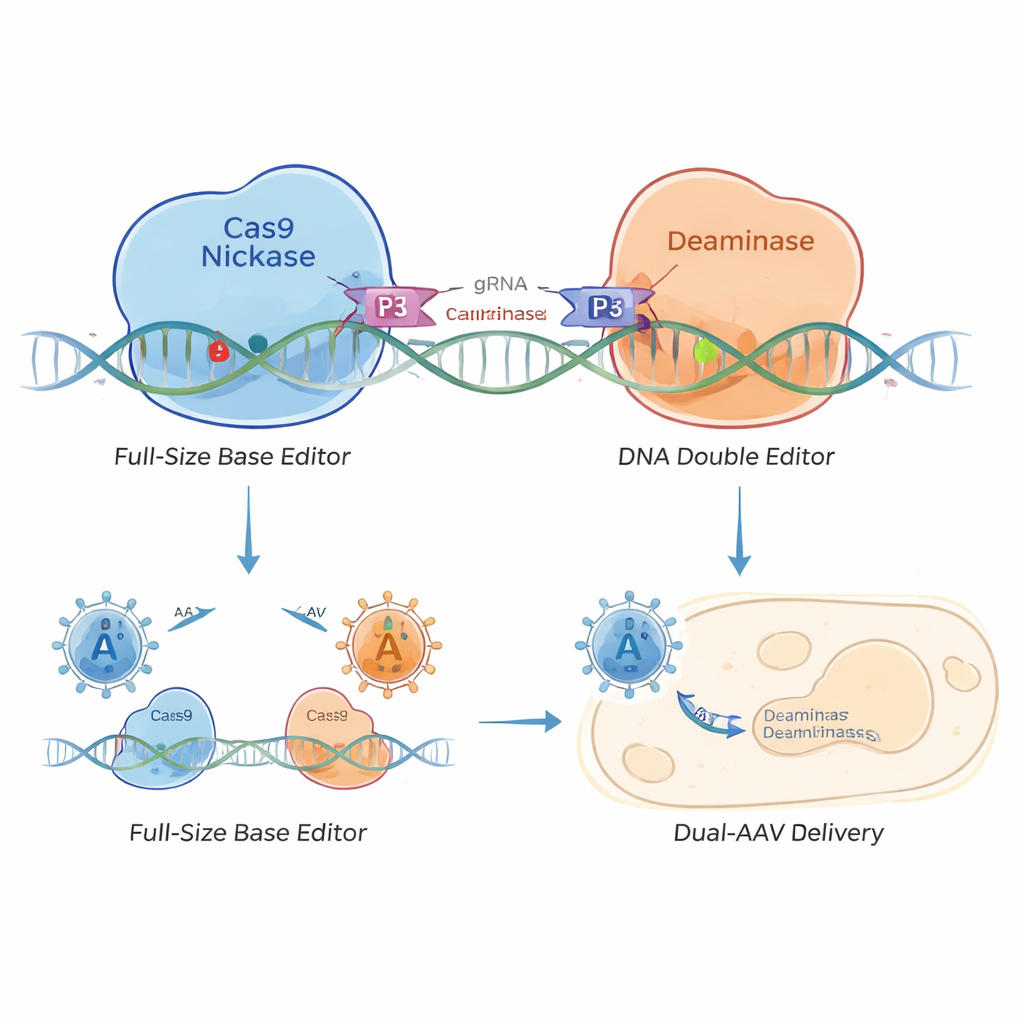
Flexibel, kraftfull och precis redigering
Teamet testade CC‑BEs i flera celltyper, inklusive humana celler och primära griseceller, och med olika former av Cas9 som känner igen ett bredare spektrum av DNA‑sekvenser. CC‑CBE‑varianterna fungerade inte bara pålitligt på många ställen utan visade också ett bredare "redigeringsfönster", vilket betyder att de kunde förändra målade bokstäver över ett större DNA‑utrymme och därmed ge forskare större flexibilitet vid val av guide‑RNA. CC‑ABE‑varianterna nådde liknande effektivitet som de bästa befintliga adeninredigerarna samtidigt som de ofta producerade färre oönskade biprodukter. Forskarna anpassade också koiled‑coil‑strategin till nyare redigeringsdesigner — såsom kompakta TadCBE och precisa ABE9 — och fann återigen att delning av verktygen med koiled‑coil‑par bevarade eller förbättrade prestandan.
Från cellodlingar till levande möss
Avgörande visade författarna att dessa delade redigerare fungerar i levande djur med hjälp av dubbel‑AAV‑leverans, där varje viruspartikel bär hälften av redigeraren. I möss uppnådde en CC‑ABE som riktade Pcsk9‑genen i levern A‑till‑G‑redigeringar i nivåer upp till cirka 70 %, vilket kraftigt sänkte Pcsk9‑protein och blodets LDL‑kolesterol utan tecken på leverskada. 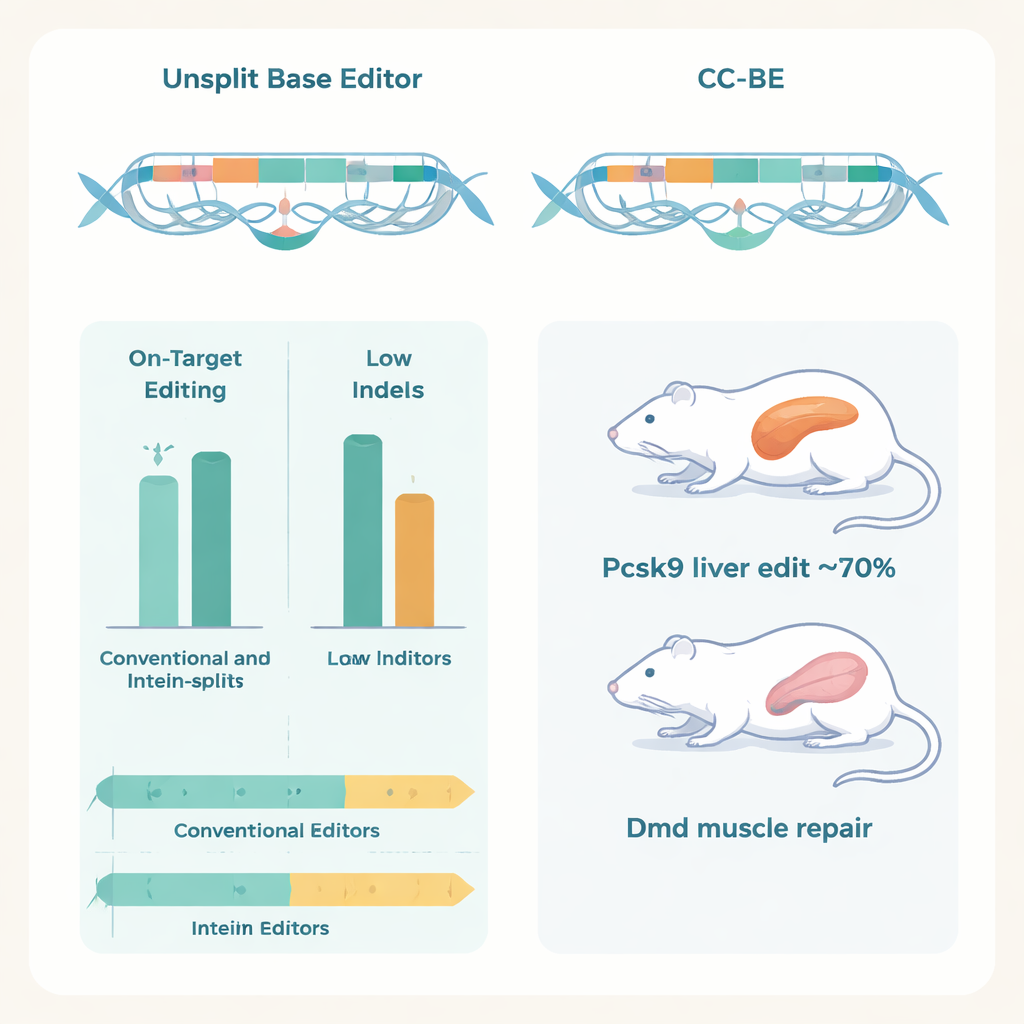
En ny väg mot praktisk DNA‑reparation
I grunden presenterar denna studie ett enkelt men kraftfullt ingenjörstrick: använd små koiled‑coil "krokar" för att dela stora basredigerare i AAV‑stora moduler som återförenas endast där de behövs. För icke‑experter är slutsatsen att forskare nu kan paketera mycket kapabla DNA‑reparationsverktyg i kliniskt beprövade virala bärare utan att offra noggrannhet eller kraft. Denna koiled‑coil‑metod kan göra det lättare att utforma behandlingar för ett brett spektrum enkla‑bokstavs‑genetiska sjukdomar i organ som lever, hjärta och muskler, och därigenom föra finkalibrerad genkorrigering ett steg närmare verklig klinisk användning.
Citering: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Nyckelord: basredigering, genterapi, CRISPR, AAV‑leverans, genetisk sjukdom