Clear Sky Science · sv
In vivo CRISPR-screening identifierar SAGA-komplexets medlemmar som nyckelregulatorer av hematopoes
Varför det är viktigt att hålla blodproduktionen i balans
Varje dag tillverkar din kropp tyst hundratals miljarder nya blodceller som transporterar syre, bekämpar infektioner och stoppar blödningar. Denna ständiga produktion är beroende av sällsynta ”moder”celler i benmärgen, kallade blodbildande stamceller. När mekanismerna som styr dessa celler går fel kan människor drabbas av anemi, försvagat immunförsvar eller cancerformer som leukemi. Denna studie ställer en enkel men kraftfull fråga: bland de tusentals generna i vårt genom, vilka är verkligen nödvändiga för att hålla blodcellsproduktionen frisk och i balans?
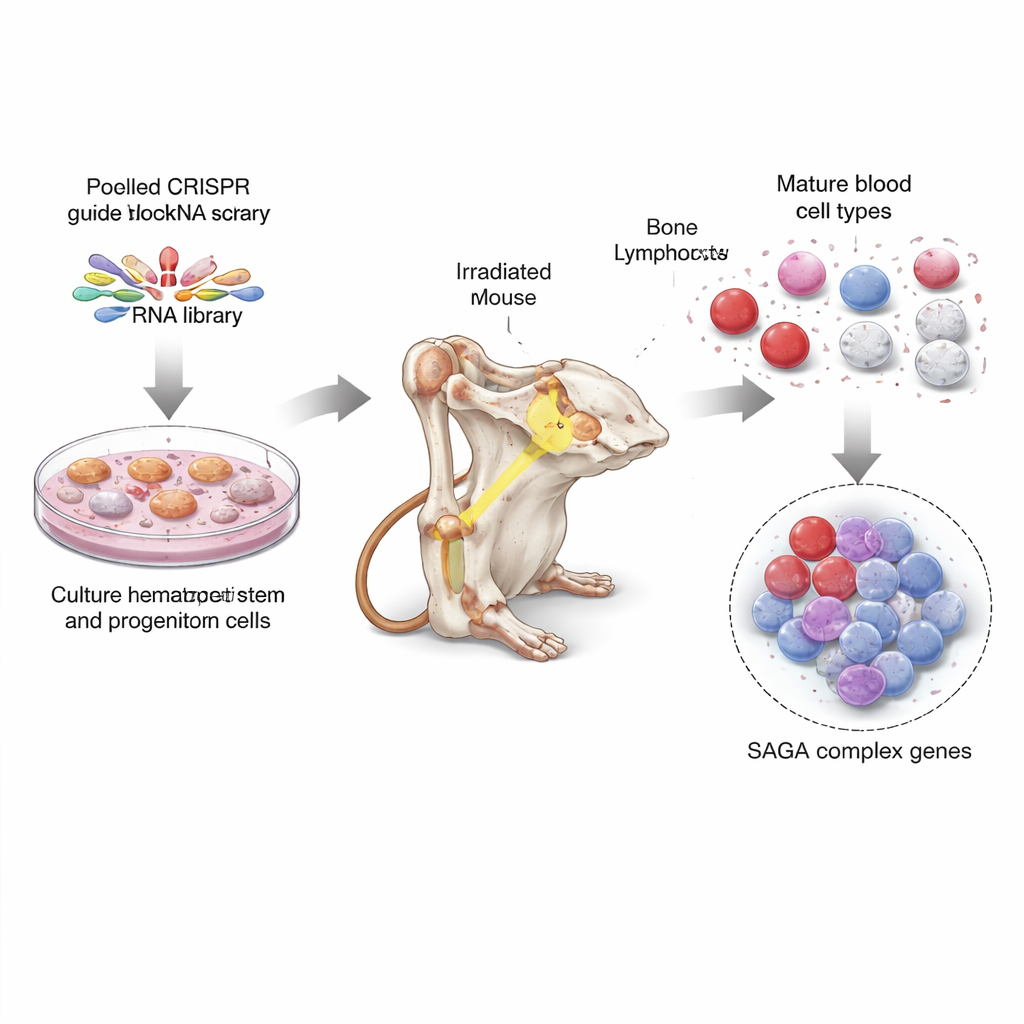
En genomsökning över hela genomet i musstamceller
För att angripa frågan använde forskarna CRISPR, det genredigeringsverktyg som ofta liknas vid molekylära saxar, för att stänga av nästan varje gen i musegenomet, tio guider per gen. De odlade först stora mängder benmärgsstam- och progenitorceller i särskilda odlingsförhållanden och infekterade sedan dessa celler med poolade CRISPR-guider så att varje cell bar en knockout av en annan gen. Därefter transplanterade de dessa blandade, redigerade celler i dussintals bestrålade möss och lät de redigerade cellerna bygga upp djurens blodsystem. Månader senare renade de olika mogna blodcellstyper och stamcells‑lika celler från benmärgen och läste av vilka CRISPR-guider som var över‑ eller underrepresenterade. Detta avslöjade vilka genförluster som gynnade omogna celler och vilka som stödde produktionen av fullt utvecklade blodceller.
En dold kontrollcentral kallad SAGA framträder
Bland många kända regulatorer av blodbildning dök ett överraskande set träffar upp: flera strukturella delar av en stor proteinassembly kallad SAGA-komplexet, inklusive gener med namnen Tada2b, Taf5l och Tada1. SAGA tillverkar inte blodceller direkt; istället hjälper det till att slå på eller av andra gener genom att kemiskt märka DNA‑paketerande proteiner kallade histoner. När teamet individuellt slog ut dessa SAGA-komponenter och transplanterade de redigerade cellerna i möss, såg de ett konsekvent mönster. Omogna benmärgsceller samlades i mängd, men deras förmåga att mogna till cirkulerande vita blodkroppar, röda blodkroppar och vissa immunceller minskade kraftigt. I huvudsak fastnade stam‑ och progenitorcellerna i en flaskhals och kunde inte slutföra resan till fullt funktionella blodceller.
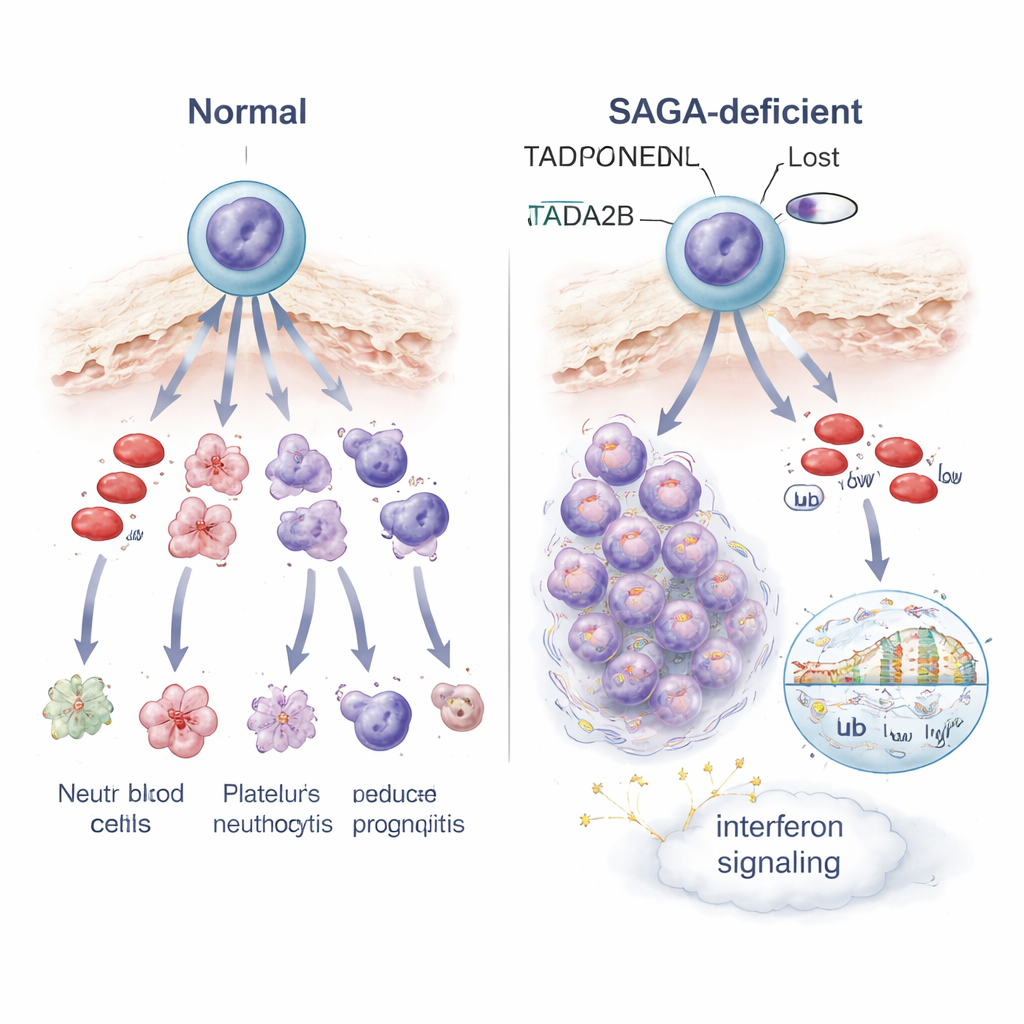
Hur störd genkontroll förändrar cellöde och stressignaler
För att förstå vad som går fel inne i dessa blockerade celler profilerade forskarna genaktivitet en cell i taget och i bulk. Förlust av Tada2b eller Taf5l omkopplade aktiviteten hos många gener i stamceller, med två slående teman. För det första aktiverades gener involverade i interferonsvar — normalt en del av kroppens antivirala försvar — vilket indikerar ett internt larm eller stressläge. För det andra blev cellernas mitokondrier, de små kraftverken som driver cellens arbete, mindre aktiva, och de förändrade cellerna blev mer känsliga för ett läkemedel som riktar sig mot mitokondriell energisproduktion. På nivån av DNA‑packetering visade celler som saknade Tada2b reducerade nivåer av en histonmarkör kopplad till öppet, aktivt kromatin, samt förändringar i en annan markör som påverkar hur gener läses. Dessa skift i kromatinkemi förklarar sannolikt varför många gener, inklusive de som styr korrekt blodmognad, blir felreglerade.
Från grundläggande mekanismer till sjukdomsmodeller
Teamet frågade sedan om att höja eller sänka SAGA‑aktiviteten kunde vända dessa effekter. Att tvinga celler att producera extra Tada2b sänkte interferonrelaterad genaktivitet och minskade andelen stamliknande celler, den spegelvända effekten av knockouten. Behandling av normala stamceller med ett läkemedel som hämmar SAGAs centrala enzymatiska underenheter reproducerade stora delar av Tada2b‑förlustens signatur, vilket förstärker idén att SAGAs kromatinmodifierande aktivitet är central för dess roll. Slutligen vände sig forskarna till en human cellmodell av myelodysplastiskt syndrom, en för‑leukemisk sjukdom där blodproduktionen sviktar och interferonvägar ofta är uppreglerade. När de slog ut SAGA‑komponenter i dessa humana celler och transplanterade dem i immundefekta möss fick de redigerade cellerna en tillväxtfördel och aktiverade återigen interferon‑ och myeloida genprogram, vilket tyder på att denna regleringsnod också formar sjukdomsbeteende.
Vad detta betyder för blodhälsa och framtida terapier
För en lekman är kärnbudskapet att denna studie avslöjar en kraftfull kontrollcentral — SAGA‑komplexet — som hjälper blodbildande stamceller att avgöra när de ska förbli omogna, när de ska mogna och hur de ska undvika skadliga stressresponser. När viktiga SAGA‑delar försvinner ackumuleras stamceller men misslyckas med att producera tillräckligt många fungerande blodceller, samtidigt som stress‑ och antivirala‑lika signaler ökar och mitokondrier sviktar. Dessa upptäckter fördjupar inte bara vår förståelse för hur hälsosam blodproduktion upprätthålls under livet, utan antyder också att subtila förändringar i SAGA‑aktivitet kan bidra till åldersrelaterade blodproblem och störningar som myelodysplastiskt syndrom. I längden kan kartläggningen av denna kontrollkrets hjälpa forskare att utforma terapier som knuffar felande stamceller tillbaka mot en balanserad, motståndskraftig blodproduktion.
Citering: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Nyckelord: hematopoetiska stamceller, CRISPR-screening, SAGA-komplexet, interferonsvar, myelodysplastiskt syndrom