Clear Sky Science · sv
Sluta ut kromatinarkitektur vid en enskild locus genom probabilistisk in situ-DNA-lokalisering
Hur DNAs tredimensionella form styr när gener slås på
Vår DNA avbildas ofta som en rak stege, men inne i celler veckas den till invecklade slingor och spolar. Dessa former spelar roll: de hjälper bestämma vilka gener som slås på, när och var. I denna studie presenteras ett nytt sätt att betrakta de mikroskopiska 3D-arrangemangen av DNA kring en enskild gen i utvecklande bananflugeembryon, vilket avslöjar hur subtila förändringar i DNA-veckning kan ändra mönster av genaktivitet som formar kroppens plan.
Att iaktta genreglering i ett utvecklande embryo
När ett embryo utvecklas måste tusentals gener slås på och av vid precis rätt tidpunkter. Många av dessa beslut styrs av korta DNA-regioner kallade enhancers, som kan ligga tiotusentals baspar bort från de gener de kontrollerar. För att fungera måste enhancers fysiskt komma i närhet till sin målgene i 3D-utrymmet genom att DNA-loopas så att avlägsna platser berör varandra. Men dessa slingor är små, dynamiska och svåra att se. Författarna fokuserade på en enskild gen, brinker (brk), i bananflugan Drosophila. Denna gen hjälper till att mönstra det tidiga embryot och slås på i en rand längs sidan av ägget. Tre närliggande DNA-kontrollelement—två enhancers (E1 och E2) och ett promoter-proximalt element (PPE) intill genen—samarbetar för att ge upphov till detta precisa mönster.
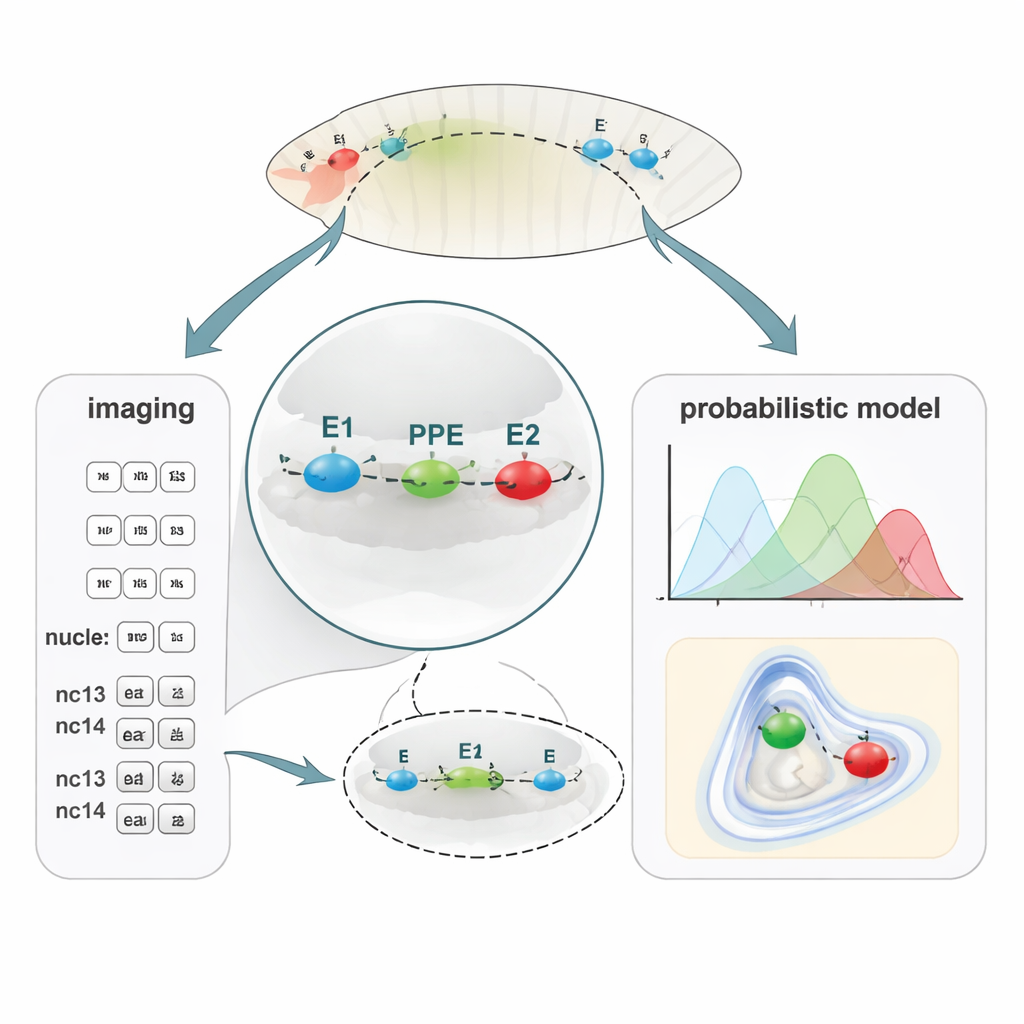
En ny metod för att kartlägga mikroskopiska DNAvstånd
För att koppla DNA-veckning till genaktivitet utvecklade teamet PLOTTED (Probabilistic Localization of Oligopaint Tagged Target Element Distances). Först använde de en DNA-märkningsmetod kallad Oligopaint FISH för att fästa tre olika fluorescerande färgämnen vid E1-, PPE- och E2-regionerna i fixerade flugembryon. Med hjälp av ett superupplösande konfokalt mikroskop mätte de 3D-avstånd mellan dessa tre färgade prickar i tiotusentals kärnor över embryon i efterföljande kärncykler, från strax innan genaktiviteten startar (pre-nc13) genom senare stadier (nc13 och nc14). De matade sedan in alla dessa avstånd i en specialbyggd beräkningspipeline som filtrerar bort brusiga mätningar och bygger sannolikhetskartor som visar var varje element mest sannolikt sitter i förhållande till de andra. Istället för en enda statisk ”slinga” producerar PLOTTED ett landskap av sannolika kromatinformer för varje utvecklingsstadium.
När DNA komprimeras väcks genen
I normala embryon fann forskarna att när embryot når kärncykel 13 rör sig båda enhancers närmare PPE: den lokala DNA-närmiljön kring brk-genen blir mer kompakt. Efter denna punkt förblir avstånden mellan de tre elementen relativt stabila. Viktigt är att denna tidpunkt sammanfaller med starten av brk-uttrycket, vilket tyder på att åtstramningen av DNA-konfigurationen hjälper genen att slås på. PLOTTED visade också att denna kompakta ordning förekommer oftare i regioner av embryot där brk är aktivt, medan lösare konfigurationer dominerar där genen är reprimerad, vilket förstärker kopplingen mellan 3D-arkitektur och transkription.
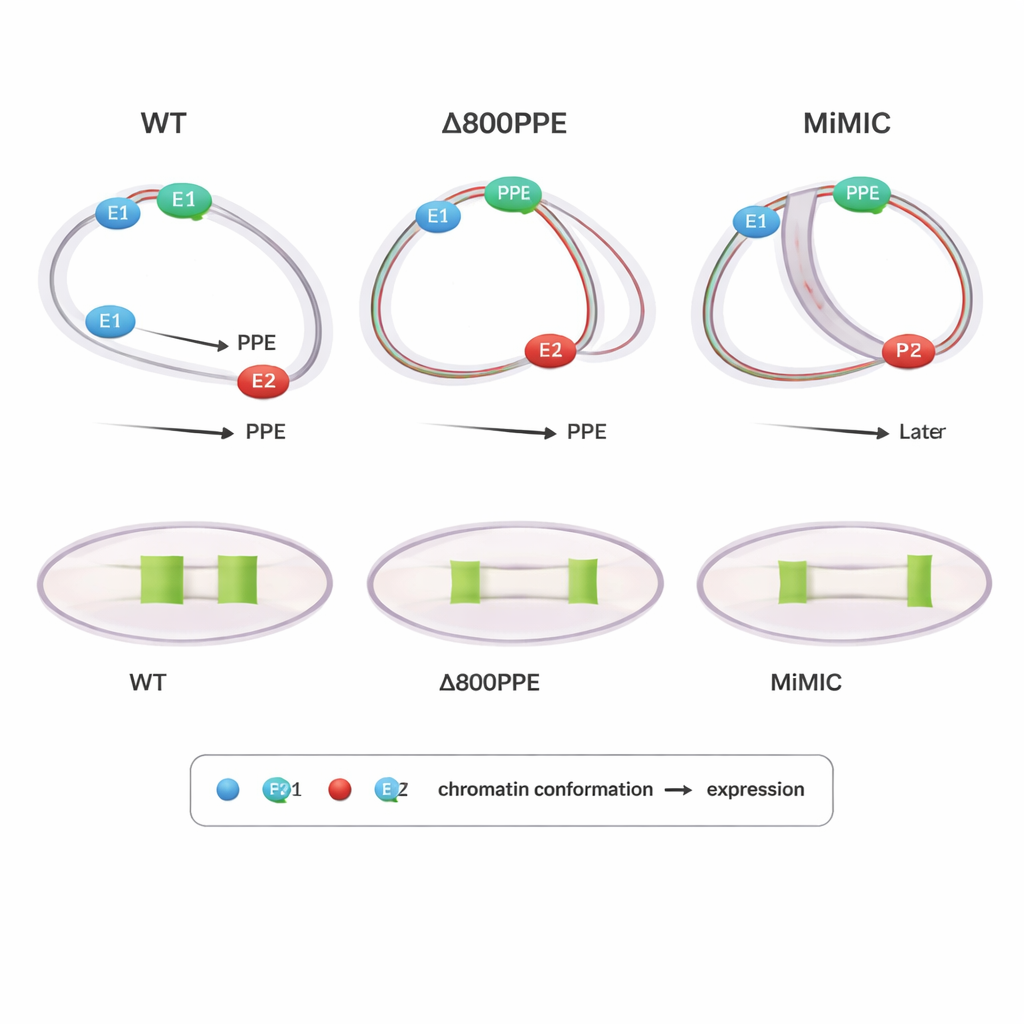
Mutationer visar hur tidpunkt och position spelar roll
För att undersöka orsak och verkan studerade författarna flugor med konstruerade förändringar vid brk-locuset. I en mutant togs 800 baspar av PPE bort, vilket försvagade detta centrala element; i en annan infogades en 7,3 kilobaspaar lång DNA-kassett (MiMIC) mellan E1 och PPE, vilket i praktiken pressade dem längre ifrån varandra och lade till en extra promotor. Båda mutanterna visade fördröjt eller minskat brk-uttryck. PLOTTED visade varför: i PPE-deletionslinjen skedde komprimeringen av avstånden mellan PPE och båda enhancers senare än normalt, och i sena stadier förblev PPE för nära E1, vilket hindrade E2 från att driva det breda uttrycksmönster som ses i vildtyp. I MiMIC-linjen associerade PPE för tidigt och för starkt med E2 och närmade sig först senare E1, vilket åter störde normal överlämning mellan enhancers. Dessa resultat antyder att det inte bara är huruvida element kommer samman utan också när och med vilken partner de är närmast som är avgörande för korrekt genuttryck.
DNA-veckning varierar över embryot
Eftersom PLOTTED bevarar rumslig information i intakta embryon kunde teamet också undersöka om DNA-arkitekturen skiljer sig åt i olika kroppsregioner. Genom att jämföra laterala zoner där brk är aktivt med ventrala zoner där det är repressoriskt fann de att de tre elementen sitter närmare varandra i aktiva regioner och sprids längre isär i reprimerade domäner. Längs huvud-till-svans-axeln observerade de att E1–PPE-avstånden förändras olika i fronten jämfört med bakdelen av embryot, vilket antyder att regionala signaler finjusterar kromatinarkitekturen för att ställa in precisa genuttrycksmönster. Dessa fynd stöder en bild där den 3D-arrangemangen av regulatoriskt DNA är kontextberoende och spårar både tid och position i det utvecklande organismen.
Varför detta är viktigt bortom bananflugor
Förenklat visar denna studie att hur DNA veckas runt en enskild gen är nära kopplat till när och var den genen slås på. Den nya PLOTTED-metoden ger ett praktiskt sätt att kartlägga dessa mikroskopiska DNA-närmiljöer i intakta vävnader med allmänt tillgängliga mikroskop och enkel kemi, kombinerat med kraftfull probabilistisk modellering. Även om metoden demonstrerats i flugembryon kan den tillämpas på många organismer och sjukdomsmodeller. När forskare alltmer upptäcker att felaktigt vikt kromatin ligger bakom utvecklingsstörningar och cancer, kommer verktyg som PLOTTED att hjälpa till att avslöja hur små skiftningar i enhancers och gens 3D-layout kan få stora följder för cellöden och hälsa.
Citering: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Nyckelord: kromatinarkitektur, enhancer-promoter-interaktioner, Drosophila-embryogenes, genreglering, superupplösningsavbildning