Clear Sky Science · sv
DKK1 och NEDD4 från neurala krestceller reglerar Wnt‑signalering i det andra hjärtfältet för att samordna utvecklingen av hjärtats utflödesbana
Varför små hjärtbyggare spelar roll
Det tidiga embryots hjärta börjar som ett enkelt rör, men måste snabbt omformas till ett komplext organ som pumpar blod både till kroppen och till lungorna. Subtila felsteg i denna byggprocess kan ge allvarliga medfödda skador, inklusive tillstånd som kräver operation strax efter födseln. Denna studie avslöjar hur två cellgrupper kommunicerar när de formar hjärtats huvudsakliga utloppsväg, och identifierar ett molekylärt fel som kan bidra till medfödda hjärtfel hos både möss och människor.
Två team som bygger hjärtats utfart
Den del av hjärtat som leder blod ut från kamrarna — utflödesbanan — bildas från en region som kallas det andra hjärtfältet. Celler här måste förbli flexibla ”progenitorer” tillräckligt länge för att kunna läggas till den växande utflödesbanan, och sedan mogna till muskel vid rätt tidpunkt. Precis intill vandrar neurala krestceller, en mobil population som hjälper till att bygga de stora artärerna och klaffarna. Tidigare arbete antydde att dessa neurala krestceller på något sätt påverkar det andra hjärtfältet, men hur denna korsprat fungerade var okänt. 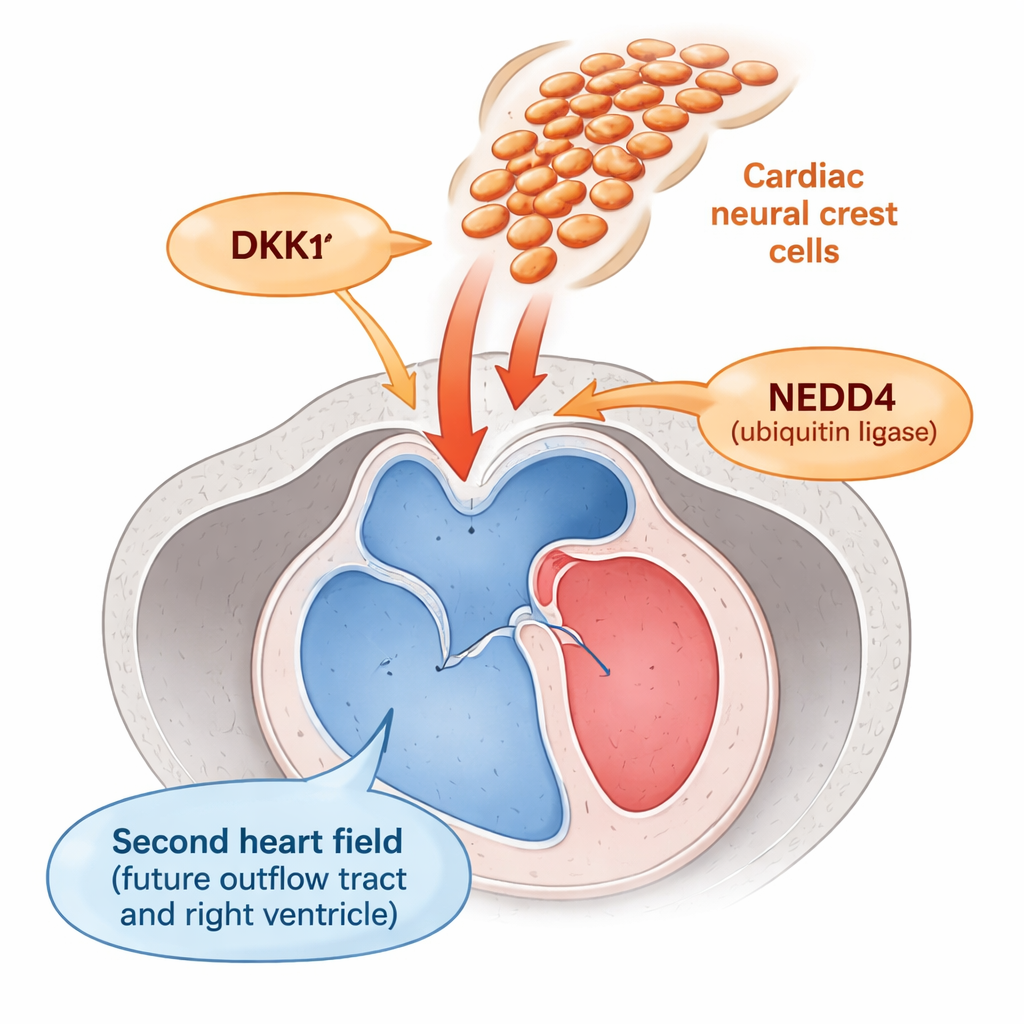
En molekylär dimmer för tillväxtsignaler
Forskarna upptäckte att neurala krestceller fungerar som en dimmer för en nyckeltillväxtsignal kallad Wnt, som håller progenitorcellerna delande och fördröjer deras mognad. De fann att neurala krestceller är en huvudkälla för DKK1, ett litet sekretoriskt protein som släcker Wnt‑signalering i närliggande celler. DKK1 hålls i sin tur normalt i schack av NEDD4, ett protein som märker DKK1 för nedbrytning. I musembryon som saknade Nedd4 specifikt i neurala krestceller, ansamlades DKK1 till onormalt höga nivåer. Det överskottet av DKK1 sänkte Wnt‑aktiviteten i det intilliggande andra hjärtfältet, vilket visades av reducerad nukleär beta‑catenin — en standardmätare för Wnt‑signalering — och lägre nivåer av flera Wnt‑responsiva gener.
När tidpunkten blir fel, misslyckas hjärtats geometri
För mycket DKK1 och för lite Wnt fick en tydlig följd: cellerna i det andra hjärtfältet började differentiera till hjärtmuskel för tidigt. Markörer för mogen muskel dök upp tidigt i detta progenitorområde, och färre odifferentierade celler fanns kvar för att förlänga utflödesbanan. Genom att följa delande celler över tid visade teamet att färre andra hjärtfältsceller lades till i utflödesbanan hos mutanterna. Som ett resultat var utflödesbanan kortare och roterad felaktigt, vilket ledde till missanpassning mellan de stora artärerna och kamrarna. Dessa strukturella fel liknade mänskliga konotruncala defekter såsom double‑outlet right ventricle och närliggande missbildningar som setts i fullständiga Nedd4‑knockoutmöss.
Bevisa signalens roll och en koppling till mänsklig sjukdom
För att bekräfta att förändrad Wnt‑signalering verkligen orsakade problemen, rubbade forskarna banan med läkemedel hos dräktiga möss. Att blockera Wnt i annars friska embryon drev dem mot samma för tidiga differentiering och rotationsfel som sågs vid förlust av Nedd4, medan minskad Dkk1‑genmängd i Nedd4‑defekta bakgrunden delvis räddade både utflödesbanans storlek och rotation. Slutligen identifierade teamet ett barn med Fallots tetrad som bar en sällsynt ärftlig förändring i NEDD4 som försvagade dess förmåga att märka DKK1 för nedbrytning. Möss konstruerade för att bära samma Nedd4‑variant utvecklade högersidiga vägg‑ och septala hjärtfel, vilket stöder idén att bristfällig NEDD4–DKK1‑kontroll kan bidra till mänskliga medfödda hjärtfel. 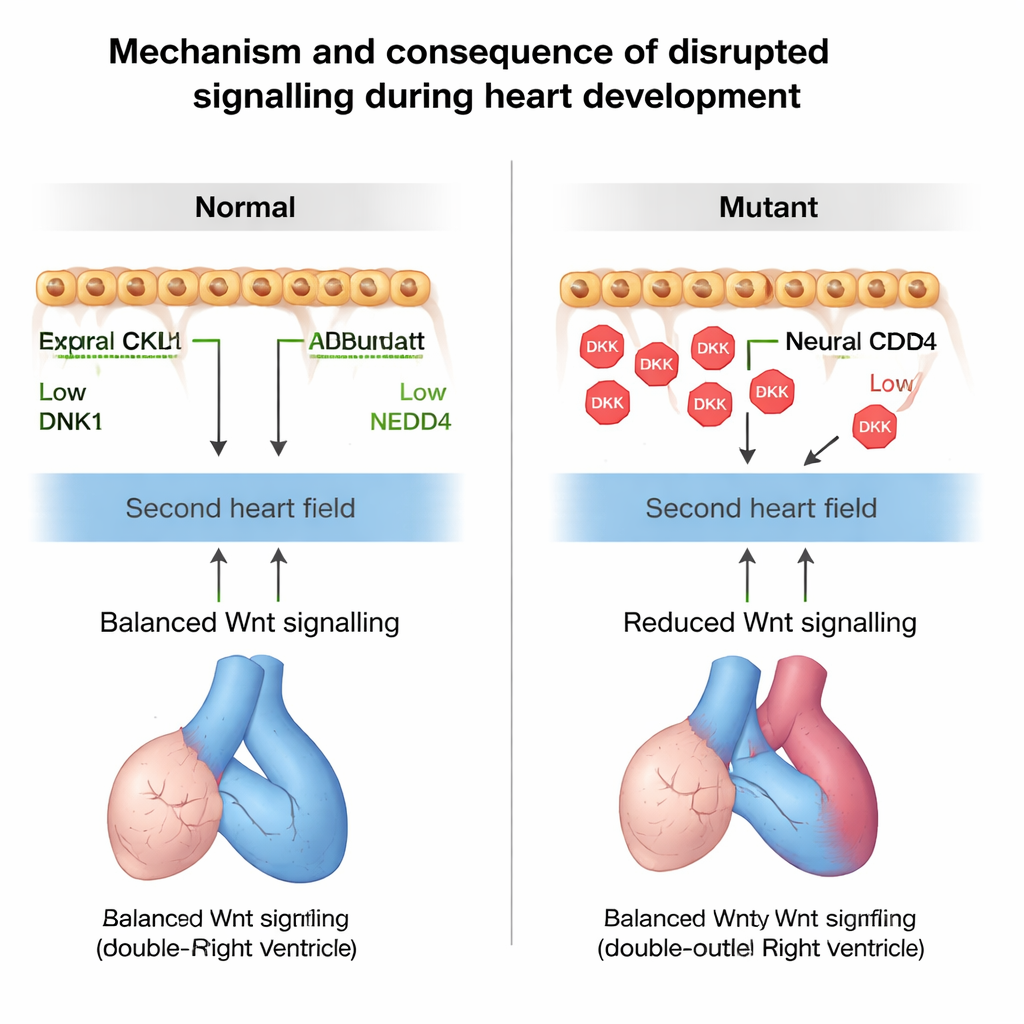
Vad detta betyder för förståelsen av hjärtfel
För icke‑specialister är huvudbudskapet att hjärtats ”utfart” är beroende av exakt timing för när dess byggstenar slutar föröka sig och börjar bli muskel. Denna tidpunkt styrs inte bara inom hjärtvävnaden själv, utan också av intilliggande neurala krestceller som finjusterar en tillväxtsignal via paret NEDD4–DKK1. När denna molekylära dimmer är inställd för lågt, blir utflödesbanan underbyggd och feljusterad, vilket leder till allvarliga medfödda defekter. Genom att kartlägga denna bana och knyta den till en mänsklig genvariant ger studien nya ledtrådar till hur vissa medfödda hjärtfel uppstår och pekar på potentiella molekylära mål för framtida diagnostik eller intervention.
Citering: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Nyckelord: medfödda hjärtfel, hjärtutveckling, neurala krestceller, Wnt‑signalering, hjärtats utflödesbana