Clear Sky Science · sv
Af-CUT&Tag: en känslig och antikropps-fri metod för kromatinkartläggning med genetiskt kodade taggar och högaffinitetsbindare fuserade med Tn5
En titt inuti vår DNA-styrcentral
Varje cell i din kropp bestämmer ständigt vilka gener som ska slås på eller av, vilket påverkar allt från leverns reparation till cancerbenägenhet. Forskare studerar dessa beslut genom att kartlägga var viktiga proteiner sitter på vårt DNA, men de bästa verktygen för detta har länge varit beroende av sköra, dyra antikroppar som inte alltid fungerar bra. Denna artikel introducerar ett nytt, antikropps-fritt sätt att kartlägga DNA–proteininteraktioner, kallat Af-CUT&Tag, som är mer känsligt, mer tillförlitligt och tillräckligt kraftfullt för att fungera även på små prover och enstaka celler.
Varför antikroppar håller oss tillbaka
Konventionella metoder för kromatinkartläggning kräver antikroppar—stora Y-formade proteiner som känner igen ett specifikt målprotein—för att leda ett enzym till rätt platser på DNA. När antikroppar fungerar perfekt tillåter de forskare att se var transkriptionsfaktorer och andra regulatorer är bundna över genomet. Men i praktiken kan antikroppar vara svåra att få tag på, ojämna i kvalitet och blockerade av vanliga kemiska modifieringar på proteiner, såsom fosforylering eller acetylering. Dessa problem kan göra kartorna suddiga, begränsa vilka proteiner som kan studeras och försvåra jämförelser mellan laboratorier eller experiment.
Små taggar och smarta bindare ersätter antikroppar
Af-CUT&Tag kringgår antikroppar helt genom att ge det protein som intresserar forskarna en liten genetisk namnetikett. Med hjälp av CRISPR-genredigering fuserar forskarna korta peptidtaggar, såsom HiBiT eller ALFA, på det naturliga proteinet inne i celler eller vävnader. De använder sedan konstruerade partnerproteiner—högaffinitetsbindare som känner igen dessa taggar—direkt fuserade med Tn5-enzymet, som klipper DNA och fäster sekvenseringsadaptrar. När binder–Tn5-fusionen fäster vid taggen på måltavleproteinet klipper den närliggande DNA och markerar dessa platser för sekvensering. Eftersom taggarna är mycket små och binder–Tn5-fusionen är mycket mindre än en antikropp, kommer detta system lätt in i celler och kärnor, binder med exceptionell precision och påverkas inte av kemiska modifieringar på målproteinet. 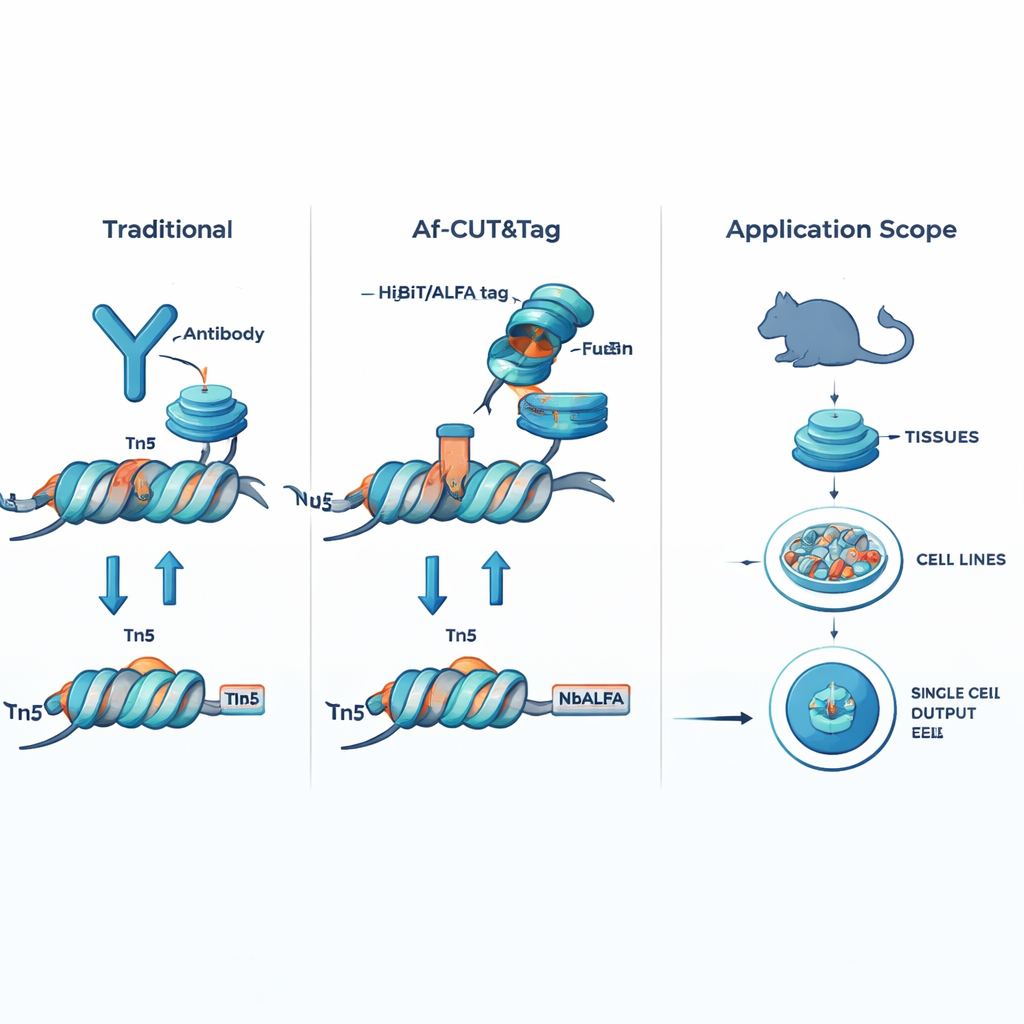
Skarpare kartor från färre celler
Teamet visade först att deras binder–Tn5-fusioner fortfarande binder taggarna mycket hårt och klipper DNA effektivt. De jämförde sedan Af-CUT&Tag med toppmoderna antikroppsbaserade metoder för att kartlägga RNA-polymeras II, enzymet som avläser proteinkodande gener, och CTCF-proteinet, en viktig organisatör av genomstrukturen. I mänskliga cellinjer gav Af-CUT&Tag renare signal vid genstartspunkter, färre off-target-klipp i öppna men irrelevanta DNA-regioner och bättre kvalitet på sekvenseringsbiblioteken. Anmärkningsvärt nog genererade metoden robusta kartor från så få som cirka 500 celler, och samma strategi kunde anpassas till många olika bindare som riktar sig mot skilda DNA-egenskaper. Metoden utökades också till enstaka celler genom att bar-koda varje cells fragment, vilket möjliggjorde konstruktion av detaljerade kromatinkartor per cell.
Följa leverreparation i realtid
För att demonstrera vad denna teknik kan avslöja i levande djur tillämpade författarna Af-CUT&Tag på musleverns regeneration. De använde virus och CRISPR för att lägga till HiBiT-taggar på två viktiga regulatorer i «Hippo»-vägen, YAP1 och TAZ, som hjälper till att kontrollera orgelstorlek och reparation. Efter att ha kirurgiskt tagit bort en del av levern isolerade de levercellskärnor före operation och 24 timmar efteråt och använde Af-CUT&Tag för att se var YAP1 och TAZ var bundna på genomet. Kartorna visade att dessa proteiner tidigt efter skada minskar sin närvaro vid gener som styr fetthantering och syntes, samtidigt som leverceller tillfälligt ackumulerar fettkärnor. Samtidigt ökade YAP1/TAZ bindningen vid gener involverade i rensning av hem, en potentiellt toxisk komponent i blodet, och vid Mir122, en gen som producerar en mikroRNA som är starkt berikad i levern.
miR-122 som en väktare av regeneration
miR-122 är en liten RNA-molekyl som hjälper till att finjustera aktiviteten hos många andra gener. Med Af-CUT&Tag såg forskarna starkare YAP1/TAZ-bindning nära Mir122-området, tillsammans med mer öppet kromatin och ökade kemiska markörer kopplade till genaktivering. Experiment bekräftade att miR-122-nivåerna stiger under den tidiga regenerationsfasen. När teamet specifikt tog bort miR-122 i musleverceller visade djuren mer fettansamling, starkare inflammatoriska svar och färre leverceller som gick in i cellcykeln efter operation. Tillsammans tyder dessa resultat på att YAP1/TAZ hjälper levern att uppnå en noggrann balans under reparation: tillfälligt lagra fett för energi, begränsa skada från hem och inflammation, och använda miR-122 för att dämpa överdriven stress samtidigt som vävnadstillväxt främjas. 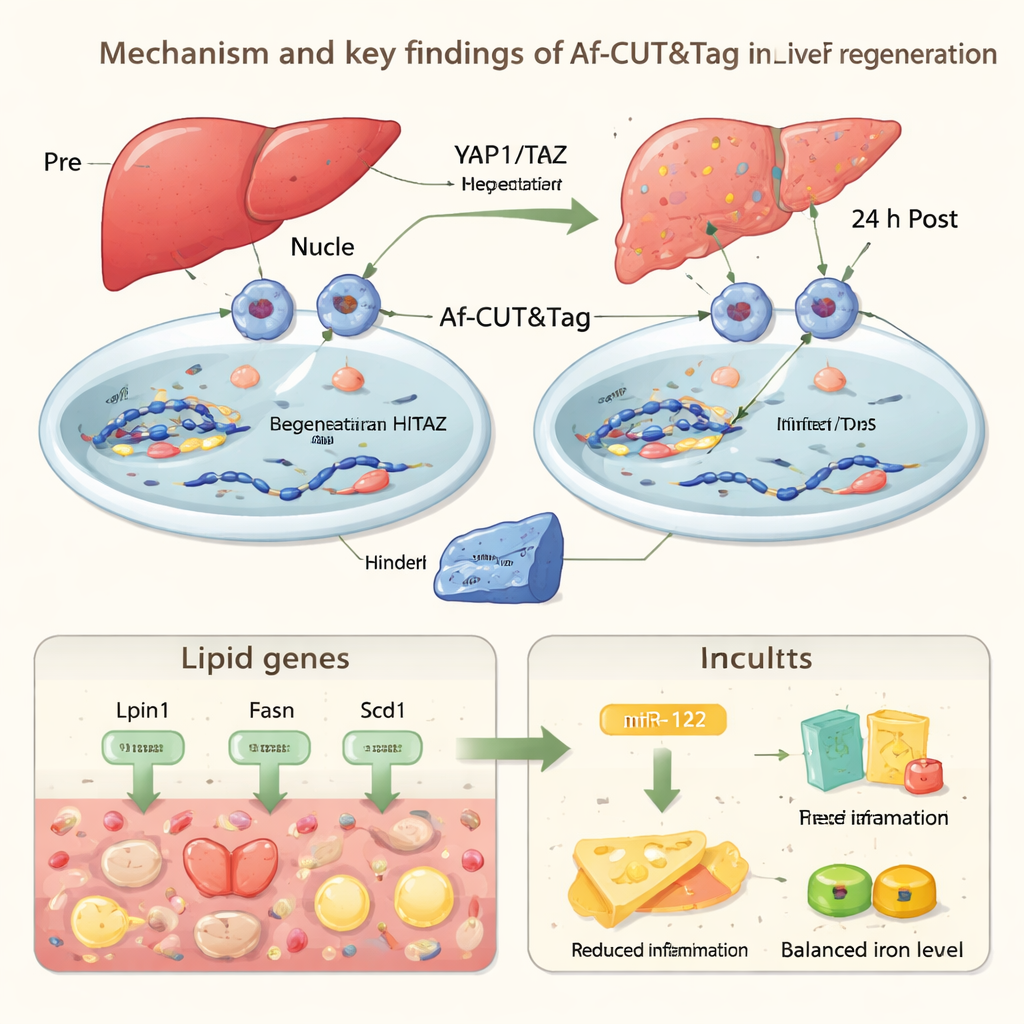
En mångsidig ny lins på genreglering
Af-CUT&Tag erbjuder ett modulärt, antikropps-fritt sätt att se var nyckelproteiner sitter på DNA i cellinjer, vävnader och till och med enstaka celler. Genom att ersätta opålitliga antikroppar med små genetiska taggar och konstruerade bindare ger metoden skarpare, mer reproducerbara kartor från långt färre celler. Tillämpad på leverregeneration avslöjade den hur YAP1 och TAZ samordnar metabolism, järnhantering och mikroRNA:t miR-122 för att stödja tidig reparation. I takt med att genredigering och designade bindare fortsätter att förbättras kan denna strategi bli ett standardverktyg för att dissekera hur genreglering fungerar vid normal utveckling och regeneration — och hur den går fel vid sjukdomar som cancer och leversvikt.
Citering: Wang, X., Deng, X., Qiu, L. et al. Af-CUT&Tag: a sensitive and antibody-free chromatin profiling method using genetically encoded tags and high-affinity binders fused to Tn5. Nat Commun 17, 1746 (2026). https://doi.org/10.1038/s41467-026-68454-9
Nyckelord: kromatinkartläggning, epigenetik, leverregeneration, YAP1 TAZ, microRNA-122