Clear Sky Science · sv
Funktionella varianter vid 1p36.23 medför risk för schizofreni genom att modulera RERE
Varför små DNA-förändringar spelar roll för psykisk hälsa
Schizofreni är en allvarlig psykisk sjukdom som påverkar hur människor tänker, känner och relaterar till andra. Den går starkt i arv, men de flesta genetiska förändringarna som är involverade är små, spridda justeringar i vårt DNA. Denna studie zoomar in på en sådan region i genomet och visar, steg för steg, hur två subtila DNA-varianter kan förändra hjärncellers utveckling och kommunikation på sätt som kan öka en persons risk för schizofreni. 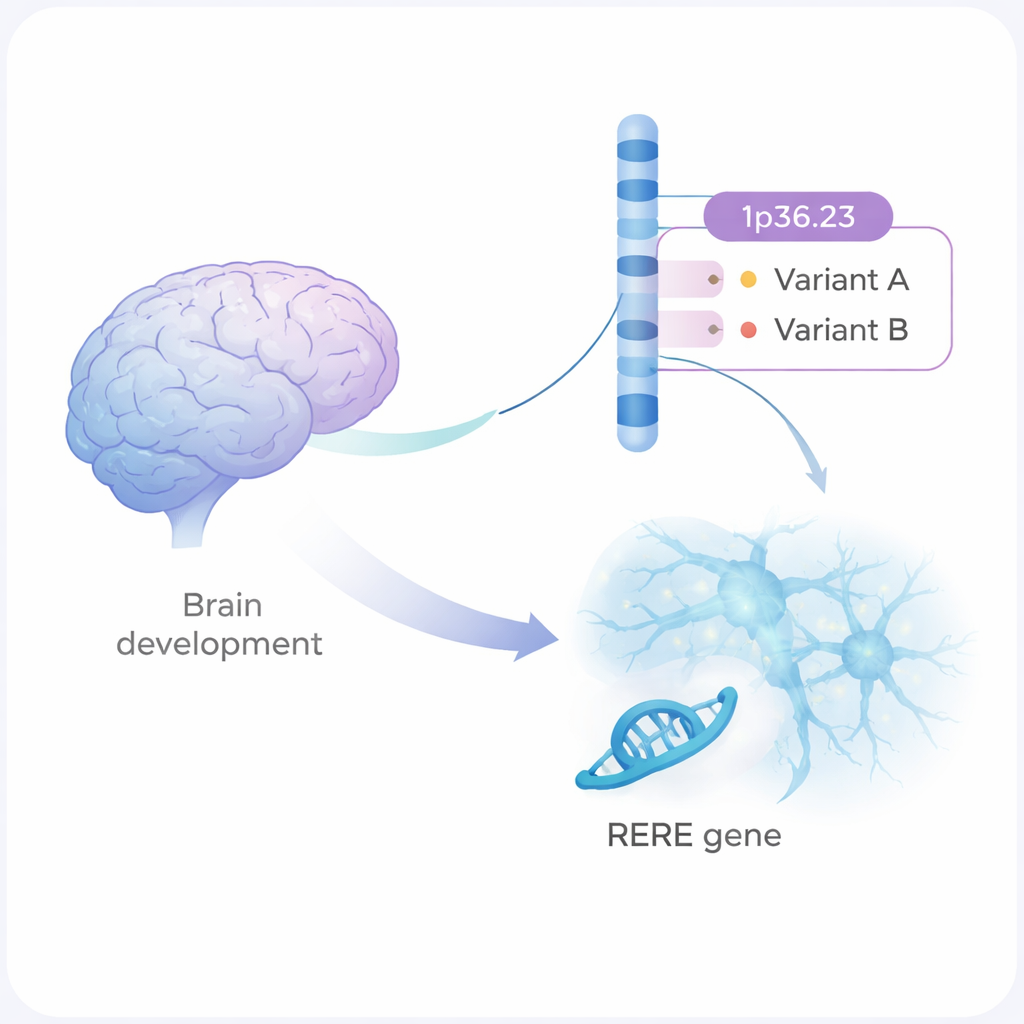
En genetisk het fläck på kromosom 1
Stora genetiska studier har pekat ut mer än 300 regioner i det mänskliga genomet som är kopplade till schizofreni. En av dessa är ett DNA-avsnitt på kromosom 1, kallat 1p36.23. Fram till nu visste forskarna inte vilka exakta förändringar i denna region, eller vilken gen, som stod för den verkliga effekten. Författarna kombinerade statistisk genetik med laboratorieexperiment och identifierade två DNA-varianter, benämnda rs159961 och rs301792, som sitter inne i en gen kallad RERE. Dessa varianter förändrar inte RERE-proteinet i sig; i stället ligger de i reglerande ”omkopplare” inne i genen som kontrollerar hur starkt RERE är påkopplat.
Hur riskvarianter skruvar upp volymen på RERE
Forskargruppen frågade först om dessa två varianter faktiskt fungerar som funktionella omkopplare. Med reporterassays—tester där en DNA-bit driver en ljusproducerande gen—visade de att de schizofreniassocierade versionerna av rs159961 och rs301792 beter sig som starkare enhancers (förstärkare) i nervliknande celler, men inte i orelaterade celltyper. Biokemiska bindningstester förklarade varför: riskformen av den ena varianten försvagar bindningen av REST, ett protein som normalt dämpar genaktivitet, medan riskformen av den andra stärker bindningen av POLR2A, en kärnkomponent i genläsningsmaskineriet. Tillsammans ökar dessa förändringar i proteinbindning aktiviteten hos enhancer-segmenten och pressar upp RERE-uttrycket.
Från ökat RERE till förändrad hjärncellstillväxt
Nästa fråga forskarna ställde var vad extra RERE gör inne i hjärnan. De fann att personer som avlidit med schizofreni visade högre RERE-nivåer i hjärnvävnad jämfört med icke påverkade individer. För att modellera detta ökade de konstgjort RERE-nivåerna i musens neurala stamceller—de omogna celler som ger upphov till neuroner och gliaceller. När RERE överproducerades delade sig stamcellerna mindre, fastnade i ett sent skede av cellcykeln och gav färre mogna neuroner samtidigt som andra celltyper mestadels var oförändrade. I odlade neuroner omformade för mycket RERE även deras förgreningsmönster och minskade antalet och typen av små utskott kallade dendritiska spines, där synapser bildas. Dessa förändringar överensstämmer med långvarig evidens för att schizofreni involverar störd hjärnutveckling och förlust av spines. 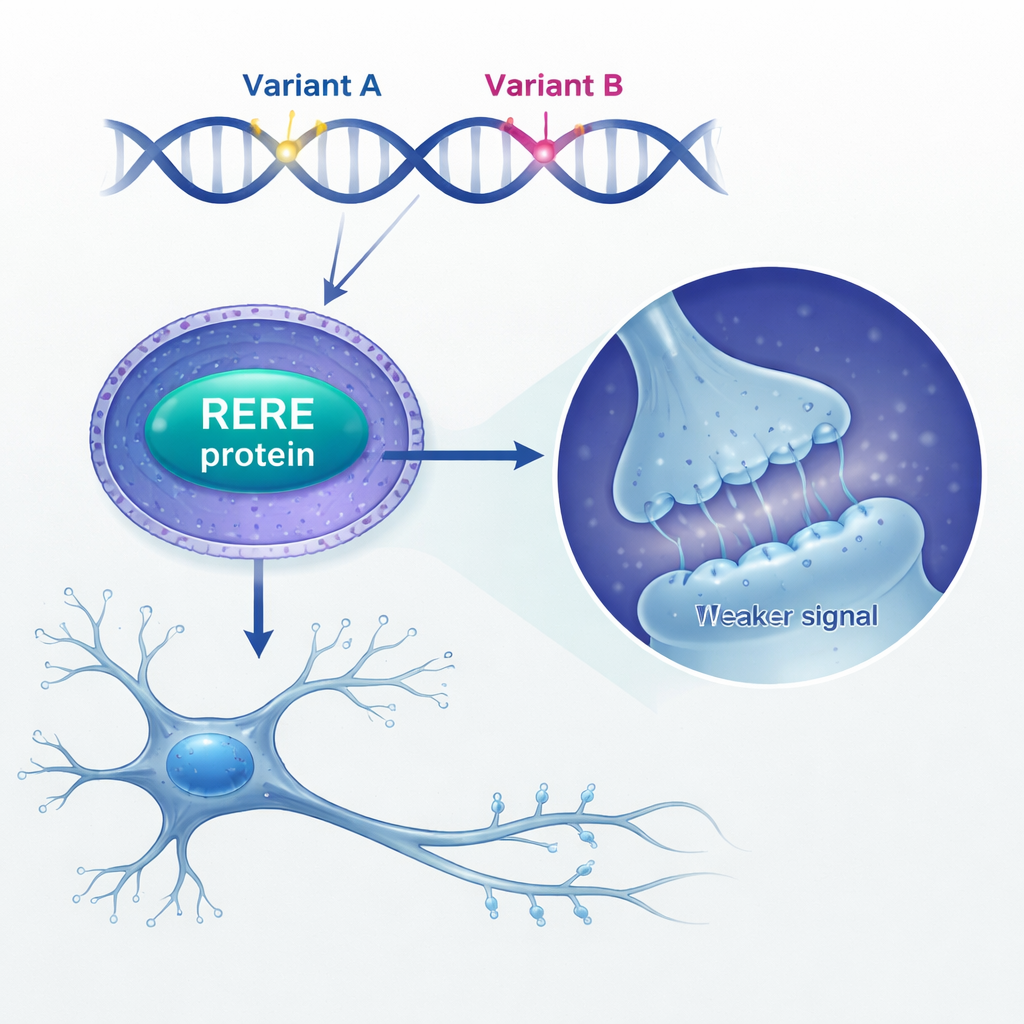
Störning av hjärnans glutamat "samtal"
När de granskade genaktivitet närmare fann teamet att RERE-överuttryck störde nätverk av gener som är involverade i dendrittillväxt och stora kemiska signaleringssystem, särskilt glutamatsignalen. Ett viktigt mål stack ut: genen GRIN2A, som kodar för en avgörande subenhet (GluN2A) i NMDA-typens glutamatreceptorer, länge implicerad i schizofreni. Författarna visade att RERE samarbetar med två andra nukleära proteiner, RARB och RXRA, för att binda direkt till GRIN2A-promotorn och dämpa dess aktivitet. I neuroner med överskott av RERE sjönk GluN2A-nivåerna och elektriska inspelningar visade svagare NMDA-receptor–medierade synaptiska strömmar, även om frekvensen av synaptiska händelser var oförändrad. Med andra ord sänktes ”volymen” på individuella excitatoriska signaler.
Att koppla DNA-varianter till hjärnfunktion
Genom att väva ihop genetik, molekylärbiologi, cellkultur och elektrofysiologi beskriver detta arbete en tydlig kausal kedja: risk-DNA-varianter vid 1p36.23 förstärker regulatoriska element inne i RERE-genen, vilket leder till högre RERE-uttryck i hjärnceller. Förhöjt RERE försämrar i sin tur neuronernas tillväxt och mognad, förändrar formen och antalet synaptiska spines och försvagar glutamatbaserad signalering genom NMDA-receptorer—särskilt de som innehåller GluN2A. För en lekmannaläsare är huvudbudskapet att mycket små DNA-förändringar kan försiktigt skifta aktiviteten hos en enskild gen, och över många hjärnceller och många år kan detta knuffa hjärnans utveckling och kommunikation ur kurs på sätt som bidrar till schizofreni.
Citering: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
Nyckelord: schizofreni genetik, RERE-genen, neurodevelopment, glutamatsignalering, synaptisk funktion