Clear Sky Science · sv
Förbättrad in vivo-genutstängning med hög specificitet med hjälp av multiplexade Cas12a-sgRNA
Mer tillförlitlig genredigering
Genredigering lovar nya sätt att studera biologi, behandla sjukdomar och till och med kontrollera skadeinsekter, men i verkliga djur fungerar det ofta mindre rent än rubrikerna antyder. Många celler undkommer redigering eller förändras bara partiellt, vilket kan göra experimentella resultat otydliga och begränsa praktisk användning. Denna artikel beskriver en ny CRISPR-baserad metod i bananflugan som gör genutstängningar mer fullständiga och mer precisa, och erbjuder en ritning för mer pålitlig genomredigering i komplexa organismer.
Varför standard-CRISPR ofta inte räcker till
Traditionella CRISPR-verktyg som Cas9 klipper DNA på en vald plats med en eller ett fåtal guide-RNA. I levande djur möter detta tillvägagångssätt flera hinder. Vissa guider fungerar helt enkelt dåligt; vissa måltavlor är svåra för enzymet att nå; och cellens reparationsmekanismer ”lagar” ofta brottet med små förändringar som lämnar genen fungerande. Resultatet blir en mosaik: intilliggande celler i samma vävnad kan bära olika mutationer, eller inga alls. Denna fläckighet gör det svårt att avgöra vad som händer när en gen verkligen stängs av, och utgör en utmaning för tillämpningar som genterapi eller genmodifierade spridningssystem som måste agera effektivt i de flesta celler.
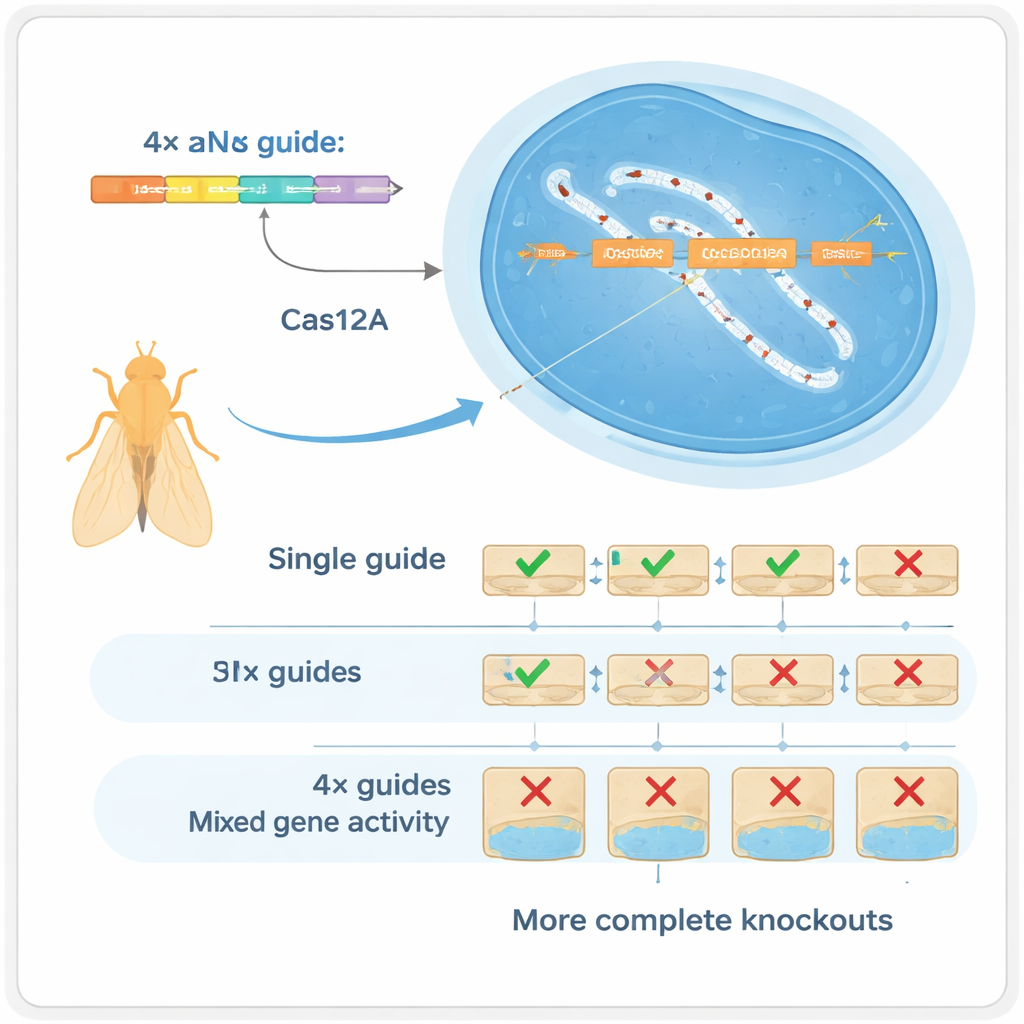
Fyra guider är bättre än en
Författarna vände sig till ett annat CRISPR-enzym, Cas12a, som kan processa kompakta arrayer av guider mycket lättare än Cas9. De byggde ett Drosophila-verktyg där varje gen riktas av en array med fyra guide-RNA, alla kodade på en enda liten DNA-fragment som kan massproduceras. I kontrollerade tester visade de att användning av fyra guider per gen dramatiskt förändrar vilka typer av DNA-förändringar som uppstår: i stället för mestadels små insättningar eller deletioner vid en enstaka plats, skapar systemet ofta större deletioner mellan klippställen som nästan alltid förstör genfunktionen. Denna ”multiplexning” fungerar på två sätt: om en guide misslyckas kan andra fortfarande göra jobbet (redundans), och när flera klipper samtidigt kan de ta bort större delar av genen (synergi).
Hög effektivitet utan extra sidoeffekter
Att skapa fler DNA-brott väcker uppenbara säkerhetsfrågor. Kan flera klipp i ett område av misstag radera närliggande gener? Kan guider fela på andra platser i genomet oftare? För att adressera detta mätte forskarna celldöd, undersökte effekter på närliggande gener och skapade ett smart assay för att visualisera kromosomreparationer kallat förlust av heterozygositet över stora DNA-avsnitt. De fann att att klustra fyra klipp inom en enda gen tolererades väl: det ökade inte celldöd jämfört med konventionella Cas9-metoder och störde sällan närliggande gener om inte en guide hamnade extremt nära ett regulatoriskt element. Storskaliga screenar med mer än 2 000 guider över en tredjedel av flugans genom visade att över 99 % av guide-arrayerna var aktiva vid sina avsedda mål, medan reproducerbar off-target-aktivitet låg under 1 %, vilket tyder på mycket hög specificitet även i en multiplexad uppsättning.
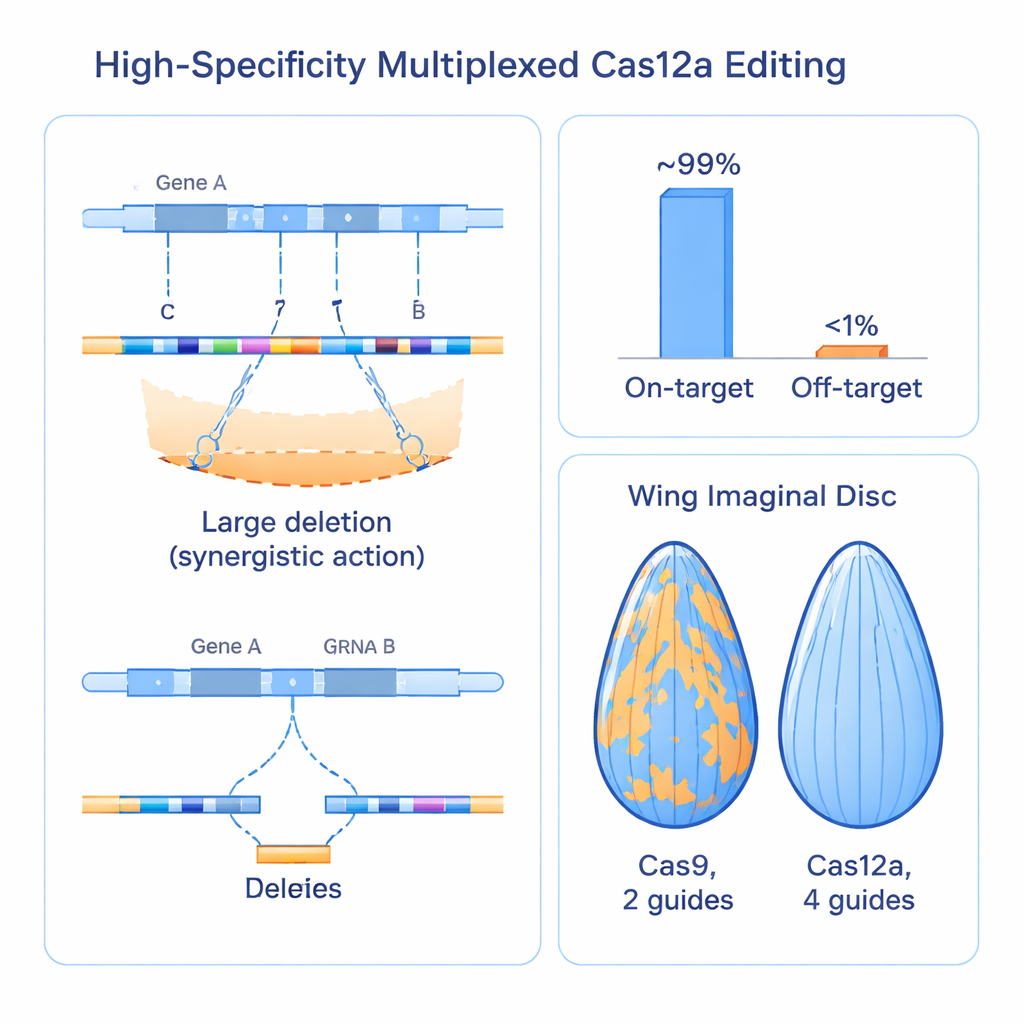
Slår etablerade Cas9-system i verkliga vävnader
För att se om dessa molekylära förbättringar leder till tydligare biologiska effekter jämförde teamet sitt Cas12a–fyra-guider-system direkt mot allmänt använda Cas9-baserade resurser som riktar mer än 100 gener i flugan. I vävnader som öga, tarm och utvecklande vinge gav Cas12a-ansatsen starkare och mer enhetliga förlust-av-funktions-effekter än Cas9, som ofta lämnade tydliga fläckar av oredigerad, normal vävnad. När de använde vingstorlek som ett kvantitativt mått genererade det nya systemet konsekvent större och mer reproducerbara tillväxthämningar för kända regulatorer, vilket visade att vissa gener tidigare bedömts som svaga eller icke-nödvändiga faktiskt missades eftersom äldre verktyg inte inaktiverade dem tillräckligt grundligt. Metodens ökade kraft avslöjade till och med en tidigare okänd, essentiell roll för en gen kallad trade embargo i vingutveckling och överlevnad.
Vad detta betyder för framtidens genredigering
Enkelt uttryckt visar detta arbete hur man kan förvandla CRISPR från en ibland rörig skalpell till en mer avgörande strömbrytare för att stänga av gener i levande djur. Genom att kombinera Cas12a med fyra guider per gen uppnår författarna nästan fullständiga utstängningar med mycket få oavsiktliga effekter, allt i ett format som är praktiskt att skala över hundratals gener. Även om metoden utvecklades i bananflugan är de grundläggande principerna — att använda flera guider för redundans och synergi och noggrant kontrollera kromosomala sidoeffekter — brett tillämpliga. Denna strategi kan förbättra grundforskning, skärpa genetiska screenar och vägleda säkrare utformningar för framtida medicinska och ekologiska tillämpningar av genredigering.
Citering: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Nyckelord: CRISPR, Cas12a, genutstängning, Drosophila, genomredigering specificitet