Clear Sky Science · sv
Shigella flexneri undviker septinmedierad cellautonom immunitet via protein‑ADP‑riboxanering
Hur vissa tarmbakterier smiter förbi vårt inre säkerhetssystem
Allvarlig diarré orsakad av Shigella‑bakterier är fortfarande ett stort problem globalt, särskilt för små barn. Våra celler är inte hjälplösa: de har inbyggda verktyg som kan fånga och förstöra angripande mikrober. Denna studie visar hur Shigella flexneri, en ledande orsak till dysenteri, använder smarta molekylära knep för att montera ner ett av dessa verktyg och på så sätt hjälpa bakterien att sprida sig från cell till cell i tarmen.
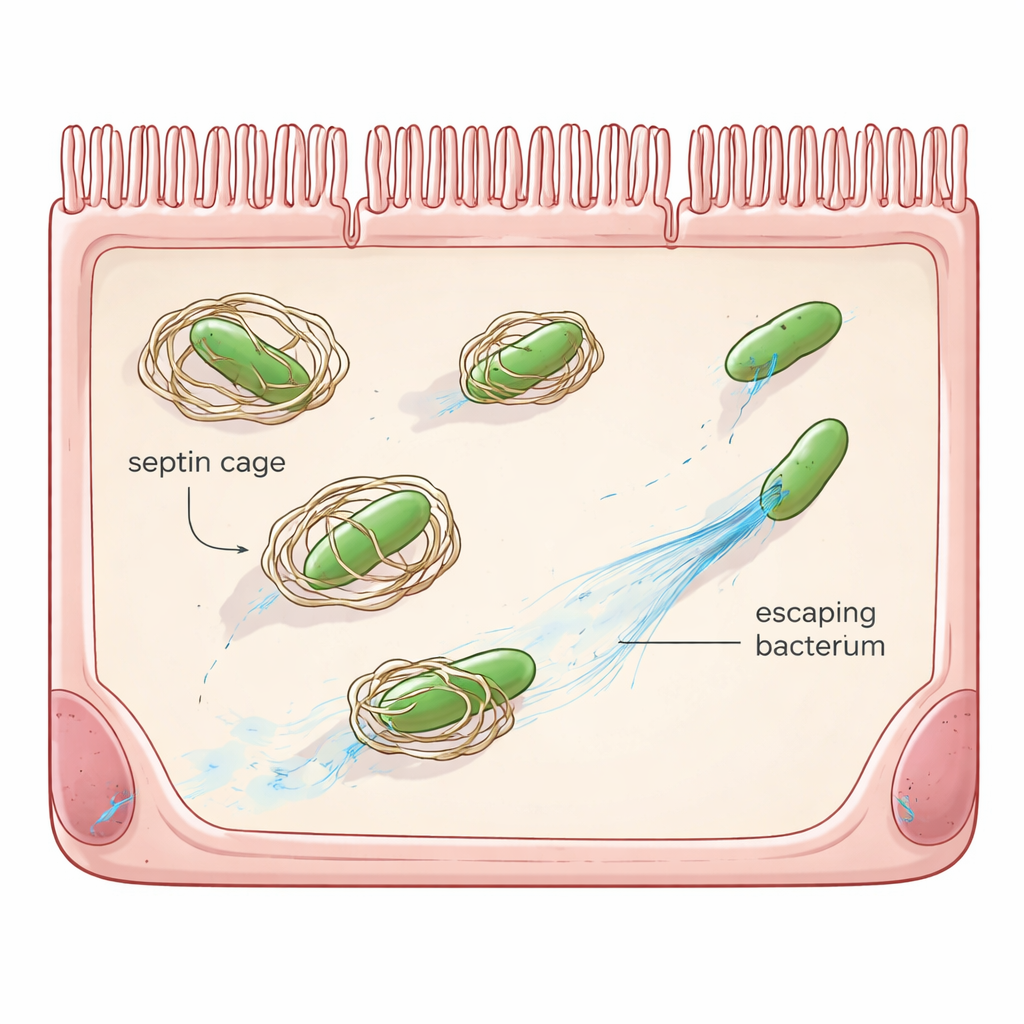
Cellens "gör‑det‑själv"‑försvar
Utöver vita blodkroppar och antikroppar bär många vanliga celler på egna nödsäkerhetssystem, så kallad cellautonom immunitet. Ett sådant system bygger på septiner, en familj av stommeproteiner som bildar ringar och bur‑liknande strukturer. När Shigella tar sig in i en cell och slinker ut i cellens geléaktiga inre kan septiner samla sig runt bakterien, blockera dess förmåga att röra sig och markera den för nedbrytning via cellulära återvinningsvägar. Tidigare arbete visade att Shigella redan har en motåtgärd, ett protein kallat OspG, som märker septiner för borttagning. Ändå undviker de flesta bakterier fortfarande att bli inburade även när OspG saknas, vilket antyder att Shigella har fler knep i ärmen.
Avslöjandet av en andra bakteriell sabotör
Forskarna riktade sin uppmärksamhet mot en annan grupp Shigella‑proteiner, kända som OspC‑familjen. Med en global metod för kartläggning av proteiner i mänskliga celler letade de efter värdproteiner som kemiskt modifierades i närvaro av OspC‑proteiner. Utöver kända mål inom proteinsyntesen fann de att flera septiner, särskilt ett som kallas SEPT9, konsekvent blev märkta. Detaljerade biokemiska tester visade att tre OspC‑proteiner kan fästa en liten energirik tagg, härledd från molekylen NAD, på flera platser i septinerna. Denna kemiska förändring, kallad ADP‑riboxanering, är en särskild, irreversibel variant av en vanligare proteinmodifiering.
Att bryta sönder proteinstommen inifrån
För att förstå hur denna kemiska tagg försvagar cellens försvar zoomade teamet in på SEPT9. Septiner bildar normalt ordnade kedjor om åtta enheter, som sedan linjeras i filament och slutligen bildar fullständiga burar runt bakterier. Forskarna upptäckte att en särskild position i SEPT9, en aminosyra kallad arginin 561, är huvudstället för ADP‑riboxanering under infektion. Strukturellt arbete och återuppbyggnadsexperiment med renade proteiner visade att denna plats ligger i en kritisk kontaktyta där två SEPT9‑enheter låser ihop sig. När den argininen kemiskt modifieras — eller ersätts med en rest som efterliknar den tillsatta negativa laddningen — faller de oktameriska kedjorna isär i mindre bitar och kan inte längre bygga stabila filament.
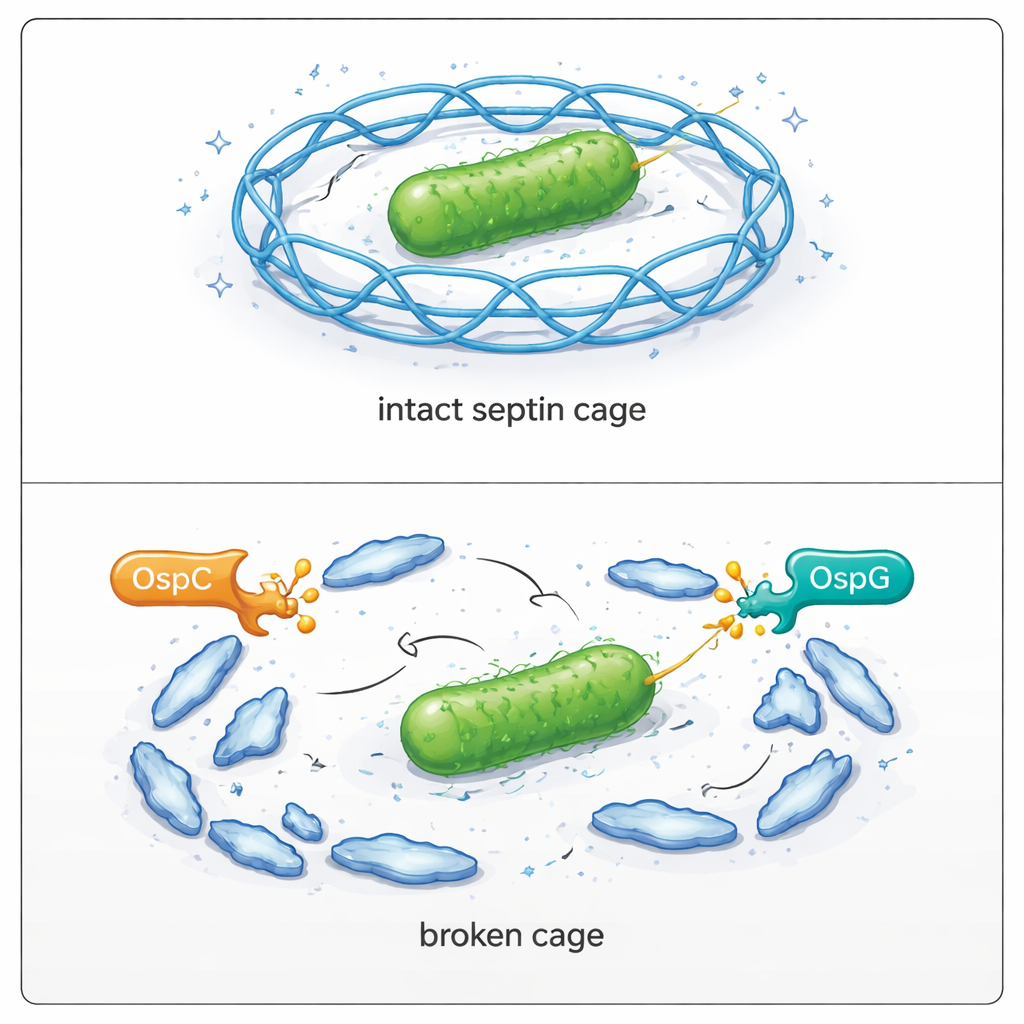
Att se hur burarna fallerar i infekterade celler
Teamet återgick sedan till levande celler för att se konsekvenserna. I mänskliga celler infekterade med normala Shigella hamnade bara en minoritet av bakterierna i septinburar. När alla OspC‑proteiner genetiskt togs bort fördubblades nästan andelen inburade bakterier. Att ta bort OspG gav en liknande effekt, och att ta bort både OspC och OspG tillsammans ökade burbildningen ännu mer och påverkade bakteriernas förmåga att sprida sig över ett cellager kraftigt. Återintroduktion av aktiva OspC‑proteiner i de mutanta stammarna återställde deras förmåga att undkomma burar och att replikera och bilda stora plack. Mikroskopi bekräftade att när SEPT9 inte kan modifieras vid arginin 561 ansluter det effektivt till burar; när det ändras av OspC sjunker burbildningen runt bakterier kraftigt.
Vad detta betyder för att bekämpa Shigella
Enkelt uttryckt visar detta arbete att Shigella bär på ett par matchade molekylära verktyg som är utformade för att bryta upp gallret i ett intracellulärt "fängelse." OspC försvagar direkt de proteinbyggstenar som behövs för att konstruera septinburar, medan OspG främjar deras borttagning via en annan kemisk väg. Tillsammans låter dessa strategier bakterierna slinka fria, röra sig inom celler och invadera grannceller. Att förstå dessa precisa flyktmekanismer fördjupar inte bara vår bild av hur cellintrinsisk immunitet fungerar, utan pekar också på nya terapeutiska angreppsvinklar: läkemedel som blockerar OspC eller skyddar viktiga septinkontakter skulle kunna hjälpa till att återställa cellens naturliga förmåga att fånga och rensa denna farliga patogen.
Citering: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Nyckelord: Shigella, septinceller, cellautonom immunitet, bakteriella virulensfaktorer, ADP‑ribosylation