Clear Sky Science · sv
Peptidiska naturprodukter som riktar sig mot ClpC1 stör proteomet i Mycobacterium tuberculosis på olika sätt
Varför det spelar roll att störa bakteriernas städpatrull
Tuberkulos är fortfarande en av världens dödligaste infektionssjukdomar, och läkemedelsresistenta stammar av Mycobacterium tuberculosis gör behandlingen svårare. De flesta befintliga antibiotika angriper bakteriens cellvägg eller dess förmåga att utvinna energi och kopiera genetiskt material. Denna studie undersöker en helt annan svag punkt: cellens interna ”städpatrull” som upprätthåller proteinernas hälsa. Genom att förstå hur nya, naturproduktbaserade molekyler rubbar detta rengöringssystem hoppas forskare kunna utforma framtida läkemedel som kan döda tuberkelbakterier på nya och mer hållbara sätt.
Cellens nav för proteinunderhåll
Liksom alla levande celler bygger, viker, reparerar och återvinner tuberkelbakterien ständigt sina proteiner. En central aktör i detta nätverk är en stor maskin kallad ClpC1–ClpP1P2-komplexet. En del (ClpC1) fungerar som en chaperon, känner igen och drar in skadade eller onödiga proteiner, medan den andra delen (ClpP1P2) klipper sönder dem för återvinning. Detta system är avgörande för bakteriens överlevnad, särskilt under stress som värme eller antibiotikapåverkan. Flera naturliga peptidföreningar — ecumicin, ilamyciner (rufomyciner) och cyclomariner — är redan kända för att binda ClpC1 och uppvisa stark TB-dödande aktivitet, vilket tyder på att detta komplex kan vara ett kraftfullt läkemedelsmål. 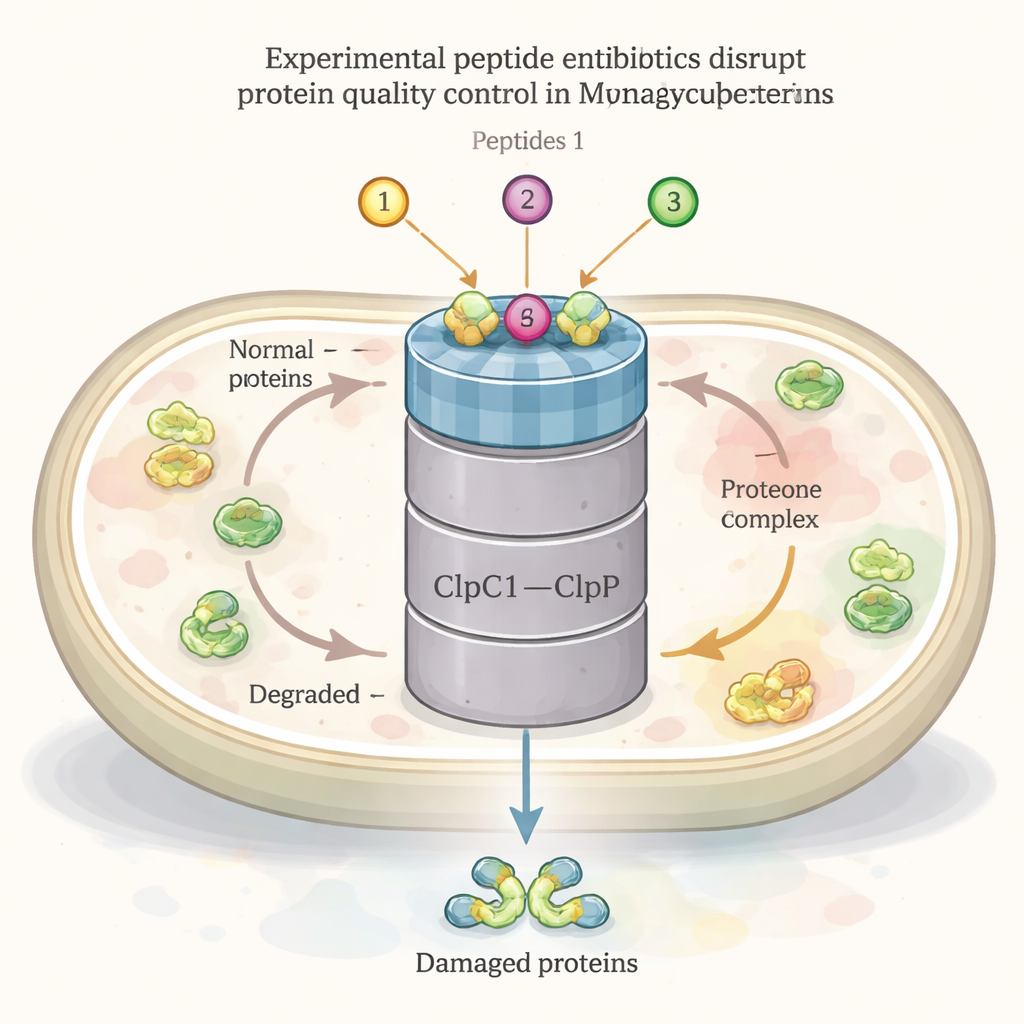
Tre besläktade läkemedel, tre olika effekter
Forskarna undersökte en representant från varje peptidfamilj: en ecumicin-analog (Ecu*), ilamycin E (IlaE) och en cyclomarin-derivat (desoxycyclomarin, dCym). Trots att alla tre fäster vid samma region på ClpC1 uppvisar de inte samma beteende i cellen. Genom kvantitativ proteomik — en metod som mäter tusentals proteiner samtidigt — fann de att Ecu* orsakade det bredaste störningsmönstret och påverkade nivåerna av nästan 17 % av alla bakterieproteiner i betydande grad. IlaE förändrade cirka 12 % och dCym cirka 7 %. Endast 72 proteiner påverkades konsekvent av alla tre föreningarna, och de flesta av dessa minskade i mängd. Detta visar att varje molekyl driver ClpC1-maskinen i olika riktningar och omformar cellens proteinlandskap på distinkta sätt snarare än att helt enkelt ”stänga av maskinen”.
Täppa igen shreddaren kontra slå av strömmen
För att sätta dessa effekter i kontext jämförde teamet peptiderna med bortezomib, en cancerläkemedel som brett blockerar protein-nedbrytande enzym. I TB-bakterier orsakade bortezomib en generell ansamling av många proteiner, vilket förväntas när shreddrarna stängs av. Till skillnad från detta gav peptiderna mer selektiva mönster: vissa kända ClpC1-mål ackumulerade, andra utarmades, och en global hämmning av all protein-nedbrytning observerades inte. Detaljerade laboratorietester med renade komponenter visade att varje peptid ändrade hur specifika substrat hanterades. Till exempel störde alla tre nedbrytningen av ett reglerande protein (PanD), men endast Ecu* blockerade nedbrytningen av ett modellprotein utan fast struktur, och endast dCym försämrade nedbrytningen av det stress-skyddande proteinet Hsp20. Dessa skillnader antyder att det övergripande formen och flexibiliteten hos varje målprotein påverkar hur det påverkas när ClpC1 blir ”felsinnad” av en given förening. 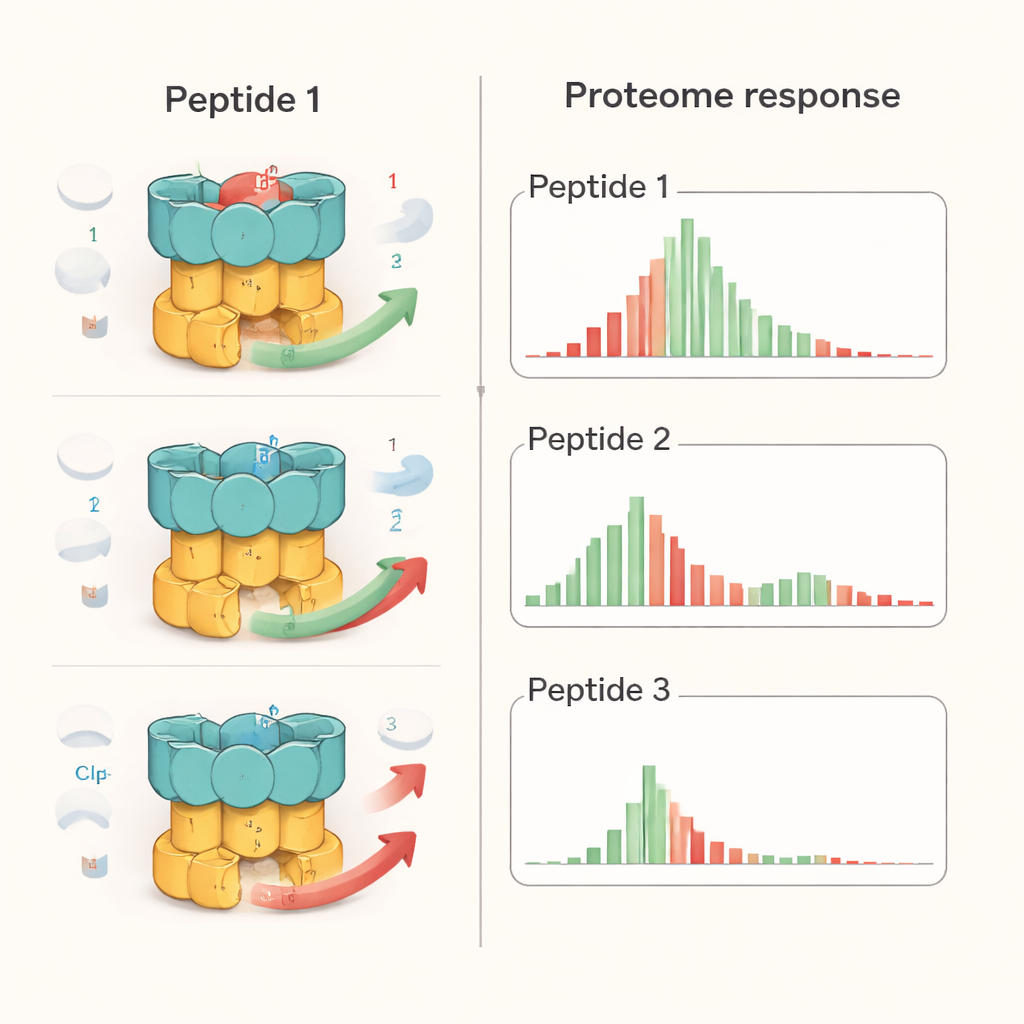
Stressreaktioner och bakreparationsmekanismer hos bakterien
Tuberkelbakterien har reservsystem för att hantera situationer när proteinskador överväldigar huvudrensningsmaskineriet. Ett sådant system involverar en annan chaperon, ClpC2, som kan binda cyclomarin-liknande molekyler och minska deras påverkan på ClpC1. Denna studie fann att även om alla tre peptider kan binda ClpC2 i provrör, var det endast cyclomarin-derivaten (dCym) som faktiskt utlöste högre ClpC2-nivåer i levande bakterier och som blev mer potent när ClpC2 experimentellt minskades. Däremot förblev Ecu* och IlaE effektiva även när ClpC2 slog ned, vilket tyder på att de i stor utsträckning kringgår denna självåterställningsväg. Teamet upptäckte också en stark, föreningsspecifik koppling till Hsp20, ett litet protein som hjälper till att förhindra skadliga sammanklumpningar: Ecu* (och i viss mån IlaE) orsakade dramatiska ökningar i Hsp20-nivåer och Ecu* band direkt till Hsp20, vilket avslöjar en ny koppling mellan dessa läkandekandidater och cellens stressresponssystem.
Att vända stress till terapeutisk fördel
Där ClpC1-systemet är särskilt viktigt under svåra förhållanden testade forskarna läkemedlen medan bakterierna utsattes för mild värmestress, vilket ökar mängden felvikta proteiner. Under dessa förhållanden blev både Ecu* och dCym mycket mer dödliga och nådde toxicitet jämförbar med bortezomib, trots att de verkar mer selektivt. Detta visar att noggrant riktade insatser mot protein-kvalitetskontrollen kan vara lika effektiva som att slå ut alla stora proteaser, men med potentiellt mer preciserad kontroll. Arbetet visade också att många av de förändringar som Ecu* orsakade i proteinnivåer inte enkelt speglade förändringar i genaktivitet, vilket understryker att störning av ClpC1 huvudsakligen rubbar reglering efter att proteinerna har tillverkats.
Vad detta betyder för framtida TB-behandlingar
För icke-specialister är huvudbudskapet att TB-bakterier är beroende av ett finstämt internt städ- och stressresponssystem för att överleva. De tre naturprodukt-deriverade peptiderna som testades här binder alla samma centrala maskin men tvingar den in i olika lägen, vilket leder till mångsidiga och mycket specifika snedvridningar i bakteriens proteinsammansättning. Viktigt är att ecumicin-liknande och ilamycin-liknande föreningar undviker en inbyggd bakreparationsmekanism som kan dämpa cyclomarins effekt, men ändå försvagar patogenen under stress. Dessa egenskaper gör dem till lovande byggstenar för framtida tuberkulosläkemedel, inklusive designade molekyler som kan tvinga TB-celler att selektivt förstöra sina egna livsviktiga proteiner eller som kan byggas in i ”proteinriktade chimärer” för att precist styra bakteriers självnedbrytning.
Citering: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Nyckelord: tuberkulos, protein-kvalitetskontroll, ClpC1, antibiotikaresistens, naturproduktantibiotika