Clear Sky Science · sv
Simultana epigenomiska profiler och mätning av regulatorisk aktivitet med e2MPRA
Att läsa cellens dolda strömbrytare
Varje cell i din kropp bär i princip samma DNA, men en nervcell och en levercell beter sig mycket olika. Hemligheten ligger i korta DNA-sekvenser som fungerar som dimmerströmbrytare för gener och kan slå upp, ner eller av uttrycket. Denna studie presenterar ett kraftfullt nytt verktyg, kallat e2MPRA, som låter forskare testa tusentals sådana strömbrytare samtidigt samtidigt som de kartlägger hur DNA:t är paketerat och märkt inne i cellen — viktiga steg för att förstå utveckling, sjukdomsrisk och varför vissa genetiska varianter spelar roll medan andra inte gör det.
Från DNA-kartor till DNA-funktion
Under det senaste decenniet har forskare ritat stora kartor över ”kandidata” regulatoriska strömbrytare, kända som cis-regulatoriska element. De använder metoder som visar var DNA är löst packat (öppet kromatin), vilka proteiner som binder och vilka histonmarkeringar som pryder det omgivande DNA:t. Dessa kartor är imponerande, men de är mest beskrivande: att ett protein binder eller att en markering syns bevisar inte att en sekvens faktiskt kontrollerar genaktivitet. Traditionella massivparallella reporterassays (MPRAs) kan testa om tusentals DNA-bitar förstärker eller tystar en reporter-gen, men de säger inte vilka proteiner som binder där eller vilka epigenetiska förändringar som följer med den aktiviteten.
En två-i-ett-assay för aktivitet och epigenetiska märken
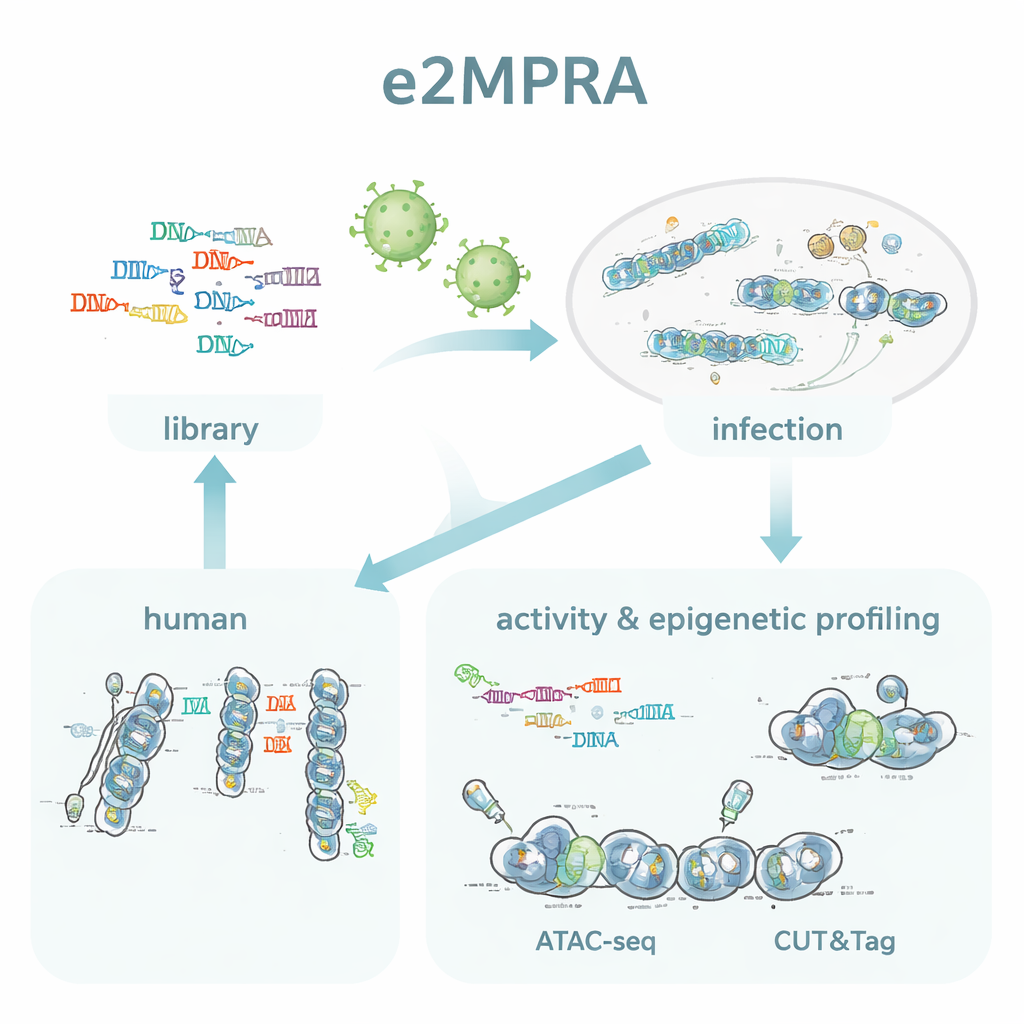
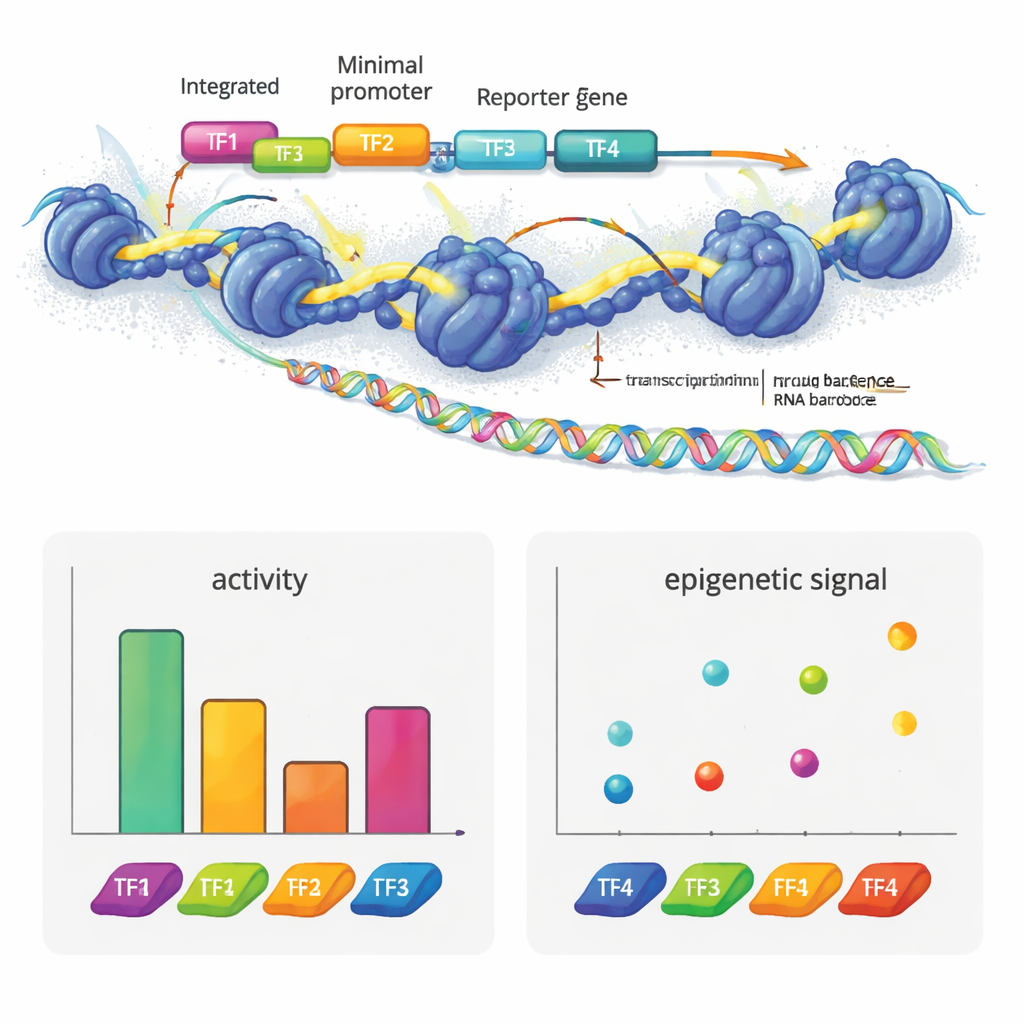
Författarna skapade e2MPRA genom att kombinera ett lentiviralt MPRA med två epigenomiska tekniker, ATAC-seq och CUT&Tag. Först bygger de ett DNA-bibliotek där varje kandidatsekvens är kopplad till en kort streckkod och placerad intill en minimal promotor och en reporter-gen. Detta bibliotek paketeras sedan i lentivirus och integreras många gånger i genomerna hos odlade humana celler. Från samma cellpool läser de streckkoderna i RNA för att mäta regulatorisk aktivitet, och de använder ATAC-seq och CUT&Tag för att mäta kromatinöppning och en viktig histonmarkering (H3K27ac) specifikt vid de insatta sekvenserna. Genom att normalisera dessa signaler mot hur ofta varje sekvens faktiskt integreras får de jämförbara mätningar av ”på/av-styrka” och epigenetiskt tillstånd för tusentals element i ett enda experiment.
Avkodning av hur transkriptionsfaktormotiv samverkar
För att se vad denna teknik kan avslöja byggde teamet syntetiska enhancers av kända transkriptionsfaktormotiv som används i leverceller. De arrangerade dessa motiv i olika antal och ordningar på neutrala DNA-mallar. Vissa faktorer, såsom HNF1A och XBP1, uppträdde som klassiska aktivatorer: fler kopior ökade reporterutslaget. Andra, som HNF1A och ONECUT1, ökade främst kromatinåtkomsten och passade in i deras roll som ”pioneer”-faktorer som öppnar sluten DNA. PPARA visade ett annat mönster, med stark påverkan på kromatin och histonmarkeringar men inte på transkription ensam, samtidigt som den samarbetade med andra faktorer för att öka genaktivitet. REST, en känd represssor, dämpade aktiviteten när den placerades intill aktivatorer. Slående nog kunde enkel omordning av fyra motiv avsevärt ändra enhancer-styrkan, och aktivatorer tenderade att fungera bäst när de låg närmare promotorn — vilket avslöjar en slags grammatisk struktur i hur dessa motiv är ordnade.
Att lokalisera känsliga baser i pluripotens-enhancers
Forskarna vände sig sedan till enhancers som är viktiga för stamcellsidentitet, med fokus på regioner bundna av pluripotensfaktorerna POU5F1 (också kallad OCT4) och SOX2. De skapade täta mutationsbibliotek där varje bas i 100 basparen långa enhancers systematiskt ändrades, tillsammans med små sex-basskift som slumpmässigt scramblingades. Genom att använda e2MPRA i inducerade pluripotenta stamceller kunde de se vilka mutationer som försvagade eller stärkte reporteraktiviteten och hur de påverkade kromatinöppning och acetylation. Att störa POU5F1::SOX2-bindningsmotivet minskade ofta både genaktivitet och epigenetiska markeringar, vilket bekräftar dess centrala roll. I en välstuderad enhancer nära POU5F1-genen fann de också att en förändring i ett YY1-motiv ökade transkriptionen men minskade kromatinöppningen, vilket antyder att vissa faktorer kan främja ett öppet tillstånd samtidigt som de håller tillbaka uttrycket.
Vad detta betyder för gener och sjukdom
e2MPRA reproducerar inte perfekt alla nyanser i genomets naturliga 3D-kopplingar, men det erbjuder ett praktiskt sätt att jämföra tusentals regulatoriska sekvenser och varianter under samma förhållanden. Genom att koppla en funktionell avläsning (hur starkt ett DNA-segment driver en gen) med epigenetiska avläsningar (hur det DNA:t är paketerat och märkt) hjälper metoden att förklara varför vissa transkriptionsfaktormotiv, kombinationer och positioner är så avgörande. På sikt kan verktyg som e2MPRA göra det lättare att tolka icke-kodande genetiska varianter kopplade till sjukdom, designa syntetiska enhancers för genterapi och bygga en mer komplett ”regulatorisk kod” som knyter DNA-sekvens till cellbeteende.
Citering: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Nyckelord: genreglering, enhancers, epigenetik, transkriptionsfaktorer, funktionell genomiik