Clear Sky Science · sv
Vårdande ubiquitin E3-ligas riktar cancerassocierade APOBEC3-deaminaser för nedbrytning för att främja människans genomintegritet
Skydda vårt DNA från vänligt eld
Våra celler använder kraftfulla enzymer för att skada virus-DNA, vilket hjälper oss att stå emot infektioner. Men några av dessa samma enzymer kan, om de lämnas utan kontroll, av misstag skada vårt eget genom och bidra till cancer. Denna studie avslöjar hur människoceller övervakar dessa riskfyllda enzymer och visar ett inbyggt "kvalitetskontroll"-system som märker farliga varianter för destruktion innan de kan skriva om vårt DNA.
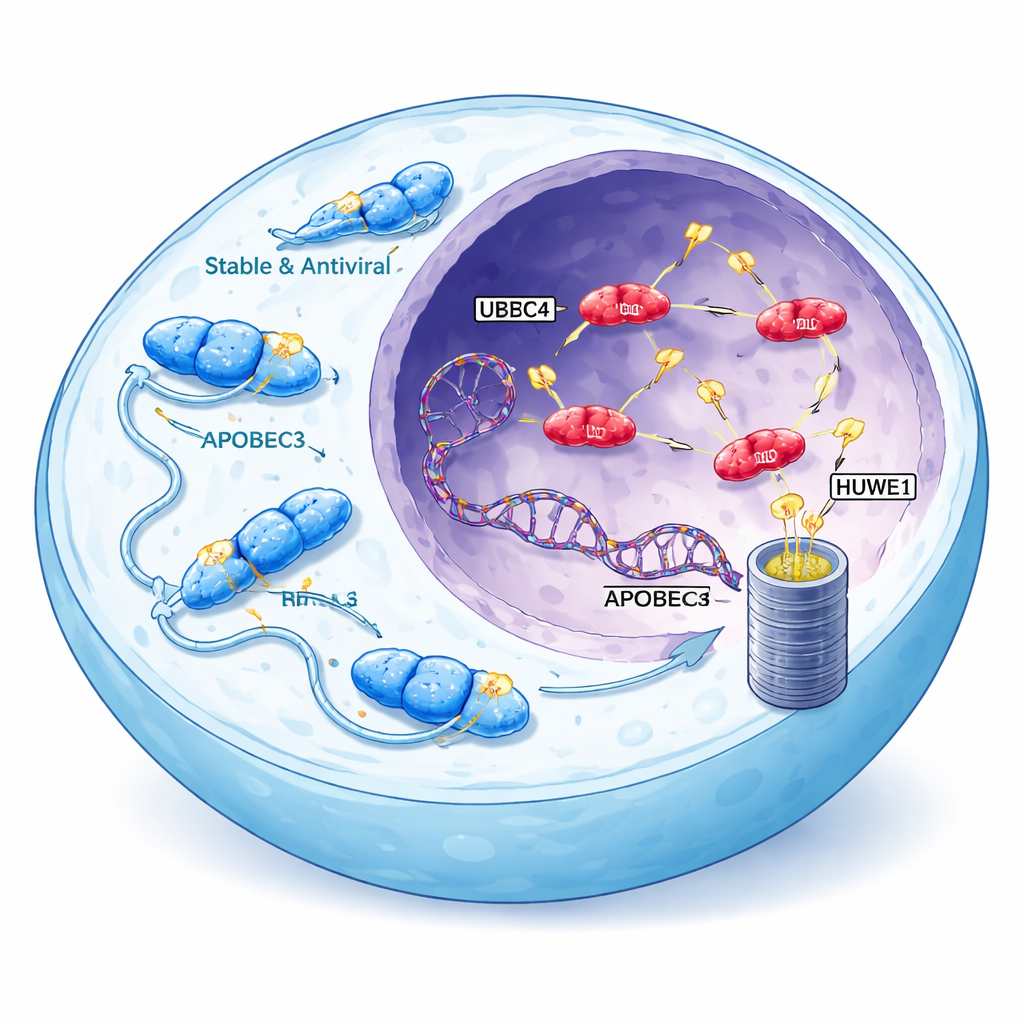
Virusbekämpare som kan vända sig mot oss
APOBEC3-familjen av enzymer hjälper normalt till att försvara mot virus som HIV genom att kemiskt ändra virusets DNA och därigenom orsaka dödande fel. Människor bär på sju APOBEC3-varianter, och tre av dem—A3A, A3B och en form av A3H kallad haplotype I (A3H-I)—är starkt kopplade till muteringsmönster som ses i många cancerformer. Dessa särskilda enzymer kan ta sig in i cellkärnan, där våra kromosomer finns, och skapa karakteristiska kluster av mutationer i genomet. Sådana APOBEC-relaterade signaturer förekommer i över hälften av alla mänskliga cancerformer, särskilt i bröst-, lunga- och blåscancer, där de ökar mängden genetiska förändringar som tumörer kan använda för att anpassa sig och motstå behandling.
Varför de farligaste formerna är märkligt instabila
Underligt nog är de APOBEC3-enzymer som starkast förknippas med cancer också de minst stabila. Till skillnad från deras cytoplasmatiska kusiner—som ackumuleras i höga nivåer och effektivt blockerar virus—bryts A3A, A3B och A3H-I snabbt ned och förekommer vanligtvis i låga koncentrationer i kärnan. Forskarna antog att denna instabilitet kan vara avsiktlig: om celler aktivt begränsar nivåerna av nukleära APOBEC3-proteiner, kan ett brott i den kontrollen släppa loss vågor av mutagenes. Med A3H-I som modell visade de att cancerassocierade APOBEC3 huvudsakligen förstörs av proteasomen, cellens proteinförstörare, efter att ha märkts med små molekylära "flaggor" kallade ubiquitin på flera aminosyraresiduer.
Hitta de cellulära väktarna
För att identifiera maskineriet som ansvarar för att märka A3H-I och A3B kombinerade teamet CRISPR-screening med kartläggning av proteinproximitet. De konstruerade celler som lyser olika beroende på hur stabil A3H-I och dess ofarliga variant A3H-II är, och störde sedan systematiskt gener involverade i proteinnedbrytning. Tre ubiquitin-ligasar—UBR4, UBR5 och HUWE1—ständigt stack ut. Att slå ut någon av dessa ligasar höjde selektivt nivåerna av den instabila, nukleära A3H-I utan att påverka den stabila, cytoplasmatiska A3H-II. Samma ligasar ökade oberoende nivåerna av endogent A3B i kolon- och immuncellinjer, och att ta bort alla tre samtidigt gav en additiv uppgång i A3B-halt. Biokemiska experiment visade vidare att UBR5 och HUWE1 fysiskt binder till A3B och A3H-I och direkt fäster ubiquitinkedjor, medan UBR4 verkar specialisera sig på att förlänga dessa kedjor för att göra proteinerna mer effektivt disponibla.
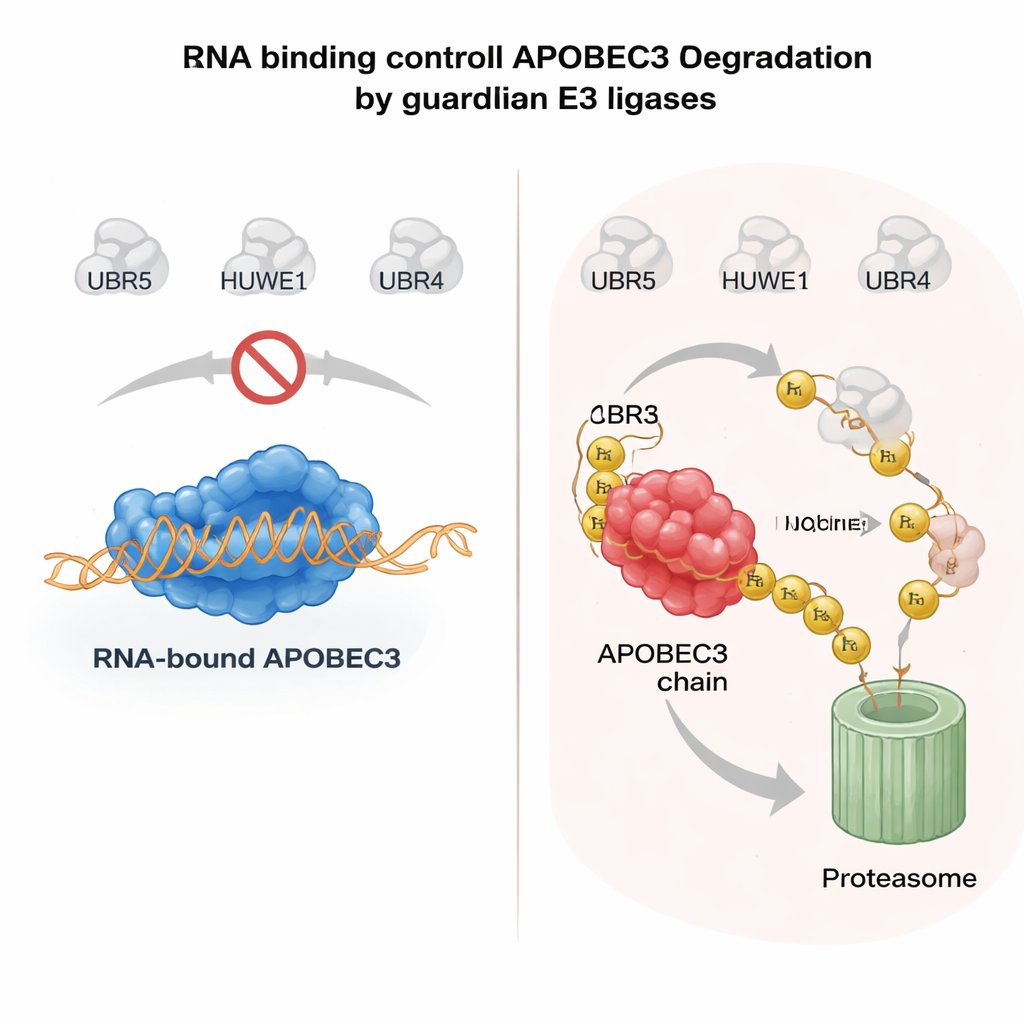
RNA som säkerhetsbälte för riskfyllda enzymer
Vad avgör om ett APOBEC3-enzym skonas eller förstörs? En viktig ledtråd kom från hur APOBEC3-proteiner fäster vid RNA-molekyler i cytoplasman. När A3H eller en annan familjemedlem, A3G, binder RNA tenderar de att förbli i stora komplex i cytosolen och är relativt stabila. Mutationer som försvagar RNA-bindningen gör att dessa enzymer driver in i kärnan, förlorar sina skyddande partners och blir mycket instabila. Författarna visade att när APOBEC3-proteiner inte är bundna till RNA, känner UBR5 och HUWE1 igen exponerade ytor på proteinet, dekorerar dem med ubiquitin och riktar dem för nukleär nedbrytning. I renade system förhöjde tillsats av RNas, som tar bort RNA, kraftigt dessa ligasers förmåga att binda och ubiquitinera APOBEC3, vilket bekräftar att RNA-bindning fungerar som en molekylär sköld. Denna mekanism tillåter celler att hålla antivirala APOBEC3 aktiva i cytoplasman samtidigt som de snabbt rensar bort alla obundna, genomhotande pooler i kärnan.
När väktarna sviktar: kopplingar till cancermutationer
Om UBR4, UBR5 och HUWE1 fungerar som väktare borde deras förlust öka mutationsnivåerna. Forskarna testade detta genom att inaktivera varje ligas i koloncancerceller och följa DNA-förändringar över tid med en känslig sekvenseringsmetod som läser mutatoriska "signaturer." Att ta bort dessa ligasar, särskilt i celler som uttrycker A3H-I, förstärkte APOBEC-specifika muteringsmönster—precis den typ som finns i mänskliga tumörer. Genom att analysera patientdata från tusentals cancergenom fann de att tumörer som bär mutationer i UBR5 eller HUWE1 hade en signifikant högre andel APOBEC-relaterade muteringssignaturer än tumörer med intakta ligasar, även efter att ha tagit hänsyn till total mutationsbörda. Detta tyder på att defekta väktarligasar hos patienter kan tillåta cancerassocierade APOBEC3-enzymer att löpa lösa och omforma tumörgenomet.
Vad detta betyder för framtida cancerbehandling
För en icke-specialist är slutsatsen att våra celler har ett sofistikerat övervakningssystem för att förhindra att hjälpsamma antivirala enzymer av misstag saboterar vårt eget DNA. UBR4, UBR5 och HUWE1 fungerar som väktare som känner av när APOBEC3-enzymer inte längre är säkert bundna till RNA och, särskilt i kärnan, skickar dem till cellens shredder. När detta kontrollsystem försvagas—genom mutationer i ligasarna eller genom läkemedel som blockerar proteinnedbrytning—kan APOBEC3-aktivitet driva den genetiska kaos som driver cancerutveckling och behandlingresistens. Att förstå detta väktarnätverk öppnar dörrar för nya diagnostiska markörer, såsom ligasmutationer eller APOBEC-proteinnivåer, och antyder att en noggrann justering av denna väg en dag kan hjälpa till att begränsa skadliga mutationsutbrott i tumörer utan att kompromettera vårt antivirala försvar.
Citering: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Nyckelord: APOBEC3, genomstabilitet, ubiquitinligas, cancermutagenes, proteinnedbrytning